ÁREA: Alimentos
TÍTULO: Comparação dos aspectos físico-químicos dos méis da abelha Apis mellifera de regiões e floradas distintas.
AUTORES: Araujo Neto, J.A.M. (UECE) ; Liberato, M.C.T.C. (UECE) ; Silva, L.C. (UECE)
RESUMO: O mel é a substância viscosa, aromática e açucarada obtida a partir do néctar
das flores das plantas que as abelhas melíferas produzem. Para atestar a boa
qualidade do mel é necessário análise de alguns parâmetros que impedem ao
consumidor o uso de um produto adulterado. O objetivo desse trabalho foi
focalizar a atenção em alguns testes físico-químicos que avaliam a qualidade de
um mel de abelha. Um exemplo de teste é o teste de cor, no qual o resultado foi:
com o mel de Lavras da Mangabeira apresentando cor Âmbar escuro (absorbância
450: 1,113 e Absorbância 720: 0,077; diferença: 1,036) e o de Serra do Perreiro
apresentando cor Âmbar (absorbância 450: 0,516 e absorbância 720: 0,107;
diferença: 0,409) Assim concluímos que o Mel de Lavras da mangabeira apresenta
uma coloração mais forte.
PALAVRAS CHAVES: mel; Apis mellifera; Prop. Físico-Químicas
INTRODUÇÃO: Mel é o produto alimentício produzido pelas abelhas melíferas a partir do néctar
das flores, das secreções procedentes de partes vivas das plantas ou de
excreções de insetos sugadores de plantas que ficam sobre partes vivas das
plantas. Para um mel de boa qualidade é essencial observar-se alguns aspectos.
Um deles, a determinação qualitativa do conteúdo de proteínas em amostras de
mel, é feita usando-se o Teste de Lund. Este teste baseia-se na precipitação de
proteínas naturais do mel pelo ácido tânico (IAL, 1985). Na presença de mel
adulterado, não haverá formação de depósito ou ele será desprezível. Um depósito
acima de 3,0 mL indica que o mel é de má qualidade.A reação de Lugol é um teste
simples para a detecção de fraude em mel por adição de glucose comercial, que é
uma reação colorimétrica qualitativa (IAL, 1985). A coloração é a primeira
característica atrativa do mel. A cor, o sabor e O aroma são fatores de
atratividade importantes para comercialização do mel. A cor do mel líquido pode
variar do branco aquoso a uma cor marrom bem escuro, próximo de preto, com
variantes tendendo para matizes de verde ou vermelho, ou mesmo azul (CRANE,
1983). O armazenamento por tempo prolongado sob condições de alta temperatura
dará origem ao hidroximetilfurfural, promovendo alteração na cor do mel (CRANE,
1983). Muxfeld (1970) afirma que as abelhas colhem a clorofila, o caroteno, a
xantofila, a antocianina, o tanino, partículas coloidais e derivados benzóicos,
podendo assim, vir a compor o padrão de cor do mel. Os pigmentos presentes nos
grãos de pólen contribuirão para formação da cor do mel (LABORIAU, 1973).
MATERIAL E MÉTODOS: Obtenção das amostras: Méis de Apis mellifera, de origens geográficas e
botânicas diferentes, foram obtidos nas cidades de Lavras de mangabeira – CE
(florada: silvestre) no período de Novembro de 2011 e Serra do Pereiro (Morada
Nova – CE) (florada: nativa). As amostras foram coletadas na estação das chuvas
no período de Fevereiro de 2012. Reação de Lund: baseia-se na precipitação de
proteínas naturais do mel pelo ácido tânico (IAL, 2005). O procedimento indica a
pesagem de 2g de amostra que são transferidas para uma proveta com rolha
esmerilhada, com o auxílio de 20 mL de água. Adiciona-se em seguida quantidade
de água suficiente para completar o volume de 40 mL. Agita-se e deixa-se
repousar por 24 horas. Na presença de mel puro, forma-se um depósito de 0,6 a
3,0 mL. Na presença de mel adulterado, não haverá formação de depósito ou ele
será desprezível. Um depósito acima de 3,0 mL indica que o mel é de má
qualidade. Reação de Lugol: é um teste que detecta fraude em mel por adição de
glicose comercial, É uma reação colorimétrica qualitativa. Pesa-se 10 g de
amostra em um béquer de 50 mL. Adiciona-se 20 mL de água e agita-se. Deixa-se no
banho-maria fervente por 1 h e resfria-se à temperatura ambiente. Após resfriar,
adiciona-se 5 a 10 gotas da solução de Lugol. Na presença de glicose comercial,
a solução ficará marrom-avermelhada à azul. A intensidade da cor depende da
qualidade e da quantidade das dextrinas presentes na glicose comercial ou amido.
Teste de coloração: foi feito espectrofotometricamente (Biomate
Spectrophotometer) nos comprimentos de onda de 450nm e 720nm fazendo-se em
seguida a subtração para se obter a indicação da cor (BERETTA et al., 2005).
RESULTADOS E DISCUSSÃO: As Analises feitas mostraram que com o teste de Lund o mel de Lavras da mangabeira
- CE resultou em uma nuvem de proteínas chegando a 3,3 mL, mas sem apresentar uma
real deposição, desta forma concluímos que o mel é de baixa qualidade, e o mel de
Serra do Pereiro (Morada Nova – CE) obteve-se uma deposição de 0,4 ml o que faz
esse resultado ser de um mel adulterado também, pois o parâmetro mostra que o mel
não é adulterado com uma deposição entre 0,6ml e 3,0ml de deposição, já o teste de
Lugol mostrou que em ambos os méis não houve uma mudança significativa na cor,
comprovando que não foram adulterados com a adição de açúcar industrializado, e
por fim na coloração os méis apresentam cores âmbar escuro e âmbar como mostra a
tabela 1.
Tabela 1
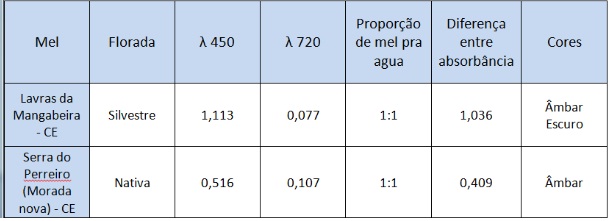
Tabela da diferença de coloração entre o mel de
Lavras da Mangabeira - CE e o mel de Serra do
Perreiro(morada nova) - CE.
CONCLUSÕES: A presença de uma nuvem de proteínas com nível maior que 3,0 ml indicou a
adulteração do mel oriundo de Lavras da Mangabeira. As diferenças de absorbâncias
obtidas espectrofotometricamente(com o aparelho Biomate 5;Biomate V7.07;Serial nº
150304) que foi para o mel de Lavras da mangabeira: absorbância 450: 1,113 e
Absorbância 720: 0,077; diferença: 1,036 o que denota em uma cora âmbar escuro e o
mel de Serra do Perreiro: absorbância 450: 0,516 e absorbância 720: 0,107;
diferença: 0,409 o que denota em uma cor âmbar.
AGRADECIMENTOS: Universidade Estadual do Ceará-UECE
REFERÊNCIAS BIBLIOGRÁFICA: BERETTA, G.; GRANATA, P; FERRERO, M.; ORIOLI, M.; FACINO, R. M. Standardization of antioxidant properties of honey by a combination of spectrophotometric/fluorimetric assays and chemometrics. Analytica Chimica Acta 533, p.185-191, 2005.
CRANE, E. O livro do mel. São Paulo: Nobel, 1983.
INSTITUTO ADOLFO LUTZ (IAL), (1985). Normas Analíticas do Instituto Adolfo Lutz. Vol. 1 Métodos Químicos e Físicos para Análise de Alimentos. São Paulo: IAL, 1985.
LABORIAU, M. L. S. A contribuição à palinologia dos cerrados. Academia Brasileira de Ciências, Rio de Janeiro, 1973. 219p.
MUXFELD, H. Apicultura para todos. 2ª Ed. Porto Alegre: Sulina, 1970. 303p.
