ÁREA: Bioquímica e Biotecnologia
TÍTULO: DESENVOLVIMENTO DE BIOSSENSOR ELETROQUÍMICO PARA DETECÇÃO DO PESTICIDA DICLORVÓS
AUTORES: Chagas, I.A.L. (UPE) ; Silva, M.M.S. (UFPE) ; Dias, A.C.M.S. (UFPE) ; Cavalcanti, I.T. (UFPE) ; Dutra, R.F. (UFPE)
RESUMO: O pesticida organofosforado diclorvós tem sido largamente utilizado na agricultura, na pecuária e no cultivo de peixes a fim de eliminar os parasitas. Sua toxicidade pode ser observada através da atividade reduzida da enzima acetilcolinesterase (AChE). Os biossensores são considerados instrumentos analíticos alternativos devido a sua alta sensibilidade e seletividade. Neste trabalho, propõe-se o emprego de um eletrodo de carbono vítreo modificado com filme de Nafion/AChE para a determinação do diclorvós, usando a técnica de voltametria cíclica. A influência do pesticida foi avaliada, revelando um decréscimo de 63,58% e 92,29% na atividade enzimática da AChE. Este trabalho apresenta resultados satisfatórios no desenvolvimento de um método sensível e rápido para detecção do pesticida.
PALAVRAS CHAVES: Biossensor; pesticida; enzima
INTRODUÇÃO: Os organofosforados constituem uma das mais importantes classes de pesticidas, sendo frequentemente utilizados no combate a insetos que atacam frutos e hortaliças. Sua intensa utilização, inclusive em campanhas municipais de controle de insetos, como no caso do mosquito da dengue, faz com que esta classe de pesticida esteja envolvida em grande parte dos casos de envenenamento, devido a seus efeitos nocivos à saúde como, por exemplo, efeitos teratogênicos (VEIGA et al, 2006). O organofosforado diclorvós possui um efeito toxicológico leve em seres humanos, porém, em altas quantidades, ataca o sistema nervoso central. O principal problema relacionado à utilização deste pesticida é que o emprego exagerado, tanto doméstico como na agricultura e pecuária, faz com que a contaminação humana se torne muito freqüente. Técnicas de cromatografia normalmente empregadas para a determinação do pesticida são consideradas sensíveis e confiáveis, mas apresentam alguns inconvenientes como, por exemplo, o complexo e trabalhoso tratamento das amostras. Além disso, só podem ser executados por profissionais devidamente treinados e não são práticos para utilização em campo (BOSSI, 2002). Logo, a aplicação do biossensor constitui uma estratégia rápida e conveniente para medidas do diclorvós. A modificação de eletrodos de carbono vítreo (ECV) com filme de Nafion/enzima acetilcolinesterase (AChE) foi realizada, podendo conferir ao biossensor uma maior sensibilidade, seletividade, e estabilidade, com obtenção de respostas em tempo real.
MATERIAL E MÉTODOS: O ECV foi imerso em uma solução de Nafion 1% diluído em etanol 95%, por 50 minutos. Para caracterização do filme de Nafion foram utilizadas diferentes concentrações do polímero (0,01; 0,05; 0,1; 0,5 e 1%). Após essa etapa, o ECV foi imerso em solução de L-lisina 3 mM por 1 hora, para adsorção da mesma. Uma solução de 1 μg/mL da AChE foi aplicada sobre a superfície do ECV modificado, e mantida por 2 horas. A técnica de voltametria cíclica foi registrada usando um potenciostato Ivium® (CompactStat, Ivium Technologies). Todos os experimentos foram realizados em tampão fosfato salino (PBS, pH 7,4) 10 mM, contendo 5 mM do complexo redox ferricianeto e ferrocianeto de potássio (proporção de 1:1), variando-se o potencial entre -0,4 e +0,8 V, com velocidade de varredura de 100 mV/s. Através da voltametria cíclica, foram avaliadas as mudanças na concentração do substrato iodeto de acetiltiocolina, utilizando o eletrodo modificado (ECV/Nafion/L-lisina/AChE). Para investigar a influência do diclorvós na atividade enzimática da AChE, foram realizadas leituras do ECV/Nafion/L-lisina/AChE na ausência e presença do pesticida. As soluções de diclorvós foram preparadas a partir de uma solução de 2 mM em água destilada com 2% de dimetil sulfóxido (DMSO) (Sigma-Aldrich, EUA).
RESULTADOS E DISCUSSÃO: Inicialmente a AChE foi caracterizada cineticamente quanto à sua afinidade com o substrato iodeto de acetiltiocolina, através do modelo de hiperbólico (Fig. 1). Foi determinada a constante de Michaelis-Mentem (Km), correspondente a 0,45 mM e também a velocidade máxima da hidrólise (Vmax) de 67,82 Unidades (U) por miligramas de proteína, sendo U definida como μM de substrato hidrolisado por mL por minuto. O efeito do diclorvós sobre a atividade da AChE livre foi observado. A inibição de 50% da atividade colinesterásica (CI50) frente ao pesticida em questão foi estimada (0,16 μM), demonstrando ser o mesmo um forte inibidor da enzima utilizada. O comportamento da AChE em várias concentrações de iodeto de acetiltiocolina (2,5; 7,5; 10; 15; 22,5; 25 mM) foi estudado. Observou-se que a intensidade da corrente dos picos anódico e catódico aumentou gradativamente com o aumento da concentração do substrato da enzima (Fig. 2), confirmando que a enzima imobilizada na superfície do ECV manteve uma elevada atividade enzimática, passível de ser quantificada eletroquimicamente. A determinação do pesticida está relacionada com a inibição da AChE, a qual é resultante da ligação irreversível da molécula ao sítio ativo da enzima. Inicialmente, a reação de oxidação da enzima com o substrato no eletrodo gera uma corrente elétrica constante e proporcional à concentração do substrato. A adição do pesticida à solução provocou a inibição na atividade da enzima, e por consequência, reduziu a densidade da corrente gerada no eletrodo. Isto pode ser avaliado pela redução dos picos do voltamograma cíclico.
Fig. 1
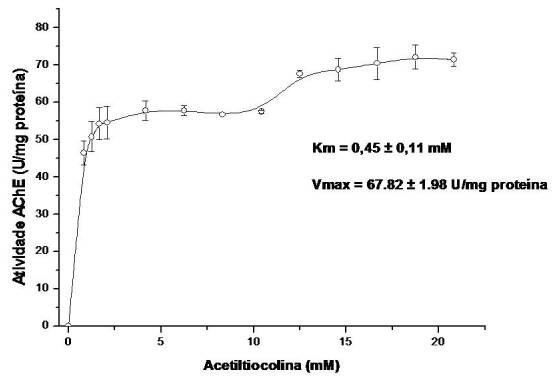
Gráfico de cinética de Michaelis-Mentem da enzima AChE solúvel utilizando o substrato iodeto de acetiltiocolina.
Fig. 2
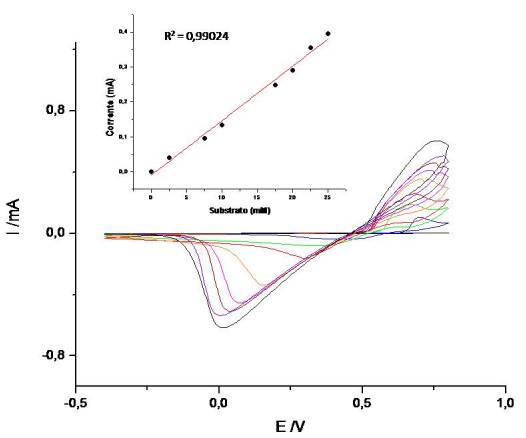
Voltamogramas cíclicos do ECV/Nafion/L-lisina/AChE nas diferentes concentrações do iodeto de acetiltiocolina (2,5, 7,5, 10, 15, 22,5, 25 mM).
CONCLUSÕES: A inibição da atividade enzimática pelo pesticida diclorvós foi obtida, com um percentual de 63,58% e 92,29% nas concentrações 0,5 e 10 μg/mL, respectivamente. O biossensor eletroquímico proposto obteve resultados satisfatórios através do desenvolvimento de um método simplificado para detecção do pesticida diclorvós, abrindo perspectivas para realização do monitoramento de contaminação de pesticidas em amostras de águas naturais.
AGRADECIMENTOS: A Capes, CNPQ, FACEPE pelo auxílio financeiro.
REFERÊNCIAS BIBLIOGRÁFICA: BOSSI, R.; VEJRUP,K.V.; MOGENSEN,B.B.; ASMN,W.A.H. 2002. Analysis of polar pesticides in rainwater in Denmark by liquid chromatography-tandem mass spectrometry. Journal of chromatography A,957: 26-36.
VEIGA, M.M.; SILVA, D.M.; VEIGA, L.B.E.; FARIA, M.V.C. 2006. Análise da contaminação dos sistemas hídricos por agrotóxicos numa pequena comunidade rural do Sudeste do Brasil. Cadernos de Saúde Pública, 22: 2391-2399.
