ÁREA: Materiais
TÍTULO: Programa Computacional como Ferramenta para Análise Química do Gesso
AUTORES: Vasconcelos, R.S. (UNICAP) ; Henauth, R.C.S. (UNICAP) ; Santos, V.A. (UNICAP)
RESUMO: Foi desenvolvido um programa em linguagem Matlab para substituir a realização de
exaustivo número de análises químicas de um gesso obtido por desidratação
térmica do minério gipsita. A composição percentual de um gesso contendo apenas
semi-hidrato de sulfato de cálcio (gesso) é de 6,21 % de água combinada, 38,62 %
de óxido de cálcio e 55,17 % de anidrido sulfúrico. Contudo, deve-se levar em
conta a ocorrência de teores de certas impurezas existentes nos minérios de
gipsita, tais como o MgCO3 e CaCO3. O programa desenvolvido correlaciona os
teores de impurezas e de CaSO4, permitindo o cálculo dos teores simultâneos de
di-hidrato, semi-hidrato e anidrita, fornecendo dados necessários ao cálculo do
teor de aditivos e anidrita II.
PALAVRAS CHAVES: Gesso; Análise Química; Matlab
INTRODUÇÃO: Teoricamente, se as condições de temperatura para a obtenção do gesso (CaSO4 ⋅
0,5H2O) por desidratação térmica do minério de gipsita fossem homogêneas, em
todo o meio reacional, toda a gipsita passaria a semi-hidrato. Na prática
entretanto, essas condições são heterogêneas, podendo ocorrer pontos dentro do
reator com temperaturas acima ou abaixo daquela desejada (PERES; BENACHOUR;
SANTOS, 2008; BALTAR; BASTOS; BORGES, 2004). Quando em algum ponto do reator a
temperatura não atinge o valor adequado, na massa do produto final fica retida
uma certa quantidade de di-hidrato. Por outro lado, se houver pontos com
temperaturas superiores, parte do material é transformado em anidrita. Nas
massas finais dos gessos produzidos por desidratação térmica da gipsita,
justifica-se, então, a existência de misturas compostas apenas de anidrita e
semi-hidrato ou, di-hidrato e semi-hidrato ou, simplesmente semi-hidrato. Os
métodos de análises de gesso apresentados na literatura para determinação dos
teores de semi-hidrato, anidrita e di-hidrato em gessos, podem ser de natureza
física ou química (CASPAR, 1996; NINAN, 1989; WENDLANDT, 1986). Os primeiros
constam basicamente em submeter as amostras desse material a ambientes úmidos,
nos quais as amostras dificilmente adquirem os graus de hidratação desejados. As
pequenas variações de composição do minério de gipsita permitem que se possa
fazer previsões com cerca de 1,5 %, sobre os teores de componentes em um minério
de gipsita, em regiões pertencentes a uma mesma mina (SANTOS, 1996). Dessa forma
o presente trabalho tem como objetivo o desenvolvimento de um programa
computacional para reduzir as dificuldades de se analisar grandes números de
amostras de gesso, com base na composição média da gipsita em uma lavra.
MATERIAL E MÉTODOS: Preliminarmente, três princípios básicos devem ser observados para auxiliar na
interpretação dos resultados fornecidos pela análise de um gesso: i) Os
carbonatos de cálcio e magnésio não se decompõem durante a desidratação térmica
para obtenção do semi-hidrato, pois a temperatura alcançada para esta reação não
é suficiente para as decomposições desses carbonatos; ii) Todo MgO é proveniente
do MgCO3 e; iii) Todo CO2 origina-se das decomposições do CaCO3 e do MgCO3. Para
se chegar às expressões de cálculo a serem utilizadas no programa computacional
proposto neste trabalho, as seguintes considerações foram necessárias:
- O MgCO3 dissocia-se segundo a estequiometria:
MgCO3(s) → CO2(g) + MgO(s)
- O CO2 origina-se da decomposição do CaCO3 a partir de reação:
CaCO3(s) → CO2(g) + CaO(s)
- Para se chegar às expressões de cálculo dos teores percentuais de anidrita,
semi-hidrato e di-hidrato, faz-se necessário o cálculo do CaO disponível para
formação do CaSO4, ou seja, da quantidade de CaO que excede àquela que compõe o
CaCO3, combinando-se com o SO3;
- O CaO disponível para formação do CaSO4 pode estar ainda em excesso com
relação ao SO3, e se não houver CaO disponível nem SO3 em excesso, isso
significa que estão totalmente combinados entre si;
- O SO3 combina-se mol a mol com o CaO disponível e para que não existam CaO ou
SO3 em excesso, a relação entre os percentuais desses dois componentes deve ser
igual a 0,7;
- A correlação entre o SO3 e o CaO disponível, qualquer dos dois em excesso,
deve então ser analisada para valores maiores ou menores que 0,7 e;
- Para finalizar, cada possibilidade para valores previstos pelas duas últimas
suposições, devem ser analisados os caso de existência de semi-hidrato apenas,
semi-hidrato e di-hidrato e semi-hidrato e anidrita.
RESULTADOS E DISCUSSÃO: Os dados de entrada para testes do programa computacional foram obtidos a partir
de uma análise química de uma amostra de gipsita e são apresentados na tabela da
Figura 1. O minério utilizado apresentou pureza da ordem de 95 %. O gráfico da
Figura 2 apresenta valores para teores de semi-hidrato e di-hidrato para
diferentes níveis de água de hidratação no gesso, obtido com auxílio de uma
balança térmica que usa a técnica de infravermelho, produzida pela GEHAKA,
modelo IV 2000.
O programa forneceu dados sobre os percentuais de anidrita, semi-hidrato e di-
hidrato com a variação da água de hidratação no gesso produzido. Esses valores
de água variaram de 10 % a 3 %, uma vez que o valor máximo encontrado na gipsita
era de 19,1 %, conforme tabela da Figura 1. A medida em que a água de hidratação
vai sendo reduzida, em torno de 10 % o teor de di-hidrato é de 27,04 % e o de
anidrita encontra-se ainda nulo. Ao atingir cerca de 6 % o valor de anidrita já
será de 1,46 %, enquanto o teor de di-hidrato reduz-se a zero. portanto, o teor
de semi-hidrato passa por um valor máximo entre 6 % e 7 % para a água de
hidratação no gesso. Juntamente com esses dados o programa pode ainda fornecer
valores de excesso de CaO ou SO3, o que pode caracterizar o tipo de gesso
formado quanto à interação com o tipo de tinta utilizada na pintura sobre esse
gesso.
Dados da análise química da gipsita utilizada na produção de gesso
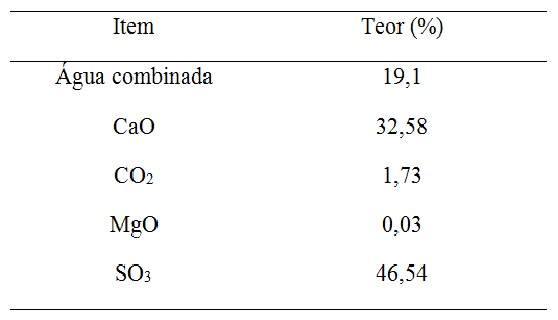
Dados para a entrada do programa computacional
Teores de anidrita di-hidrato e semi-hidrato no gesso analisado
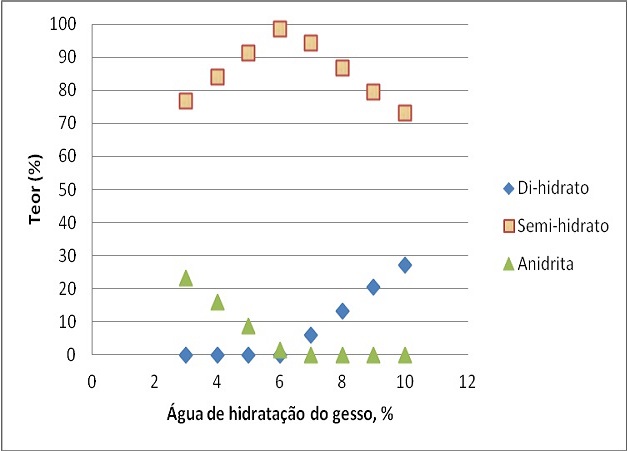
Resultados da simulação
CONCLUSÕES: O método de análise desenvolvido tem como base as estimativas dos teores
percentuais de semi-hidrato, di-hidrato, anidrita e excesso de anidrido sulfúrico
e óxido de cálcio. Apresenta-se como uma opção vantajosa, porque foi elaborado
para a realização de análises com grandes quantidades de amostras e considerável
redução no exaustivo número das mesmas, requeridas pelos métodos convencionais. O
método proposto substitui as longas e dispendiosas análises de laboratório
necessitadas normalmente para todas as amostras.
AGRADECIMENTOS: Os autores são gratos a Universidade Católica de Pernambuco - UNICAP pela
oportunidade de participação no 52º Congresso Brasileiro de Química.
REFERÊNCIAS BIBLIOGRÁFICA: BALTAR, C. A. M; BASTOS, F. F.; BORGES, L. E. P. Variedades Mineralógicas e Processos Utilizados na Produção dos Diferentes Tipos de Gesso. In.: Encontro nacional de tratamento de minérios e metalurgia extrativa. Anais: Florianópolis, 2004. p.329.
CASPAR, J.; DANY, C.; AMATHIEU, L.; REINAUT, P.; FANTOZZI, G. Influence of the Microstructure of set Plaster on its Mechanical Properties. Versailles: Euro gypsum – XXI Congress, 1996.
NINAN, K. N., Kinetics of solid state-thermal decomposition reactions, Journal of Thermal Analysis, 35, 1267-1278, 1989.
PERES, L; BENACHOUR, M.; SANTOS, V. A. O GESSO: Produção e Utilização na Construção Civil. Recife: SEBRAE, 2008.
SANTOS, V. A., Análise cinética da reação de desidratação térmica da gipsita na obtenção do gesso beta. Tese de Doutorado. Departamento de Engenharia de Sistemas Químicos e Informática. Universidade Estadual de Campinas. Campinas: 1996. 170 p.
WENDLANDT, W. W., Thermal Methods of Analysis, 3rd ed., N. York: J. Wiley, 1986.
