ÁREA: Ambiental
TÍTULO: Estudo do pH no processo de remoção do corante Verde Brilhante sobre Ligno-Celulose em solução aquosa.
AUTORES: Matos, N. (UFPA) ; Rodrigues, H. (UFPA) ; Araújo Jr., E. (UFPI) ; Moura, J. (UFPI) ; Silva Filho, E. (UFPI) ; Cláudio Lima, (UFRGS) ; Alencar, W. (UFPA)
RESUMO: Realizou-se um estudo da variação do pH da solução aquosa do corante Verde
Brilhante no processo de adsorção sobre Ligno-Celulose proveniente do talo do
cacho do açaí in natura. Verificou-se que o processo de adsorção era favorecido
com o aumento do pH da solução. As forças de Coulomb são as mais importantes no
processo de adsorção pois a ligno-celulose em pH elevado apresenta caráter
aniônico e o corante catiônico. Nesse trabalho, obteve-se resultados de 90% e 99%
de remoção do corante em pH igual a 5,0 e 9,0, respectivamente.
PALAVRAS CHAVES: Ligno-celulose; corante; adsorção
INTRODUÇÃO: No século 21, a poluição ambiental tem sido uma das principais ameaças à vida
humana. Entre os diferentes tipos de poluição, o fluxo de águas residuais é um
dos principais problemas devido a grande quantidade de água utilizada em
residências, hospitais, indústrias e outros. Águas residuais contendo corante,
oriunda de indústrias têxteis e gráficas, tem sido uma das principais fontes de
poluição da água (ROYER et al.,2009). As aplicações de corantes e pigmentos têm
aumentado de um modo considerável nos últimos anos (ROYER et al.,2009). Uma
serie de indústrias têm sido criadas e com isso tem atenuando a demanda contínua
e crescente de corantes e pigmentos. Os corantes são utilizados nas indústrias
têxteis, de alimentos, bebidas industriais e processos de impressão (CARDOSO et
al., 2011). O consumo total de corante da indústria têxtil em todo o mundo esta
em excesso de 107 Kg por ano (CALVETE et al., 2010). No entanto, aproximadamente
um milhão de kg por ano de corantes é descarregado em correntes de água pela
indústria têxtil (CALVETE et al, 2010). A presença de corantes em águas, provoca
sérios problemas ao ecossistema aquático, desde a diminuição de oxigênio como
também a variação do pH da água, além de muitos serem agentes carcinogênicos
(CARDOSO et al, 2011). Estudos de adsorção de corantes tem sido realizado usando
desde carvão ativo e processos eletroquímicos ou de membranas até o uso de
resíduos vegetais (ALENCAR et al, 2012). Este último apresenta-se como uma
alternativa de baixo custo e eficiente tão quanto aos demais métodos levando em
conto a relação custo-benefício. Neste trabalho, é apresentado um estudo da
variação do pH da solução aquosa do corante verde brilhante no processo de
adsorção sobre ligno-celulose proveniente do talo do açaí
MATERIAL E MÉTODOS: Foi utilizada água deionizada ao longo dos experimentos para preparações de
soluções. O corante Verde Brilhante (VB, CI - 42040, CAS - 633-03-4,
C27H34N2O4S, 482,64 g/mol). A solução estoque foi preparada pela dissolução do
corante em água destilada obtendo uma concentração de 5,0 g/L. As soluções de
trabalho foram obtidas pela diluição da solução estoque do corante para as
concentrações desejadas (ALENCAR et al, 2012). Neste sentido, para ajustar o pH
das soluções, foram utilizadas soluções 0,10 mol/L NaOH e/ou HCl. Para manter
estabilizado o pH, foram usadas também soluções tampão. O pH das soluções foram
medidos usando um pHmetro fixo SCHOTT Lab-850.
O talo do cacho do açaí (biossorvente) foi adquirido em um sítio de Marabá-PA.
Os resíduos foram lavados em água em água deionizada. O biossorvente foi seco a
70 °C em uma estufa por 8 horas (ROYER et at, 2010). Após a secagem, o material
foi triturado em um moinho de facas e peneirado com rendimento de 95%. Foi usada
a porção do biossorvente que apresentou diâmetro de partículas < 250 µm.
O estudo de remoção do corante em soluções de pH diferentes foi realizado usando
o método de contato direto dos grupos, conforme proposto na literatura (Royer et
al, 2009). A concentração final dos corantes remanescentes na solução foi
determinada por espectrofotometria visível usando um Espectrofotômetro T90+ UV-
VIS fornecido pela PG Instruments (Londres, Ingraterra), equipado com células
ópticas (cubetas) de quartzo. As medidas de absorbância foram feitas no
comprimento de onda máximo do corante.
A quantidade do corante adsorvido e a porcentagem de remoção de corante pelo
biossorvente foram calculadas pela aplicação das equações (q = [(Co - Cf)/m].V)
e (% Remoção = 100.[(Co - Cf)/Co]).
RESULTADOS E DISCUSSÃO: Um dos fatores mais importantes em estudos de adsorção é o efeito da acidez do
meio (ALENCAR et al, 2012). Espécies diferentes podem apresentar faixas
divergentes de pH adequado, dependendo do adsorvente que é utilizado. Nesse
sentido, foi avaliado dentro da faixa de pH entre 1 a 9, o percentual de remoção
do corante VB usando o biossorvente Ligno-Celulose proveniente do talo do cacho
do açaí (figura abaixo) a fim de entender a importância do pH no processo de
remoção do contaminante VB. O percentual de remoção do corante aumentou
notavelmente do pH 1,0 (45%), atingindo 99 % em pH 9,0. Comportamento semelhante
na remoção de corantes catiônicos utilizando adsorventes ligno-celulósicos
também tem sido observado (ROYER et al, 2010). A variação da percentagem de
remoção é mais claramente observada na tabela abaixo. Através da tabela acima, é
possível afirmar que o aumento do potencial hidrogeniônico da solução do corante
favoreceu grandemente ao processo de adsorção.
O corante VB dissolvido em água apresenta cargas positivas, devido seus
grupos amino protonados. A adsorção deste corante ocorre quando o biossorvente
apresenta uma carga negativa em sua superfície. Em pH 9,0; estes materiais
ligno-celulósicos apresentam carga negativa na superfície (ROYER et al, 2010),
possibilitando assim a formação de bases de Bronsted ou sítios de Lewis. Este
comportamento explica a capacidade de adsorção elevada da ligno-celulose para o
corante VB, em solução pH 9,0. Este fato revela a importância de conhecer o pH
ideal para a remoção de um corante poluente em águas. Nesse caso, a partir do pH
4,0 é possível uma remoção acima de 90%.
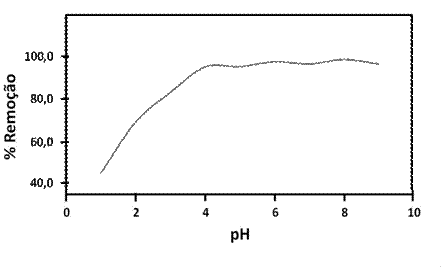
FIGURA. Efeito do pH na remoção do corante VB sobre
Ligno-Celulose. Condições:Co = 20,0 mg/L do corante
VB em solução: 2,5 g/L; T=298 K, t= 5 h.
TABELA. Comparação dos valores da percentagem de remoção com a variaçã

CONCLUSÕES: O estudo de pH no processo de remoção do corante Verde Brilhante, sobre ligno-
celulose oriunda do talo do cacho do açaí, releva que o percentual de remoção é
dependente das condições da água, principalmente da concentração de íons H3O+ em
solução. O melhor pH para remoção desse contaminante em águas foi o pH 9,0, onde
obteve-se um percentual de 99% de remoção. A ligno-celulose proveniente do açaí,
demonstrou ser um excelente material alternativo na remoção do corante verde
brilhante.
AGRADECIMENTOS: A UFPA pela bolsa concedida pelo projeto PAPIM 2011.
REFERÊNCIAS BIBLIOGRÁFICA: ALENCAR, W. S.; LIMA, E. C.; ROYER, B.; SANTOS, B. D.; CALVETE, T.; SILVA, E. A.; ALVES, C. N. Application of aqai stalks as biosorbents for the removal of the dye Procion Blue MX-R from aqueous solution. Separation Science and Technology, v. 47, p. 513-526, 2012.
CALVETE, T.; LIMA, E. C.; CARDOSO, N. F.; DIAS, S. L. P.; RIBEIRO, E. S. Removal of brilliant Green dye from aqueous solutions using home-made activated carbons. Clean: Soil, Air, Water, v. 38, p. 521-532, 2010.
CARDOSO, N. F.; LIMA, E. C.; PINTO, I. S.; AMAVISCA, C. V.; ROYER, B.; PINTO, R. B.; ALENCAR, S. A.; PEREIRA, S. F. P. Application of cupuassu Shell as biosorbente for the removal of textile dyes from aqueous solution, Journal of Environmental Management, v. 92, p. 1237-1247, 2011.
ROYER, B.; CARDOSO, N. F.; LIMA, E. C.; VAGHETTI, J. C. P.; SIMON, N. M.; CALVETE, T.; VESES, R. C. Applications of Brazilian-pine fruit Shell in natural and carbonized forms as adsorbents to removal of methylene blue from aqueous solutions – Kinetic and equilibrium study. Journal of Hazardous Materials, v. 164, p. 1213-1222, 2009.
ROYER, B.; CARDOSO, N. F.; LIMA, E. C.; MACEDO, T. R.; AIROLDI, C. A useful organofunctionalized layered silicate for textile dye removal. Journal of Hazardous Materials, v. 181, p. 366-374, 2010.
