Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Orgânica
TÍTULO: Estudo da relação estrutura-atividade de maleimidas análogas via cálculos teóricos e análise quimiométrica.
AUTORES: Tavares, L.A. (UFES) ; Nascimento Jr, C.S. (UFSJ) ; Potasio, M.P. (UFES) ; Velloso, M.H.R. (UFES)
RESUMO: Cálculos de estrutura eletrônica e análise quimiométrica foram realizados a fim de se estudar a relação estrutura-atividade de oito maleimidas. É conhecido da literatura, que das oito maleimidas estudadas, três apresentam atividade analgésica e cinco não apresentam tal atividade. A análise de componentes principais e a análise por agrupamentos hierárquicos foram aplicadas aos parâmetros físico-químicos descritores obtidos via cálculos teóricos (entalpia, logP, momento de dipolo, massa molecular e volume) para classificar os compostos de acordo com a presença ou não da atividade analgésica. Segundo os resultados, concluiu-se que os métodos quimiométricos foram capazes de distinguir os compostos ativos dos inativos e ainda identificar as variáveis mais relevantes para essa discriminação.
PALAVRAS CHAVES: Estrutura-Atividade; QSAR; Quimiometria
INTRODUÇÃO: As imidas cíclicas são compostos que apresentam o grupo –CO-N(R)-CO-, onde R pode ser um átomo de hidrogênio, um grupo alquila ou arila. Esta classe de compostos é conhecida devido as suas atividades biológicas, tais como bactericidas, fungicidas, inseticidas e analgésicas [1]. A ação terapêutica de fármacos resulta de interações químicas destes com sistemas biológicos e é dependente de fatores relacionados com sua estrutura química e, consequentemente, de suas propriedades físico-químicas. Estes fatores sejam eles de caráter eletrônico, hidrofóbico ou estérico, influenciam a interação do fármaco com a biofase e a sua distribuição nos compartimentos que compõem o sistema biológico. Assim, fármacos estruturalmente semelhantes, diferenciando-se apenas por algum substituinte ou posição que estes ocupam na molécula, podem apresentar diferenças em suas propriedades físico-químicas e, consequentemente, em suas atividades biológicas. A metodologia sequencial de modelagem molecular baseada em estudos QSAR “Quantitative Structure-Activity Relationship” [2] em conjunto com análises quimiométricas, tem sido usada para descrever quantitativamente as relações entre a estrutura química de moléculas e a atividade biológica por elas desempenhadas, visando a identificação de valores ótimos para determinadas propriedades físico-químicas e, por meio deles, fundamentar o planejamento de novas substâncias que possuam perfil terapêutico mais adequado às necessidades atuais. Nesse trabalho, métodos quimiométricos foram aplicados a diversos parâmetros físico-químicos (entalpia, logP, momento de dipolo, massa molecular e volume) com o objetivo de se estudar a relação estrutura-atividade das distintas maleimidas, discriminando assim aquelas ativas quanto ao efeito analgésico, daquelas inativas.
MATERIAL E MÉTODOS: No presente trabalho, oito maleimidas análogas (etilmaleimida, propilmaleimida, sec-butilmaleimida, dietilmaleimida, pirrolidinamaleimida, piperidinamaleimida e piperazinamaleimida ) foram submetidas a cálculos de otimização de geometria, na fase gasosa, através da Teoria do Funcional de Densidade (DFT), com o funcional B3LYP e um conjunto de base contendo funções de polarização d e p em todos os átomos (B3LYP/6-31G(d,p)). Propriedades termodinâmicas foram calculadas à 298K e 1 atm. Todos os cálculos de estrutura eletrônica, bem como dos parâmetros físico-químicos descritores, foram realizados através dos pacotes computacionais Gaussian 2009 e Hyperchem 8.0. A análise quimiométrica dos parâmetros físico-químicos foi realizada utilizando-se o programa Pirouette v.4.5. Na análise de componentes principais (PCA) foi aplicado o autoescalamento dos dados com o objetivo de atribuir a todas as variáveis a mesma importância quando avaliadas pelo programa. Na análise por agrupamentos hierárquicos (HCA) utilizou-se o método incremental como método de ligação entre os grupos.
RESULTADOS E DISCUSSÃO: Após obtenção dos parâmetros físico-químicos descritores, já citados anteriormente, via cálculos de estrutura eletrônica DFT, os dados foram submetidos a análises quimiométricas. A figura 1 exibe o gráfico de scores, que mostra a discriminação dos compostos ativos e inativos com relação à atividade analgésica. Observa-se que a PC2 é o fator responsável pela discriminação desses compostos. As maleimidas com atividade analgésica encontram-se em valores positivos de PC2 enquanto as maleimidas inativas apresentam valores negativos. A figura 2 mostra o gráfico de loadings, que indica quais variáveis do conjunto original contribuem para a discriminação observada no gráfico de scores. Nela pode ser observado que a variável momento de dipolo é a maior responsável pela separação dos compostos ativos contribuindo para que as maleimidas correspondentes tenham valores positivos em PC2, e as variáveis Entalpia e logP são as que mais contribuem para que os compostos inativos tenham valores negativos em PC2. Portanto, maleimidas contendo mais átomos eletronegativos e cadeias carbônicas substituintes menos volumosas, apresentaram baixos valores de logP, e contrariamente, altos valores do momento de dipolo. Isso mostra a correspondência entre as duas variáveis, sugerindo que maleimidas mais polares e, portanto, maleimidas que tem maiores afinidades pela fase aquosa, apresentam maior atividade analgésica. Com relação à variável entalpia, pode-se observar que as maleimidas estudadas apresentaram variações significativas nos valores, sendo, portanto, um parâmetro importante também na discriminação da atividade analgésica. A análise por agrupamentos hierárquicos (HCA) mostrou discriminação semelhante ao PCA, distinguindo as maleimidas ativas das inativas, quanto à atividade analgésica.
Figura 1
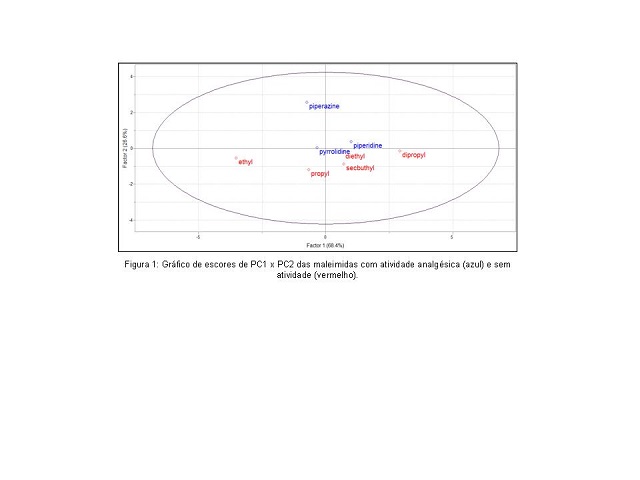
Gráfico de escores.
Figura 2
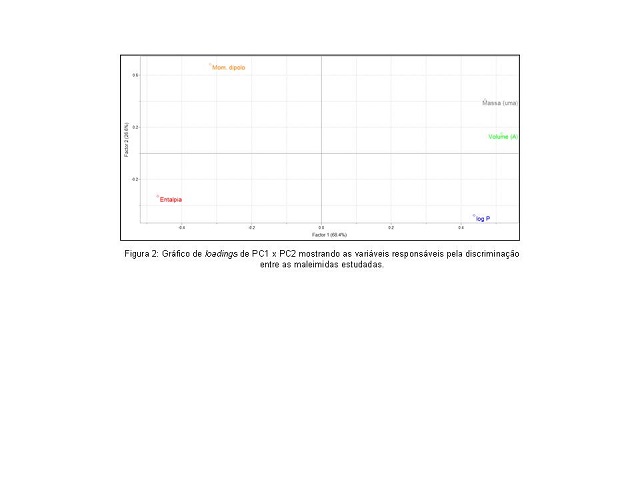
Gráfico de loadings.
CONCLUSÕES: Os métodos quimiométricos PCA e HCA foram aplicados com sucesso para um conjunto de parâmetros físico-químicos calculados para oito maleimidas análogas. Tais análogos foram discriminados em ativos e inativos, quanto à atividade analgésica. Verificou-se uma contribuição significativa dos parâmetros momento de dipolo, logP e entalpia para a distinção observada. Com base nos resultados obtidos nesse trabalho, acreditamos que os pesquisadores devem investir na síntese de maleimidas com grupos substituintes mais polares, se o objetivo for a obtenção de compostos com maior atividade analgésica.
AGRADECIMENTOS: À FAPES e a FAPEMIG pelo apoio financeiro.
REFERÊNCIAS BIBLIOGRÁFICA: 1.CECHINEL FILHO, V.; CORRÊA, R.; CAMPOS, F. C. Aspectos químicos e potencial terapêuticos de imidas cíclicas: uma revisão da literatura. Química Nova, v. 26, n. 2, p. 230-241, 2003. 2.VERMA, J.; KHEDAR, V. M.; COUTINHO, E. C. 3D-QSAR in drug design-a review. Current Topics in Medicinal Chemistry, v.10, n. 1, p. 95-115, 2010.
