Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Orgânica
TÍTULO: Hidrólise de éster aromático catalisada por células íntegras da macaúba (Acrocomia aculeata)
AUTORES: Soares, S.H. (UFPI) ; Moraes, M.I. (UFPI) ; Costa, J.G.M. (URCA) ; Machado, L.L. (UFBA) ; Nunes, F.M. (UFC) ; Lemos, T.L.G. (UFC) ; Santos, A.K.L. (UFPI)
RESUMO: Reações de biotransformações estão cada dia mais sendo utilizadas nas indústrias
químicas. A obtenção de compostos quirais é a principal vantagem do uso da
biocatálise na química, pois produz substâncias enantiomericamente puras. Na
biotransformação foi utilizado como biocatalizador, a macaúba: polpa e casca, e
como substrato o éster, benzoato de etila (1) onde obteve-se o ácido carboxílico
correspondente, ácido benzóico. A polpa da macaúba mostrou-se bastante eficaz para a hidrólise enzimática de éster aromático.
PALAVRAS CHAVES: Hidrólise enzimática; éster aromático; macaúba
INTRODUÇÃO: Dentro das novas tecnologias para a síntese de compostos enantiomericamente
puros, temos a biocatálise como um dos campos mais promissores.1 Pois a mesma
consiste no uso de catalisadores naturais, as enzimas, para realizar
transformações químicas em compostos orgânicos.2 Esses processos enzimáticos
apresentam-se vantajosos quando comparados aos processos químicos convencionais, o que representa uma grande vantagem econômica e ambiental.³ A macaúba é uma fruta da palmeira nativa brasileira (Acrocomia aculeata),encontrada principalmente na floresta latifoliada semidecídua, e é conhecida como coco-espinho. O presente trabalho teve como objetivo, realizar hidrólise enzimática com o biocatalizador macaúba utilizando as células íntegras da polpa e da casca,
mostrando que as reações desse processo são rotas importantes para a geração de
ácidos carboxílicos, com menores custos e impactos ambientais.
MATERIAL E MÉTODOS: A metodologia empregada foi adaptada de literatura4. Nos experimentos foram
utilizados 23 g de material vegetal: cascas e a polpa da macaúba como
biocatalisador, em solução aquosa, juntamente com 200 mg do substrato benzoato de etila. Os mesmos foram agitados em Shake (150 rpm) durante 72h. As amostras foram filtradas, extraídas com AcOEt, secas com sulfato de sódio anidro e evaporado até secura com rota-evaporador rotativo. As amostras obtidas foram cromatografadas em sílica gel e analisadas em CCD, IV, RMN 1H e 13C, CG/EM.
RESULTADOS E DISCUSSÃO: Inicialmente foi realizada a determinação proteica pelo método de Lowry
modificado por Hartree, resultando em 0,954 mg/mL para a polpa e 2,22 mg/mL para a casca, de teor proteico. Para a biotransformação foi utilizado como substrato o benzoato de etila (1) obtendo o ácido benzóico (Esquema 1). Na reação foi utilizada células íntegras da polpa e casca da macaúba. A conversão foi determinada por RMN 1H e 13C e CG/EM, os resultados são apresentados na Tabela 1.
Esquema 1
Tabela 1: Resultados da hidrólise enzimática do benzoato de etila
Biocatalisador C% (ácido carboxílico) ee%
Casca da macaúba 8,7 NT
Polpa da macaúba 86,0 NT
Apesar do bioproduto obtido a partir da hidrólise enzimática com as células íntegras da macaúba não ter fornecido um composto quiral devido o substrato utilizado, mas pode-se comprovar a eficácia de enzimas deste vegetal para tal finalidade. Visto que serão repetidas tais reações com substratos que forneçam produtos enantiomericamente puros para assim atingir o objetivo da biocatálise.
Esquema 1
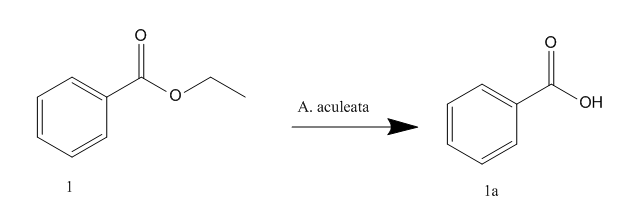
Esquema da hidrólise enzimática do benzoato de etila
utilizando células íntegras da macaúba
CONCLUSÕES: O fruto macaúba (Acrocomia aculeata), mais especificamente a polpa, apresenta-se como um bom biocatalisador, cujas enzimas atuam na hidrólise enzimática de éster, pois produziu o ácido carboxílico 1a com 86% de conversão. Enquanto que a casca não obteve bom resultado, pois houve conversão de apenas 8,7%. Dessa forma, a polpa da macaúba mostrou-se bastante eficaz para a hidrólise de éster aromático.
AGRADECIMENTOS: Os autores agradecem ao CNPq, FUNCAP e LBPN-UFC.
REFERÊNCIAS BIBLIOGRÁFICA: 1 CARVALHO, P. O.; CALAFATTI, S. A.; MARASSI, M.; SILVA, D. M.; CONTESINI, F. J.; BIZACO, R.; MACEDO, G. 2005. Potencial de biocatálise enantiosseletiva de lipases microbianas. Química Nova, 28: 614.
2 OLIVEIRA,S.C.; OMORI,T.A.; PORTAS,B.V.2012. Redução enzimática do 4-(dimetilamino)benzaldeído com pedaços de cenoura (Daucus carota): Um experimento simples na compreensão da biocatálise. Química Nova, 35: 435-437.
3.PATEL, R.N.2002. Microbial/enzymatic synthesis of chiral intermediates for pharmaceuticals. Enzyme and Microbial Technology, 31: 804-826.
4 FONSECA, A. M.; MONTE, F. J. Q.; OLIVEIRA, M. C. F.; MATTOS, M. C.; CORDELL, G. A.; BRAZ-FILHO, R.; LEMOS, T. L. G. 2009. Coconut water (Cocos nucifera L.)—A new biocatalyst system for organic synthesis. Journal of Molecular Catalysis B: Enzymatic. 57: 78.
