Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Iniciação Científica
TÍTULO: Combinação de reações de CWPO e HDC de 4-clorofenol utilizando argilas pilarizadas como catalisadores
AUTORES: Silva, M.V.C. (UNIVERSIDADE FEDERAL DO PARÁ) ; Pizarro, A.H. (UNIVERSIDAD AUTÓNOMA DE MADRID) ; Molina, C.B. (UNIVERSIDAD AUTÓNOMA DE MADRID) ; Zamian, J.R. (UNIVERSIDADE FEDERAL DO PARÁ) ; Carvalho, S.M.L. (UNIVERSIDADE FEDERAL DO PARÁ)
RESUMO: O presente trabalho objetivou determinar o potencial de aplicação de argilas pilarizadas como catalisadores em reações acopladas de Oxidação catalítica com peróxido de hidrogênio (CWPO) e Hidrodescloração catalítica (HDC) para remoção de 4-clorofenol de efluentes sintéticos. Dois acoplamentos foram realizados: CWPO em série com HDC e vice-versa. Os experimentos foram realizados em um reator em batelada de vidro a 25°C e pressão atmosférica. As amostras foram analisadas por HPLC, Cromatografia Iônica, TOC e Espectrofotometria na região do UV-VIS. Medidas de ferro lixiviado foram determinadas por um método colorimétrico. Os dois experimentos obtiveram bastante êxito, com a total remoção do 4-clorofenol, sendo a combinação CWPO em série com HDC a mais eficiente.
PALAVRAS CHAVES: argilas pilarizadas; CWPO; HDC
INTRODUÇÃO: Um dos mais prejudiciais compostos orgânicos presentes em efluentes industriais é o 4-clorofenol, que é extremamente tóxico, de difícil biodegrabilidade e persistente no meio ambiente (Pera-Titus et al., 2004). A busca por métodos de tratamento e purificação de efluentes industriais poluentes vem ganhando destaque no mundo científico. Devido suas inúmeras vantagens em relação aos tratamentos convencionais, duas técnicas estão em crescente ascensão: a Hidrodescloração catalítica (HDC) e a Oxidação catalítica com peróxido de hidrogênio (CWPO). A HDC promove a descloração da molécula orgânica utilizando o gás hidrogênio como agente redutor (Murena e Gioia, 2002). A CWPO promove a oxidação da molécula orgânica, utilizando o reagente Fenton (peróxido de hidrogênio e íons ferro), em fase heterogênea (Molina et al., 2006). Entretanto, essas duas técnicas também possuem desvantagens: a HDC não promove a completa mineralização dos produtos restantes, sendo necessário um tratamento adicional para essa remoção. A CWPO pode produzir produtos altamente tóxicos, persistentes e prejudiciais, assim como os compostos originais tratados (Munoz et al., 2011). Todo esse panorama evidencia a importância do desenvolvimento de estudos detalhados sobre a possibilidade de acoplamento de ambos os experimentos, uma vez que as limitações de um processo são sanadas pelo outro. Na literatura, existem somente dois trabalhos que tratam sobre essa combinação de reações (Yalfani et al., 2011; Munoz et al., 2013). E não existe nenhum trabalho acerca desse acoplamento utilizando argilas pilarizadas como catalisadores. Assim, o presente trabalho buscou promover esse acoplamento utilizando argilas pilarizadas, visando melhorar a remoção final dos poluentes orgânicos, obtendo produtos pouco tóxicos.
MATERIAL E MÉTODOS: Preparação da Al-Fe-PILC: a solução pilarizante foi preparada pela adição lenta de NaOH (0,2 M) a uma solução de nitrato de alumínio (0,1 M) misturada com uma solução de nitrato de ferro (0,1 M), a 25°C. A solução resultante foi exposta a uma temperatura de 90°C durante 3h e depois foi adicionada lentamente à suspensão da argila bentonítica Fisher (1% m/v), a 25°C. Em seguida, a mistura foi lavada sucessivas vezes por agitação/centrifugação. O produto sólido obtido foi seco a 60°C por 15h e calcinado a 350°C por 2h. Preparação da Pd-Al-PILC: foi realizado o método da impregnação com uma solução de cloreto de paládio (dissolvido em HCl 1M). Em seguida a amostra foi seca a 25°C por 2h e a 60°C por 15h. Posteriormente, a amostra foi calcinada a 500°C por 2h. As reações de CWPO em série com HDC foram realizadas a 25°C e 1 atm em um reator em batelada. 0,2 g de Al-Fe-PILC foram misturados com 100 mL de solução de 4-clorofenol (100 mg/L) e 100 mL de solução de peróxido de hidrogênio (350 mg/L), a pH 3,5. Depois de 4h, a solução resultante foi filtrada e 100 mL da mesma foram misturados com 0,1 g de Pd-Al-PILC e gás hidrogênio (50 mL/min). O mesmo experimento também foi realizado com quantidade subestequiométrica de peróxido de hidrogênio (75 mg/L). A combinação reversa (HDC em série com CWPO) também foi realizada. Os valores de “carbono orgânico total” (TOC) foram determinados por um analisador (Shimadzu). As concentrações de 4-clorofenol e dos produtos foram determinadas por HPLC (Prostar, Varian). As concentrações de peróxido de hidrogênio e os valores de Fe lixiviado foram medidos por um método colorimétrico utilizando um espectrofotômetro UV-Visível. As concentrações de íons cloreto foram determinadas por Cromatografia Iônica (Metrohm, 761 Compact IC).
RESULTADOS E DISCUSSÃO: De acordo com as figuras 1 e 2, verifica-se que o 4-clorofenol foi eliminado por completo em aproximadamente uma hora de reação em ambos os experimentos. O produto principal, fenol, também foi eliminado com sucesso em ambos. A cicloexanona (c-ona), produzida por HDC de 4-clorofenol, também foi totalmente removida com duas horas. A conversão final de TOC foi de aproximadamente 50% em ambos os experimentos. Na etapa de HDC na combinação (CWPO ⇒ HDC), houve uma conversão adicional de 12% de TOC, provavelmente devido à decomposição dos ácidos carboxílicos formados (o que se discutirá posteriormente). Uma notável diferença entre essas duas combinações foi a conversão final de peróxido de hidrogênio que foi de 75% para (CWPO ⇒ HDC) e 94% para (HDC ⇒ CWPO). Os ácidos carboxílicos produzidos na CWPO estão de acordo com os trabalhos de Zazo et al. (2006), Bautista et al. (2010) e Munoz et al. (2011). Na combinação (CWPO + HDC), os ácidos que se formam na primeira etapa foram praticamente removidos na etapa de HDC, sendo o oxálico eliminado em menor escala. No outro acoplamento, os ácidos oxálico e malônico são os principais produtos finais. Os resultados para a combinação de (CWPO ⇒ HDC) com quantidade subestequiométrica de peróxido de hidrogênio mostraram que compostos orgânicos clorados se formaram durante a etapa de CWPO (82% no fechamento do balanço de massa para o cloro). E confirmou-se também que esses compostos são removidos completamente na etapa de HDC (balanço de massa para o cloro de 100%). A quantidade de Fe lixiviado foi de 4,7 mg/L para (HDC ⇒ CWPO) e 1,7 mg/L para (CWPO ⇒ HDC). A maior quantidade de ferro perdida no primeiro caso pode ser explicada pela grande concentração de HCl (produzido pela HDC) ao redor dos centros ativos de Fe, favorecendo sua lixiviação.
Figura 1: CWPO em série com HDC
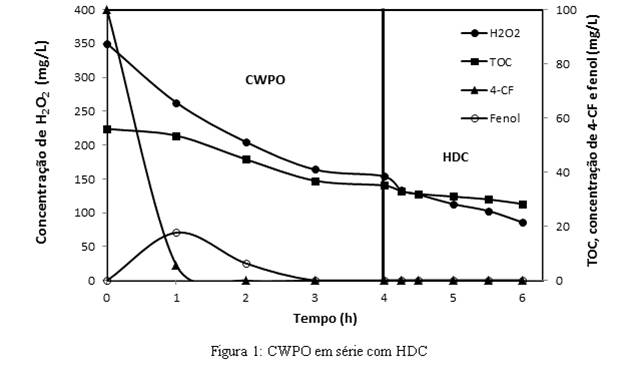
Resultados de TOC e concentrações de reagentes e produtos na combinação de CWPO em série com HDC.
Figura 2: HDC em série com CWPO
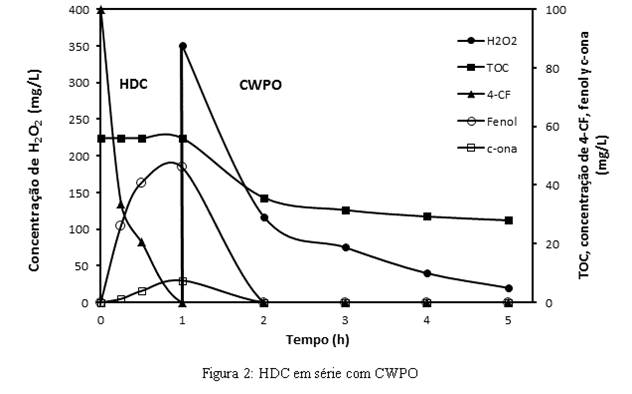
Resultados de TOC e concentrações de reagentes e produtos na combinação de HDC em série com CWPO.
CONCLUSÕES: A combinação de CWPO em série com HDC se mostrou mais eficiente, pois: possui baixa lixiviação de Fe (evitando que tratamentos posteriores sejam realizados para sua eliminação); possui maior eficiência no consumo de peróxido de hidrogênio (que é o principal custo no tratamento de oxidação, sendo possível o seu uso em quantidades subestequiométricas); os compostos clorados são totalmente removidos. Em suma, a combinação de CWPO em série com HDC utilizando argilas pilarizadas representa uma importante alternativa na otimização do tratamento de efluentes industriais clorados.
AGRADECIMENTOS: CNPq e DAIE/PROEX/UFPA
REFERÊNCIAS BIBLIOGRÁFICA: Bautista, P.; Mohedano, A. F.; Menendez, N.; Casas, J. A.; Rodriguez, J. J. (2010). Catalytic wet peroxide oxidation of cosmetic wastewaters with Fe-bearing catalysts. Catalysis Today, v. 151, p. 148-152.
Molina, C. B.; Casas, J. A.; Zazo, J. A.; Rodríguez, J. J. (2006). A comparison of Al-Fe and Zr-Fe pillared clays for catalytic wet peroxide oxidation. Chem. Eng. J., v. 118, p. 29–35.
Munoz, M.; de Pedro, Z. M.; Casas, J. A.; Rodriguez, J. J. (2011). Assessment of the generation of chlorinated byproducts upon Fenton-like oxidation of chlorophenols at different conditions. Journal of Hazardous Materials, v. 190, p. 993-1000.
Munoz, M.; de Pedro, Z. M.; Casas, J. A.; Rodriguez, J. J. (2013). Chlorophenols breakdown by a sequential hydrodechlorination-oxidation treatment with a magnetic Pd–Fe/γ-Al2O3 catalyst. Water Reserach, v. 47, p. 3070-3080.
Murena, F. & Gioia, F. (2002). Catalytic hidrodechlorination of dechaclorobifenil. Appl. Catal. B: Environ., p. 38-39.
Pera-Titus, M.; García-Molina, V.; Baños, M. A.; Giménez, J.; Espuglas, S. (2004). Degradation of chlorophenols by means of advanced oxidation processes: a general review. Applied Catalysis B-Environmental, v. 47, p. 219.
Yalfani, M. S.; Georgi, A.; Contreras, S.; Medina, F.; Kopinke, F. (2011). Chlorophenol degradation using a one-pot reductioneoxidation process. Appl. Catal. B: Enron., v. 104, p. 161-168.
Zazo, J. A.; Casas, J. A.; Mohedano, A. F.; Rodríguez, J. J. (2006) Catalytic wet peroxide oxidation of phenol with a Fe active carbon catalyst. Appl. Catal. B: Environ., v. 65, p. 261–268.
