Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Inorgânica
TÍTULO: Compostos de coordenação: complexos ternários formados entre o alumínio(III), a adenosina 5’-trifosfato e os aminoácidos sulfurados
AUTORES: Tenório, T. (PUC-RIO) ; Ramos, J.M. (UFRJ) ; Buarque, C.D. (PUC-RIO)
RESUMO: O estudo de complexos ternários de Al(III) com o adenosina 5’-trifosfato (ATP) e os aminoácidos (aas) sulfurados (metionina, cisteína, homocisteína e penicilamina) foi realizado em solução aquosa por meio de titulações potenciométricas na proporção metal:ligante:ligante 1:1:1. As constantes de estabilidade [T=25°C e I=0,1 mol.L-1 (KNO3)] dos complexos ternários com o Al(III) foram determinadas. A especiação dos sistemas também foi feita. Nas espécies AlATPaas, o ATP deve comportar-se como ligante bidentado. A partir dos valores das constantes de estabilidade dos complexos propõe-se que a penicilamina comporte-se distintamente dos demais aminoácidos. A metionina, a cisteína e a homocisteína atuam como bidentados enquanto a penicilamina atua como ligante tridentado.
PALAVRAS CHAVES: Potenciometria; Especiação; Sistemas ternários
INTRODUÇÃO: O alumínio(III) é encontrado em pequenas concentrações no organismo humano –em média, 7,0 μg/L no sangue–(OMS, 1998). Este íon está presente em produtos animais, água ingerida, grãos, ervas e temperos, vegetais, frutas, legumes, aditivos alimentares e utensílios e recipientes contaminados. Soluções de nutrição parenteral, fórmulas infantis e medicamentos podem conter Al(III) (GREGER, 1993). Sua absorção ocorre no estômago e no duodeno proximal e é facilitada pela formação de complexos com ligantes biológicos (EICHHORN et al., 1980), em especial, aqueles com grupos carboxilatos, catecolatos, fenolatos e fosfatos (EICHHORN et al., 1980). Ligantes dietéticos, como os aminoácidos, também afetam a absorção e o transporte do Al(III) in vivo (BERTHON, 2002).
A toxicidade ocorre geralmente em casos de superexposição provocados por infusão de fluidos dialisados ou nutrição parenteral contaminados. O Al(III) causa inúmeros efeitos nocivos entre os quais se destaca osteomalácia, anemia hipocrômica microcítica e doenças neurodegenerativas, como Parkinson, Alzheimer e escleroses (BARQUERO-QUIROS et al., 2001).
Em fluidos corporais com baixa concentração de transferrina, os nucleosídeos di e trifosfatos e os aminoácidos podem agir como ligantes do Al(III) compondo espécies solúveis (SCHÄFER e JAHREIS, 2006). Biomoléculas de baixo peso molecular formam complexos que aumentem o pH de precipitação do Al(III) e sua absorção gastrointestinal (BERTHON, 2002).
O objetivo da pesquisa foi avaliar a capacidade de formação e a estabilidade de complexos ternários em solução aquosa formados entre o Al(III), o ATP e os aminoácidos sulfurados.
MATERIAL E MÉTODOS: Os reagentes utilizados foram o nitrato de alumínio nonahidratado P.A. (Merck), o adenosina 5’-trifosfato (Sigma), a metionina (Reagen), a cisteína (Sigma), a homocisteína (Sigma) e a penicilamina (Acros Organics).
Empregou-se o aparelho de titulação potenciométrica Metrohm 809 Titrando, o pHmetro Micronal B375 e o agitador magnético Metrohm 801 Stirrer. Antes da realização de qualquer experimento, as vidrarias foram limpas e secas de modo a evitar contaminações. Todas as titulações foram realizadas no mesmo dia do preparo das soluções.
Conservou-se à temperatura, à agitação e à força iônica constantes, sendo a temperatura mantida a 25,0°C, a partir da utilização de um equipamento de banho termostatizado, a agitação mantida constante e branda pelo agitador magnético e a força iônica mantida a 0,1 mol/L. O eletrólito suporte KNO3 foi usado, devido às características de seus íons, que não interfere na titulação.
As titulações foram realizadas a partir de adições sucessivas de incrementos de 0,1 mL de solução padrão de KOH 0,1 mol/L a um volume inicial de 120,00 mL de mistura. Titulou-se 50,00 mL da solução de adenosina 5’-trifosfato 2x10-3 mol/L, 50,00 mL da solução de um dos aas 2x10-3 mol/L, 10,00 mL de KNO3 1,2M e 10,00 mL da solução de Al 1x10-2 mol/L.
O estudo em solução aquosa de complexos ternários revela além da possibilidade da formação de complexos e das ligações que podem suceder nesses, as interações ou sua ausência quando certos sítios coordenativos estão impedidos e outros livres nos complexos com metais.
RESULTADOS E DISCUSSÃO: A partir das análises em solução aquosa dos sistemas ternários na proporção 1:1:1, os valores dos logaritmos das constantes de formação das espécies ternárias foram encontrados. Os logaritmos das constantes de estabilidade dos complexos ternários formados no sistema Al(III):ATP:L 1:1:1 a 25°C e I = 0,1 mol/L (KNO3) podem ser observados na tabela 1. Propostas estruturais foram feitas a partir dos valores de constante de estabilidade encontrados para as espécies AlATPL.
Os valores de constante de estabilidade para as espécies AlATPL são semelhantes para os aminoácidos metionina (Met), cisteína (Cis) e homocisteína (Hcis). Contudo, para a espécie AlATPPenicilamina é encontrado um valor diverso, próximo a 20,00, por isso, propõe-se que as espécies ternárias AlATPL apresentam modos de coordenação distintos em relação aos aminoácidos.
Provavelmente, a Met, a Cis e a Hcis atuam como ligantes bidentados através do oxigênio do carboxilato e do nitrogênio do grupo amino, comportamento este característico para os aminoácidos. Já a penicilamina (Pen) deve se comportar como tridentada através do oxigênio do carboxilato, do nitrogênio do grupo amino e do enxofre do grupo tiol.
O ATP nas espécies AlATPL parece comportar-se da mesma forma independente de qual aminoácido seja o segundo ligante a coordenar-se ao metal. Ele deve comportar-se como ligante bidentado através de um oxigênio do grupo fosfato γ e de um oxigênio do grupo fosfato β.
As curvas de distribuição de espécies em função do pH para os quatro sistemas, figura 1, mostram que as espécies hidrolisadas do metal ou dos complexos binários e ternários predominam em pH fisiológico.
Figura 1
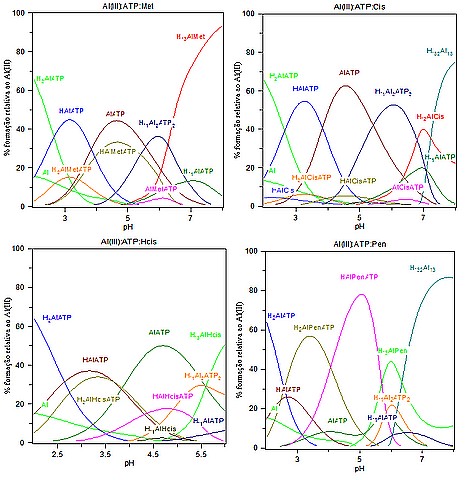
Curvas de especiação para os sistemas ternários Al:ATP:aas.
Tabela 1
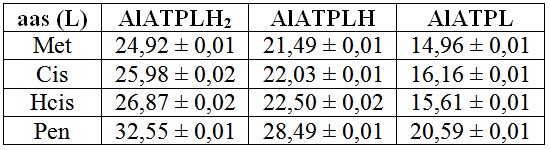
Logaritmos das constantes de estabilidade para os complexos formados entre o Al(III), o ATP e os aminoácidos sulfurados a 25°C e I = 0,1 mol/L (KNO3).
CONCLUSÕES: No que diz respeito aos complexos ternários com o ATP, os valores das constantes de estabilidade para as espécies AlATPL (log βAlATPL) sugerem que os aminoácidos Met, Cis e Hcis atuam como ligantes bidentados. Para a Pen indica-se o comportamento tridentado através dos átomos de oxigênio do carboxilato, de nitrogênio da amina e de enxofre. O ATP agiria como ligante bidentado. O íon metálico adotaria então o número de coordenação seis, com uma geometria octaédrica. A esfera de coordenação do Al(III) nos complexos seria completada por moléculas de água de coordenação.
AGRADECIMENTOS: O trabalho foi apoiado pelo CNPq, pela PUC-Rio e pela UFRJ.
REFERÊNCIAS BIBLIOGRÁFICA: BARQUERO-QUIROS, M.; VARGAS-ROJAS, R.; BLANCO-SAENZ, R. 2001. Neurotoxicidad y enfermedades óseas provocadas por la contaminación con aluminio de soluciones de diálisis renal. Revista Costarricense de Ciencias Médicas, 22: 179 -189.
BERTHON, G. 2002. Aluminium speciation in relation to aluminium bioavailability, metabolism and toxicity. Coordination Chemistry Reviews, 228: 319-341.
EICHHORN, G. L.; BUTZOW, J. J.; CLARK, P.; VON HAHN, H. P.; RAO, G.; HEIM, J. M.; TARIEN, E.; CRAPPER, D. R.; KARLIK, S. J. Em: MARTELL, A. E., editor. 1980. Metal Ion-Nucleic Acid Interactions: Aging and Alzheimer's Disease. Inorganic chemistry in biology and medicine, American Chemical Society, 140: 75-88.
GREGER, J.L. 1993. Aluminum metabolism. Annual Review of Nutrition, 13: 43-63.
ORGANIZAÇÃO MUNDIAL DA SAÚDE (OMS). 1998. Elementos traço na nutrição e saúde humanas, Ed. Roca, 18: 194-195.
SCHÄFER, U.; JAHREIS, G. 2206. Exposure, bioavailability, distribution and excretion of aluminum and its toxicological relevance to humans. Trace Elements and Electrolytes, 23: 162-172.
