Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Analítica
TÍTULO: ELETRODO PARA DETECÇÃO DE HISTIDINA
AUTORES: Hoss, D. (UNIOESTE) ; Lindino, C.A. (UNIOESTE)
RESUMO: Sensores eletroquímicos são dispositivos extensamente utilizados em análises de
materiais biológicos. O uso de metodologia eletroquímica se deve ao seu custo
menor, precisão, exatidão, possibilidade de análise in situ e com o mínimo de
geração de resíduos, em consonância com os princípios da Química Verde. Preparou-
se um sensor baseado em pasta de carbono, polímero condutor e o aminoácido
histidina. A incorporação do aminoácido na matriz do polímero condutor em meio
ácido é o que apresenta melhor resultado com o polímero atuando ao mesmo tempo
como suporte físico e mediador eletroquímico.
PALAVRAS CHAVES: sensor; aminoácido; polímero condutor
INTRODUÇÃO: Os aminoácidos são estruturas bases de diversos processos bioquímicos e sua
detecção é de importância vital. Mesmo proteínas podem ser detectadas se
desnaturadas ou rompidas suas ligações peptídicas, que são ligações que se
estabelecem entre um grupo carboxila de um aminoácido e um grupo amina de outro
aminoácido subsequente, com formação de uma molécula de água, gerando seus
respectivos aminoácidos.
Sensores são dispositivos que empregam um elemento de reconhecimento acoplado a
um transdutor, que converte a energia do evento em um sinal mensurável.1
Portanto, a utilização de sensores eletroquímicos é uma das formas mais
interessantes para a detecção de aminoácidos, pois apresenta um custo menor,
precisão, exatidão, possibilidade de análise in situ e com o mínimo de geração
de resíduos, em consonância com os princípios da Química Verde ou Química Limpa.
Eletrodos modificados são alterações que são realizadas em eletrodos
tradicionais com o intuito de prover maior seletividade, sensibilidade e
correlação na determinação de espécies. A escolha desse material base para a
modificação desejada é um aspecto extremamente importante, pois deve ser
eletroativo, permitir reação redox, permitir diversas imobilizações, ser estável
e de preferência de baixo custo.
Polímeros condutores são alguns dos materiais utilizados como suporte e
que podem conduzir a corrente elétrica, atuando como mediadores eletroquímicos,
que podem ser utilizados na construção de biosensores.
A incorporação de aminoácidos em diferentes matrizes na detecção
eletroquímica permite não só a determinação destes mesmos, mas abre a
possibilidade de detecção de proteínas e anticorpos.
MATERIAL E MÉTODOS: Todos os reagentes utilizados foram grau para análise. O gás utilizado para
desoxigenação nas medidas voltamétricas foi o N2 (AGA, 99,999 %). A água
utilizada para o preparo de soluções foi purificada por destilação e osmose
reversa (ADAMO).
Utilizou-se a célula eletroquímica com eletrodo de referencia de Ag/AgCl/KCl
saturado, eletrodo de trabalho de pasta de carbono modificado e eletrodo
auxiliar de Pt.
Foram preparados eletrodos modificados sem e com o polímero condutor. Para isto,
foram montados dois eletrodos: um eletrodo contendo somente pasta de carbono e
outro eletrodo com pasta de carbono incorporado com 10% de polímero condutor
sintetizado quimicamente (o-anisidina) e o aminoácido histidina (VETEC) e
colocados em um suporte plástico apropriado. O contato elétrico foi realizado
com um fio de cobre imerso na pasta de carbono. O eletrodo preparado deste modo
foi nomeado PCPA.
A característica eletroquímica da interação aminoácido-polímero foi determinada
por voltametria cíclica, em solução tampão pH = 6,98 verificando-se o desempenho
em diferentes velocidades de varredura (20, 50, 100, 150 e 200 mVs-1) e
potenciais entre 0,0 e 1,0 V. As condições de trabalho foram estabelecidas no
potenciostato Microquímica PG-01 acoplado a um computador.
Após os teste eletroquímicos foi avaliada a influência do pH, na qual foram
preparadas soluções de histidina em pH 3, 4, 5 e 6. Posteriormente, o estudo
eletroquímico foi realizado por voltametria cíclica contendo 15 mL da solução de
histidina 1 mmol L-1, com velocidade de varredura de 100 mVs-1 entre os
potenciais de 0,0 V a 1,0 V adicionando-se 50 µL da mesma solução após cada
medida, até a resposta ser invariável.
Todas as medidas foram realizadas a 25°C.
RESULTADOS E DISCUSSÃO: Os resultados mostraram que o processo é controlado por difusão, com a obtenção
de resposta com correlação de 0,9727 no gráfico corrente versus raiz quadrada da
velocidade de varredura.
No estudo da variação do pH da solução contendo histamina verificou-se que o
eletrodo apresenta maior alteração no sinal da corrente em pH = 3,0. Neste pH, a
poli-o-anisidina apresenta condutividade maior, facilitando os processos de
trocas iônicas e transporte de elétrons2. Neste pH, a histidina apresenta o
grupo
carboxila desprotonado.
A voltametria mostrou o surgimento de dois picos anódicos em 0,53 V e 1,0 V e um
pico catódico em 0,19 V, nos quais a corrente gerada aumenta com o aumento na
concentração do aminoácido histidina. A resposta do eletrodo modificado no
potencial de 0,53 V é linear na concentração entre 1 x 10-3 e 1,58 x 10-2 mol
L-1, com coeficiente de correlação de 0,9947 (Figura 1). Testes mostraram que
este
resultado é repetitível. Novos estudos estão sendo realizados para se determinar
as demais figuras de mérito analítico.
Histidina
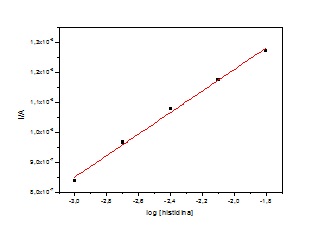
Resposta eletroquimica do eletrodo de pasta
carbono/poli-o-anisidina à histidina, a 25 °C.
CONCLUSÕES: A incorporação do polímero condutor (poli-o-anisidina) em pasta de carbono
juntamente com o aminoácido histidina permitiu obter resposta eletroquímica com a
concentração do aminoácido na faixa entre 1 x 10-3 e 1,58 x 10-2 mol L-1, com
coeficiente de correlação de 0,9947 em pH = 3, indicando a possibilidade deste
sistema como um sensor à aminoácidos.
AGRADECIMENTOS: À Fundação Araucária (Paraná) pela Bolsa de Iniciação Científica de Débora Hoss.
REFERÊNCIAS BIBLIOGRÁFICA: 1. TARLEY, C.R.T; SOTOMAYOR, M.D.P.T; KUBOTA, L.T. Química Nova 28, 2005, 1087
2. MATTOSO, L. H. Polianilinas: síntese, estrutura e propriedades. Química Nova, São Paulo, v. 19, n. 4, p. 388-399, 1996.
