Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Analítica
TÍTULO: UTILIZAÇÃO DE BIOMASSA E PLANEJAMENTO EXPERIMENTAL EM ESTUDOS DE ADSORÇÃO DE Cu2+ EM SOLUÇÃO AQUOSA
AUTORES: Lima, A.N. (UNIOESTE) ; Alcantara, M.S. (UNIOESTE) ; Fleck, L. (UNIOESTE) ; Leonel, L.V. (UNIOESTE) ; Koelln, F.T.S. (UNIOESTE) ; Vasconcelos, H.L. (UNIOESTE)
RESUMO: A remoção de metais pesados por adsorção se destaca devido à possibilidade de utilizar resíduos como adsorvente e diminuir os custos do processo. Este trabalho avaliou o desempenho da casca da castanha do Brasil como adsorvente na remoção de íons Cu2+ presentes em soluções aquosas. Alíquotas de 100mL com concentrações de Cu2+ entre 40 e 160 mg/L foram avaliadas em pH de 1,1 a 5,9 e massa do adsorvente entre 9 e 271 mg. A avaliação estatística realizada pelo
delineamento composto central rotacional gerou um modelo matemático para o desempenho do adsorvente utilizado. Nas condições avaliadas, a maior adsorção de Cu2+ por massa de adsorvente, superior a 25 mg/g, foi verificada em condições de pH entre 4,1 e 5,9, massa do adsorvente abaixo de 41,75 mg e concentração de Cu2+ acima de 100 mg/L.
PALAVRAS CHAVES: Biomassa; Metal Pesado; DCCR
INTRODUÇÃO: Atividades como mineração, tratamento incorreto de efluentes urbanos e industriais e incineração de materiais tóxicos têm aumentado a concentração de metais pesados no ambiente natural (PIZZOL et al., 2011). Os metais pesados possuem como características a não biodegradabilidade e alta solubilidade em água, dessa forma são facilmente inseridos na cadeia alimentar e podem
afetar diretamente a saúde humana e ao meio ambiente (ZAINI et al., 2010) devido ao seu potencial tóxico e cancerígeno (ZHOU et al., 2004, RAHMANI et al., 2010).
Desta forma, vários métodos têm sido sugeridos para a remoção de metais pesados tais como: troca iônica, precipitação, tratamento eletroquímico, floculação, ozonização e filtração. Apesar de comprovada eficiência, esses métodos se tornam restritos devido à sua inviabilidade econômica ou ao tempo de
tratamento requerido (KARNITZ et al., 2010).
Um método alternativo e muito eficaz é a biossorção caracterizada pela aplicação em sistemas com capacidade de detoxificar grande volume de efluente com baixo custo operacional, possível seletividade, recuperação da espécie metálica e biodegradabilidade.
Resíduos vegetais como talos de girassol, casca de eucalipto, farelo de milho, casca de coco, resíduos de chá, palha de arroz e folhas de árvores tem sido investigados como adsorventes na remoção de metais pesados de soluções aquosas (DHIR; KUMAR, 2010) devido ao seu baixo custo, elevada disponibilidade e alta eficiência na adsorção de diferentes tipos de íons metálicos (BHARGAVA et al., 2012).
Neste sentido, o objetivo deste trabalho foi avaliar a eficiência de cascas de castanha-do-Brasil (Bertholletia excelsa) como material adsorvente de íons cobre (II) presentes em solução aquosa, utilizando técnicas de planejamento experimental.
MATERIAL E MÉTODOS: Cascas de castanha do Brasil (Bertholletia excelsa) com granulometria inferior a 2 mm foram utilizadas como material adsorvente nos ensaios experimentais realizados. O material adsorvente, previamente triturado em moinho de facas, foi lavado com água destilada e seco em estufa a 105ºC até atingir peso constante.
Os ensaios experimentais foram realizados de acordo com um delineamento fatorial 2³ completo, com 8 pontos fatoriais (níveis ± 1), 3 pontos centrais (nível 0) e 6 pontos axiais (± α), totalizando 17 ensaios.
Este planejamento teve como objetivo avaliar, em diferentes níveis, os efeitos da concentração inicial de metal (50 a 150 mg/L), do pH (1,5 a 5,5) e da massa de adsorvente (30 a 250 mg) sobre a quantidade de íons Cu(II) adsorvido (qe). A quantidade de íons Cu(II) adsorvido por unidade de massa de adsorvente para todos os ensaios foi calculada a partir da diferença entre as concentrações inicial e final do metal no volume de solução.
Na condução do experimento, alíquotas de 100 mL da solução de metal foram colocadas em contato com o material adsorvente, sob agitação contínua de 200 rpm, por 8 horas a 25º C. Após este período, as soluções foram filtradas e a concentração do metal foi determinada na fase líquida por espectrometria de absorção atômica - método 3111A (APHA, 2005).
A determinação dos efeitos dos fatores estudados, coeficientes de regressão, análise de variância e gráficos de superfícies de resposta e de contorno, ao nível de 10% de significância, foi realizada por meio da utilização do software STATISTICA versão 7.1 (StatsoftTM, USA).
A validação experimental do modelo matemático proposto para qe foi realizada em quadruplicata nas condições ótimas estabelecidas. Foram calculados a média, o desvio-padrão e o coeficiente de variação (CV).
RESULTADOS E DISCUSSÃO: A partir dos resultados obtidos foi possível verificar que as variáveis pH, massa de adsorvente e concentração inicial do metal se mostraram estatisticamente significativas, ao nível de 90% de confiança para a adsorção de Cu(II). Entretanto, a interação entre as mesmas não foi significativa. O modelo matemático codificado, para os parâmetros significativos, está representado na Equação 1 (Figura 1).
O modelo proposto apresentou adsorção de metal máxima explicável de 87,3%. A análise de variância, ao nível de 10% de significância, indicou regressão significativa. A validação experimental do modelo foi realizada nas condições otimizadas de pH, massa de adsorvente e concentração inicial do metal de 5,07, 30 mg e 115,3 mg/L, respectivamente. O valor de qe obtido na validação foi de 31,8±2,15 mg/g com CV de 0,06%, confirmando a capacidade de reprodutibilidade do processo, constatada pelo baixo coeficiente de variação, o que indica a homogeneidade dos resultados obtidos.
A relação entre as variáveis dependentes e independentes é representada tridimensionalmente pela superfície de resposta gerada pelo modelo (Figura 2), em que neste caso os valores codificados das variáveis foram utilizados no gráfico apresentado.
Foi possível verificar que em menores quantidades de biomassa e maiores concentrações iniciais de metal e pH, houve uma maior quantidade adsorvida do íon metálico Cu(II) por unidade de massa do adsorvente.
Também foi possível constatar que a casca de castanha do Brasil apresentou boa capacidade de adsorver íons Cu(II) quando comparada com outros tipos de biomassas. CHAVES e TITO (2011) obtiveram taxas de adsorção abaixo de 2 mg Cu(II)/g de argila bentonita, valores bem inferiores aos alcançados neste trabalho.
Figura 1
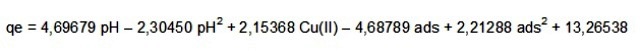
Modelo matemático codificado, com os parâmetros significativos, para a adsorção de íons cobre(II) por cascas de castanha do Brasil.
Figura 2
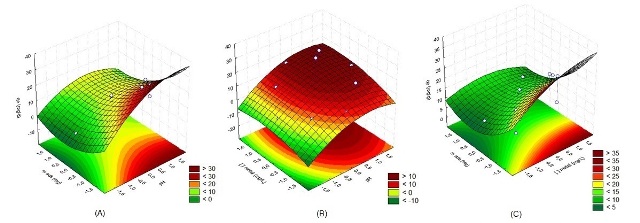
Superfícies de resposta para a quantidade de Cu(II) adsorvido (qe):(A)massa adsorventeXpH; (B)concentração CuXpH e (C)massa adsorventeXconcentração Cu
CONCLUSÕES: Os resultados mostraram que a eficiência de adsorção de Cu(II) em solução aquosa utilizando cascas de castanha do Brasil aumenta em concentrações elevadas de metal e em baixas concentrações do material adsorvente, na faixa de pH entre 4,1 e 5,9. A utilização de cascas de castanha do Brasil (Bertholletia excelsa) como adsorventes de íons cobre presentes em efluentes líquidos pode ser uma alternativa viável de aplicação em escala industrial tendo em vista apresentar baixo custo e não ter necessitado de nenhum tipo de tratamento especial para ser utilizado no presente estudo.
AGRADECIMENTOS: À Fundação Araucária, Ao Programa de Pós-gradução em Engenharia Agrícola e à Universidade Estadual do Oeste do Paraná
REFERÊNCIAS BIBLIOGRÁFICA: American Public Health Association - APHA, 1998. Standard methods for the examination of water and wastewater. 20. ed. American Public Health Association/ American Water Works Association/ Water Environment Federation, Washington, DC, USA.
BHARGAVA, A.; CARMONA, F. F.; BHARGAVA, M.; SRIVASTAVA, S. 2012. Approaches for enhanced phytoextraction of heavy metals. Journal of Environmental Management, 105:103-120.
CHAVES, L. H. G.; TITO, G. A. 2011. Cadmium and copper adsorption on bentonite: effects of pH and particle size. Revista Ciência Agronômica, 42:278-284.
DHIR, B.; KUMAR, R. 2010. Adsorption of Heavy Metals by Salvinia Biomass and Agricultural Residues. International Journal Environmental Research, 4:427-432.
KARNITZ, J. O.; GURGEL, L. V. A.; GIL, L. F. 2010. Removal of Ca(II) and Mg(II) from aqueous single metal solutions by mercerized cellulose and mercerized sugarcane bagasse grafted with EDTA dianhydride (EDTAD). Carbohydrate Polymers, 79:184–191.
PIZZOL, M.; CHIRSTENSEN, P.; SCHMIDT. J.; THOMSEN, M.2011. Impacts of metals on human health: a comparison between nine different methodologies for Life Cycle Impact Assessment (LCIA). Journal of Cleaner Production, 19:646-656.
RAHMANI, A; MOUSAVI, Z; FAZLI, M. 2010. Effect of nanostructure alumina on adsorption of heavy metals. Desalination, 253:94-100.
STATSOFT, Inc. Statistica for Windows (Data analysis software system), versão 7.1. Tulsa: Statsoft, 2005. APHA. Standard methods for the examination of water and wastewater. Washington: American Public Health Association.
ZAINI, M. A. A.; AMANO, Y.; MACHIDA, M. 2010. Adsorption of heavy metals onto activated carbons derived from polyacrylonitrile fiber. Journal of Hazardous Materials,180:552-560.
ZHOU, D; ZHANG, L; ZHOU, J; GUO, S. 2004. Cellulose/chitin beads for adsorption of heavy metals in aqueous solution. Water research, 38:2643-2650.
