Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Ensino de Química
TÍTULO: O PODER DAS MOEDAS: ESTUDOS ELETROQUÍMICOS VOLTADOS PARA O ENSINO MÉDIO
AUTORES: Pereira, M.R.S. (UEMA) ; Ferreira, D.R.M. (UEMA) ; Menezes, L.C. (UEMA) ; Costa, T.T.B. (UEMA) ; Santos, M.S. (UEMA) ; Silva, M.V.V. (UEMA) ; Campos, V.N.S. (UEMA) ; Froz, M.K.V.C. (UEMA) ; Vale, R.C. (UEMA) ; Costa, M.C.P. (UEMA)
RESUMO: Foram apresentados neste trabalho experimento da eletroquímica, os diversos
modelos da pilha da moeda com diferentes soluções e formas aplicáveis no ensino
médio e a sua discussão de suas principais características físico-químicas,
visando o uso didático por educadores da área de ensino de ciências. Os resultados
confirmam que a experimentação configura-se como potencialmente útil para auxiliar
os alunos a construírem suas concepções relacionadas ao conhecimento científico.
PALAVRAS CHAVES: ELETROQUÍMICA; PILHAS; MOEDAS
INTRODUÇÃO: A primeira pilha elétrica foi desenvolvida por Alessandro Giuseppe Antonio
Anastásio Volta (1737-1827), a partir da divulgação de resultados de pesquisa de
Luigi Galvani (1737-1798). Galvani observou contrações musculares nas pernas de
rãs mortas, quando o metal onde estavam penduradas (cobre) entrava em contato
com o suporte de ferro. Ele interpretou o fenômeno como “eletricidade de origem
animal”, isto é, os músculos armazenavam eletricidade e os nervos a conduziam
(FELTRE, 2009). A eletroquímica abrange os processos químicos que envolvem
transferência de elétrons. Assim, quando um processo químico ocorre, produzindo
transferência de elétrons, é chamado de pilha ou bateria. Portanto, pilha e
bateria são processos químicos que ocorrem espontaneamente e geram corrente
elétricas. (RUSSELL, 2008). Diante do exposto é de grande relevância adaptar
métodos de ensino que possam contribuir para o entendimento qualitativo da
Eletroquímica visando facilitar suas transformações. O presente trabalho tem
como proposta a adaptação do experimento sobre Eletroquímica, utilizando
materiais alternativos do cotidiano, aliado à caracterização qualitativa,
destinados a alunos do ensino médio.
MATERIAL E MÉTODOS: Foram construídas pilhas simples, em paralelo e em série, com moedas. Utilizou-
se solução de salmoura, solução de ácido acético, solução de ácido sulfúrico,
solução de sulfato de cobre e solução de cloreto de potássio para serem o
eletrólito. Na determinação da voltagem da pilha simples, pegou-se dois vidros
de relógio e colocou-se o papel de filtro umedecido com a solução de salmoura,
onde as moedas foram fixadas sobre este eletrólito. Outro modelo desta pilha foi
realizado, diferenciando-se apenas pelas soluções (sulfato de cobre e cloreto de
potássio). Em seguida, para determinar as pilhas em paralelo com moedas
prateadas e bronzeadas colocou-se nas diferentes soluções de ácido acético e
ácido sulfúrico. Logo após mediu-se a voltagem com o uso de um voltímetro.
Posteriormente, analisou-se a pilha em série, pegaram-se quatro béqueres de 200
mL e quatro vidros de relógio, contendo a solução de salmoura, colocaram-se as
moedas presas pelas garras de jacaré e as mergulhou na solução e anotou-se a
voltagem.
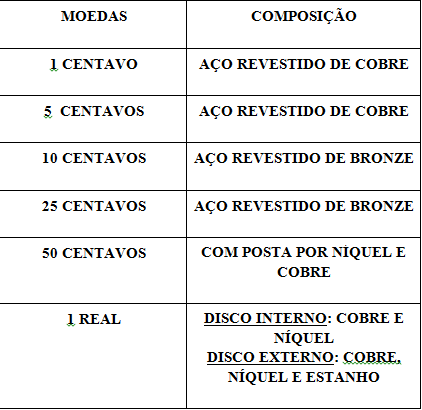
RESULTADOS E DISCUSSÃO: A tabela 1 mostra os tipos de metais que contém em cada moeda, destacando qual a
moeda que melhor oxida e qual a moeda que melhor reduz.
A pilha simples foi reproduzida diversas vezes com intuito de comparar as suas
respectivas voltagens. Logo, as moedas que apresentaram melhor corrente
elétricas, foram às moedas de cinco centavos bronzeada e as de um real.
A pilha em série foi montada através de uma inovação da pilha simples,
utilizando os mesmos materiais e acrescentando duas moedas. As moedas de cinco
centavos bronzeada e as de um real foram colocadas nas extremidades por
apresentarem maior voltagem, completando o sistema, adicionou- se moedas
aleatórias. Este modelo de pilha foi reproduzida, trocando o vidro de relógio
pelo béquer de 200 mL a fim de aumentar a superfície de contato. Resultando em
uma maior voltagem em relação ao sistema anterior, ressaltando que notou-se
macroscopicamente a oxidação da moeda que continha cobre. A pilha em paralelo
foi construída com cinco moedas de cinco centavos prateada e cinco moedas de
cinco centavos bronzeada, com o intuito de demonstrar o estudo da oxi-redução.
No final da formação do sistema, observou-se macroscopicamente a oxidação da
moeda de cinco centavos bronzeada.
A diferenciação dos dois sistemas realizados ocorre pelo fato de que o primeiro
sistema (pilha série) tem a passagem de apenas uma corrente elétrica, podendo
ser anulada, quando uma moeda estiver desgastada. Já o sistema em paralelo
dispõe de várias passagens elétricas, pois cada pilha formada fornece uma
corrente elétrica, logo, ao ocorrer o desgaste de uma moeda no sistema o mesmo
ainda assim funciona.
tabela1:moedas vs composição
CONCLUSÕES: Os experimentos foram reproduzidos de modo que os resultados encontrados
satisfazem o objetivo proposto neste trabalho. No desenvolvimento das pilhas de
moedas observou-se a praticidade da realização deste experimento. De modo que, a
sua aplicação em sala de aula constitui de uma ferramenta importantíssima no
ensino de ciências, trabalhando conceitos básicos de oxi-redução. Resultando em
uma maior participação do aluno e maior facilidade em entender acerca do assunto,
já que se utiliza da prática e materiais encontrados em seu cotidiano.
AGRADECIMENTOS: Laboratórios de Macromoléculas e Produtos Naturais da UEMA.
REFERÊNCIAS BIBLIOGRÁFICA: FELTRE, R; Físico Química 2, editora MODERNA, 2009
RUSSEL, B. J; Química Geral volume 2, 2ºedição, editora MAKRON BOOKS, 2008
