Realizado no Rio de Janeiro/RJ, de 14 a 18 de Outubro de 2013.
ISBN: 978-85-85905-06-4
ÁREA: Química Tecnológica
TÍTULO: ADSORÇÃO DO EXTRATO METANOLICO DA RAIZ DE Derris urucu EM COLUNA DE LEITO FIXO
AUTORES: Silva, P. (UNIVERSIDADE FEDERAL DO PARÁ) ; Teixeira, M. (UNIVERSIDADE FEDERAL DO PARÁ) ; Chagas, B. (UNIVERSIDADE FEDERAL DO PARÁ) ; Brito, R. (UNIVERSIDADE FEDERAL DO PARÁ) ; Vera, G. (UNIVERSIDADE FEDERAL DO PARÁ) ; Ferreira, R. (UNIVERSIDADE FEDERAL DO PARÁ) ; Machado, N. (UNIVERSIDADE FEDERAL DO PARÁ) ; Rodrigues, E. (UNIVERSIDADE FEDERAL DO PARÁ) ; Almeida, O. (UNIVERSIDADE FEDERAL DO PARÁ) ; Tenoro, E. (UNIVERSIDADE FEDERAL DO PARÁ)
RESUMO: Neste trabalho, desenvolveu-se um estudo comparativo para avaliar a capacidade de
adsorção do extrato bruto metanoico da raiz de Derris urucu (DU_MeOH), em coluna
de leito fixo com dois tipos de adsorventes, alumina ativada a 500 ºC e carvão
ativado comercial. O adsorvente que melhor descreveu a capacidade de adsorção foi
alumina ativada na condição 2 (com auxílio da bomba peristáltica). Os dados
experimentais de adsorção se ajustaram bem ao modelo de Langmuir com R2 = 1,0000,
e EMR = 0,45%, em 136,14 min. O fator de separação RL = 0,0952 foi favorável,
encontra-se na faixa entre 0 e 1. Não foi possível analisar quimicamente as
frações coletadas em nenhuma das condições para avaliar sua composição.
PALAVRAS CHAVES: Adsorção; Leito fixo; Adsorventes
INTRODUÇÃO: A OMS classifica a rotenona e a piretrina como inseticidas orgânicos de uso
doméstico moderadamente perigoso, classificada como grau 3 numa escala de 1
(mais tóxico) a 4 (menos tóxico). Pesquisas realizadas em todo o mundo têm
indicado mais restrições sobre o uso da rotenona. Muitos países que possuem
grande biodiversidade de peixes costeiros, tropicais e subtropicais, restringem
ou até proíbem pesquisadores de usá-la. Como inseticida natural de contato, pode
causar a morte de animais por meio da inibição da cadeia respiratória
mitocondrial, pelo bloqueio da fosforilação do ADP a ATP, sendo peixes e insetos
altamente sensíveis (MASCARO et al., 1998). E ao contrário de outros não é
neurotoxina, mas funciona como inibidor de enzimas respiratórias, causando a
diminuição do consumo de oxigênio, redução da respiração e ataques que provocam
convulsões e conduzem finalmente a paralisias e morte por parada respiratória
(SILVA et al., 2002).
Diante do exposto, torna-se necessário estudar alternativas que não percam a
atuação como inseticida, ao mesmo tempo em que haja redução da toxicidade. Neste
intento, é realizado o estudo da Derris urucu, como inseticida alternativo, cuja
avaliação da adsorção do extrato bruto dessa raiz, em leito fixo, é apresentada
no presente trabalho. Para avaliar a afinidade dos adsorventes foram feitas
isotermas de adsorção, com solução do extrato bruto em metanol, sobre carvão
ativado comercial e alumina ativada a 550 ºC.
MATERIAL E MÉTODOS: Foram dissolvidos 5,0g (DU_MeOH) em 2000 mL de metanol (P.A, CRQ, Brasil). A
mistura foi transferida para frascos de vidro âmbar e guardada ao abrigo da luz.
A alumina adsorvente foi obtida pela decomposição térmica do Al2O3.3H2O em um
forno tipo mufla (LINN ELEKTRO THERM, LM 312.6 SO 1729), durante 2 horas, na
temperatura de 550ºC. O carvão ativado (P.A, CRQ, Brasil), foi seco em estufa na
temperatura de 105ºC, durante 2 horas.Os ensaios de adsorção foram realizados em
uma coluna de vidro, dimensões, 40 cm de altura por 1,40 cm de diâmetro interno.
O leito foi formado pelo empacotamento manual do adsorvente com auxílio de um
funil de vidro. Um tampão de algodão foi colocado em cada extremidade do leito.
Foi acionado um compressor, após a montagem da coluna, para bombear o extrato
DU_MeOH contido em um reservatório para o interior da coluna de cima para baixo.
Realizou-se ensaios até que a saturação da coluna atingissem 90% da concentração
inicial (alimentação). Foram coletadas alíquotas em balões volumétricos de 25
mL, para cada alíquota, anotava-se o tempo de vazão. Um pH-metro digital
(SCHOTT) mediu o pH da solução trabalho e das frações coletadas. Os ensaios
foram realizados em duplicata. As frações coletadas foram transferidas para
cápsulas de porcelana previamente pesadas, e submetidas a secagem em estufa na
temperatura de 50 ºC. A massa de adsorvente (alumina e carvão ativado) usada
para cada experimento foi de 10g. Para estabelecer a correlação mais apropriada
para as curvas de equilíbrio foram utilizados os modelos de Langmuir e
Freundlich. Os parâmetros das isotermas foram determinados através de regressão
linear e não linear utilizando o software OriginPro v.8.0724 (OriginLab
Corporation, USA).
RESULTADOS E DISCUSSÃO: A perda de massa durante a calcinação esta relacionada com a perda das
hidroxilas dos arranjos estruturais das moléculas do trihidroxido de alumino,
apresentando uma perda d massa teórica de 34,62%.
As isotermas foram ajustadas aos dados experimentais nos modelos de Langmuir e
de Freundlich (curvas linearizadas), a fim de determinar a capacidade de
adsorção de (DU_MeOH)(Figuras 1).
Os valores médios de qmax para o modelo de Langmuir, variaram de 71,9424 a
238,0952 mg.g-1 (alumina, C1 e C2) e de 243,9024 mg.g-1 (carvão ativado, C2).
Todos os valores de RL, encontram-se no intervalo de 0 e 1 (adsorção é do tipo
favorável).
No modelo de Freundlich, os valores de KF e n, que indicam a capacidade e a
intensidade da adsorção, respectivamente, variaram entre 282,9437 a 266,2564
L.g-1 (alumina, C1 e C2) e 252,1158 L.g-1 (carvão ativado, C2). Para n, todos os
valores ficaram abaixo da unidade (Tabela 1).
Dados experimentais se ajustaram às equações de Langmuir e de Freundlich (R2 >
0,900). Comparados os valores de R2 obtidos no ajuste dos dados experimentais às
duas equações, observa-se que o modelo de Langmuir apresentou melhor resultado,
com bomba peristáltica (C2).
Neste trabalho as isotermas obtidas através dos tratamentos estatísticos são do
tipo linear(Da classe Langmuir), apresentaram duas regiões distintas: uma o
inicio, linear sugere alta difusão do soluto para o adsorvente, seguido de uma
região côncava conforme mostrado na figura 1, que representa a saturação dos
poros do adsorvente, sugerindo não haver nenhuma forte competição entre o
solvente e o soluto para a ocupação dos sítios de adsorção.
tabela 1
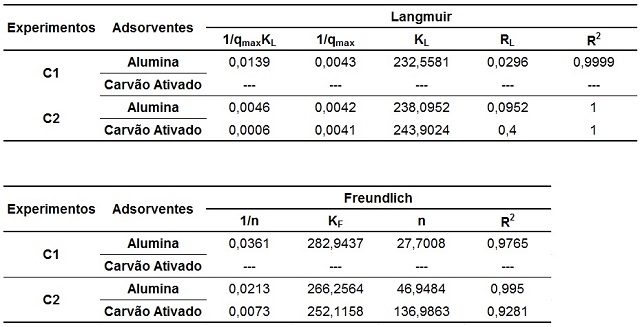
Parametros das isotermas de Langmuir e Freundlich
para a adsorção do extrato bruto da raiz de derris
urucu.
figura 1
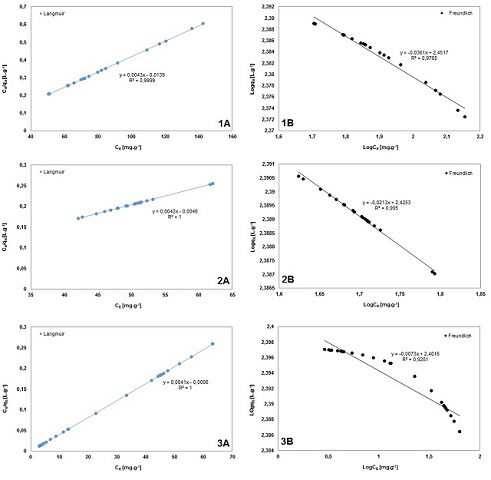
Isotermas de adsorção do DU_MeOH em leito fixo a
28,5 ºC, modelos de Langmuir(1A,2A e 3A) e de
Freundlich(1B, 2B e 3B)(Alumina,C1 e C2; car.
Ativ.,C2)
CONCLUSÕES: Descreveu-se por meio de isotermas a capacidade de adsorção do extrato bruto da
raiz de Derris urucu para análise e projeto de sistema de adsorção. Os dados
experimentais de adsorção se ajustaram bem aos modelos de Langmuir e Freundlich.
Mas, o modelo de Langmuir (R2 = 1,0000, EMR = 0,45%) foi o que descreveu melhor o
processo de adsorção para os ambos adsorventes: alumina e carvão (ativados), com
auxílio da bomba peristáltica (C2).
AGRADECIMENTOS:
REFERÊNCIAS BIBLIOGRÁFICA: ADAMSON, A. W. and GAST, A. P. Physical Chemistry of Surfaces. Wiley, New York, 6th edition, 1997.
AGUERRE, R. J.; SUAREZ, C.; VIOLLAZ, P.E. New BET type multilayer sorption isotherms. Part II: Modeling water sorption in foods, Lebensmittel-Wissenschaft & Technologie, London: Academic Press Ltd., v.22, n.4, p.192-195, 1989.
CIOLA, R. Fundamentos da catálise, 1ª edição, Editora Moderna, Editora da Universidade de São Paulo-SP. 1981.
COULSON, J. M., RICHARDSON, J. F. Tecnologia Química. 3ª Edição, Lisboa: Fundação Caloustre Gulbernkian, V.3, 1982.
FREUNDLICH, H. The teory of adsorption. Zeitschrift fuer Chemie und Industrie der Kolloide, v.3, p.212-220, 1909.
GILES, C. H.; D’SILVA, A. P.; EASTON, I. A. General treatment and classification of solute adsorption-isotherm.2. Experimental Interpretation. Journal of Colloid and Interface Science, v.47, p.766-778, 1974.
GILES, C. H.; SMITH, D.; HUITSON, A. General treatment and classification of solute adsorption-isotherm .1. Theoretical. Journal of Colloid and Interface Science, v.47, p.755-765, 1974.
GOMIDE, R. Operações unitárias. São Paulo: Gomide, 1980.
LANGMUIR, I. The Adsorption of Gases on Plane Surfaces of Glass, Mica and Platinum. Journal of the American Chemical Society, v.40, p.1361-1403, 1918.
McCABE, W. L.; SMITH, J. C.; HARRIOT, P. Unit operations of chemical engineering. 6rd Ed. McGrall Hill, 2001.
MISRA, C. Industrial Alumina Chemicals, Washington, DC.: American Chemical Society (ACS Monograph 184), p.165,1986.
RICHARDSON, J.F.; HARKER, J.H.; BACKHURST, J.R. Coulson and Richardson’s Chemical Engineering Vol. 2 Particle Technology and Separation Process 4ª Ed. Butterworth Heinemann: Oxford, 1979.
