Software Avogadro no ensino/aprendizagem de polaridade molecular.
ISBN 978-85-85905-21-7
Área
Ensino de Química
Autores
Wanzeler, H.P. (IFPA) ; Ferreira, R.B.V. (IFPA) ; Corrêa, S.M.V. (IFPA)
Resumo
O objetivo deste trabalho interventivo e quantitativo foi utilizar o Avogadro (um simulador computacional de modelos tridimensionais) na mediação entre o ensino do conteúdo de polaridade molecular e a capacitação de habilidades visuais, espaciais e operacionais para clarificar conceitos abstratos a alunos da 1ª série do Curso Técnico em Estradas Integrado ao Ensino Médio do Instituto Federal de Educação, Ciência e Tecnologia do Pará (IFPA). Especificamente, mensurou o desempenho dos estudantes pelos índices de acertos no pré e pós-teste com cinco questões objetivas em sala de aula. Na sistematização os melhores incrementos (do pré-teste ao pós-teste) ocorreram nas notas: três (5,9% a 24,9%), quatro (0% a 23,5%) e cinco (0% a 17,6%). Mostrando que a metodologia pode ser viável e promissora.
Palavras chaves
Avogadro; Mediação; Modelos 3D
Introdução
Os conceitos de Química, em especial de átomos, muitas vezes são abstratos e compreender sem o uso de analogias e modelos é uma tarefa dificílima (GABEL, 1999). Visualizar e em seguida operar com estas abstrações são algumas das principais barreiras que tornam a relação de ensino/aprendizagem, na visão dos alunos, não promissora. Na tentativa de tornar estes conceitos mais compreensíveis e “concretos”, o uso das tecnologias de informação e comunicação para educação tem sido alvo de estudos de professores e profissionais simpatizantes. Este trabalho de abordagem interventiva e quantitativa teve por objetivo geral a utilização de um programa de simulação computacional de modelos tridimensional (3D) chamado Avogadro, na mediação entre o ensino do conteúdo de polaridade molecular e a capacitação de habilidades visuais, espaciais e operacionais na clarificação de conceitos abstratos a alunos da 1ª série do IFPA. Tangente ao objetivo especifico, mensurou-se o desempenho dos estudantes pelos índices de acertos no pré e pós-teste em sala de aula. Sob a justificativa de que as formas clássicas de ministrar o conteúdo polaridade molecular utilizando-se de desenhos no quadro negro ou figuras de livros didáticos são fortemente desfavorecidas pelo plano bidimensional (2D), resultando, em muitas ocasiões, em perdas significativas na compreensão de pontos fundamentais do estudo, a título de exemplo, o momento dipolar resultante. Valendo-se da capacidade de visualização 3D possibilitada pelo Avogadro, com seus ricos e dinâmicos modelos moleculares (HANWELL et al, 2012) foi suposto que o software trabalhe como agente complementador do método 2D, facilitador e potencializador das habilidades visuais, espaciais e operacionais.
Material e métodos
Com o tema polaridade molecular e suas aplicações, a aula, de aproximadamente cem minutos na turma de Técnico em Estradas, se iniciou com uma breve justificativa e explicação para a realização da atividade aos 17 alunos presentes. Contou com a utilização de um projetor de imagens, um computador (com o programa Avogadro instalado) e do quadro-negro. Os estudantes dispuseram de 10 minutos para a realização de um pré-teste com cinco questões objetivas sobre polaridade molecular e, ao seu término, explorou-se o tema. Apresentaram-se duas questões cotidianas aos estudantes: Por que lavar as mãos só com água não remove a sujeira ocasionada pela graxa? E por que o álcool etílico se dissolve em água? Com o auxílio do Avogadro modelos foram apresentados: água, gás oxigênio, etanol e gasolina (figura 1a). Solicitou-se aos alunos identificarem, intuitivamente, quais das moléculas projetadas eram polares e apolares. Partindo de observações feitas aos modelos 3D da água e gás oxigênio (moléculas simples) e do momento dipolar resultante indicado pelo programa, definiu-se polaridade molecular (figuras 1b e 1c). No quadro-negro também se demonstrou, qualitativamente, como se obter o momento dipolar resultante (usando a eletronegatividade e vetores) e, por conseguinte determinou-se uma molécula polar e uma apolar. Alguns exercícios foram realizados com os estudantes e, finalmente, as questões iniciais foram respondidas com o argumento de polar dissolve polar e apolar dissolve apolar (TITO; CANTO, 1998). Por fim, um pós-teste de 10 minutos semelhante ao teste inicial foi realizado.
Resultado e discussão
O teste inicial foi realizado rapidamente pelos estudantes, pois o término
ocorreu em três minutos e sete segundos. Duas hipóteses surgiram do
ocorrido: que a maioria dos estudantes já dominava o assunto ou que
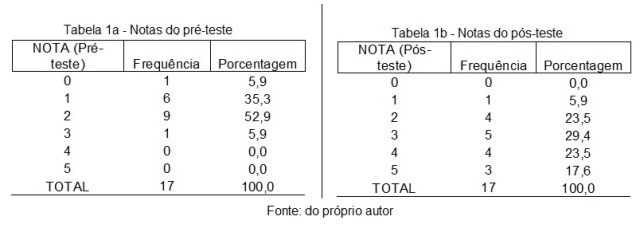
responderam as questões “no chute”. Ao observar os resultados do pré-teste
na tabela 1a (onde a nota máxima era cinco), as notas mais expressivas
obtidas pela turma foram: nota dois (52,9%) e nota um (35,3%). Deste modo, a
segunda hipótese acabou prevalecendo. A exposição dialogada e interrogada
(CURY, 2013) utilizando-se dos modelos no Avogadro cumpriram suas propostas
ao introduzir, atrair a atenção e tornar os alunos participativos, pois
facilitaram a compreensão da definição e reconhecimento de moléculas polares
e apolares tanto nas versões 3D no programa (a protuberância da nuvem
eletrônica nos átomos mais eletronegativos nas moléculas polares foi um
fator marcante na classificação), quanto nas versões 2D no quadro- negro (os
estudantes perceberam que a protuberância no Avogadro era o momento dipolar
resultante demonstrado na lousa). A afirmação de ocorrência de facilitação
na compreensão do tema pela metodologia baseia-se nas respostas verbais
corretas dadas pelos alunos para as questões introdutórias e nos resultados
obtidos no pós-teste, ver tabela 1b, que ao comparar estas com as notas
iniciais, notam-se os incrementos ocorridos nas notas: três (5,9% a 24,9%),
quatro (0% a 23,5%) e cinco (0% a 17,6%); e consequentemente um decréscimo
nas notas: zero (5,9% a 0%), um (35,3% a 5,9%) e dois (52,9% a 23,5%). Outro
ponto interessante de ser observado foi que os estudantes se esforçaram um
pouco mais para resolver o teste final, pois foi finalizado em cinco minutos
e dezesseis segundos.
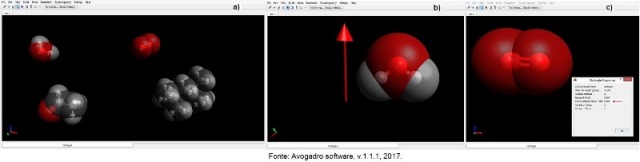
Figura 1a - Simulação moléculas de oxigênio, água, etanol e gasolina. Figuras 1b e 1c - molécula polar e molécula apolar (respectivamente).
Conclusões
Sinaliza-se que, o trabalho cumpriu seu principal objetivo ao verificar a ocorrência de mediação e consequentemente facilitação, ocasionada pelo Avogadro na mudança de referencial (3D para 2D e vice-versa), decorrendo em aumento das percepções e habilidades dos discentes. Tal incremento foi observado ao se comparar os aspectos quantitativos referentes a acertos de questões nos pré e pós-testes. Os resultados, que ainda podem ser maximizados, apontam que a metodologia é viável e promissora.
Agradecimentos
Ao Profº. Johny da Silva Oliveira por ceder o espaço para a realização da atividade.
Referências
CURY, Augusto. Pais brilhantes, professores fascinantes. 13 ed. Rio de Janeiro: Sextante, 2003. 177 p.
GABEL, D. Improving teaching and learning through chemistry education research: Look to the future. Journal of Chemical Education, v.76, n.4, p.548,1999.
HANWELL, Marcus D. et al. Avogadro: an advanced semantic chemical editor, visualization, and analysis platform. Journal of cheminformatics, v. 4, n. 1, 2012.p.1-17.
PERUZZO, Francisco. CANTO, Eduardo. Química na abordagem do cotidiano. 2 ed. São Paulo: Moderna, v. 1,1998.
































