ANÁLISE DA EFETIVIDADE DO SULFATO DE TETRAKIS HIDROMETILFOSFÔNICO (THPS) NA CORROSÃO MICROBIOLÓGICA DO AÇO DUPLEX 2205 EM SISTEMA COM ALTA CONCENTRAÇÃO DE ÍONS CLORETO
ISBN 978-85-85905-23-1
Área
Materiais
Autores
Cordeiro Antunes de Araújo, L. (UFMA) ; da Silva Ribeiro, P.R. (UFMA) ; Reznik, L.Y. (UFRJ) ; Soares Lutterbach, M.T. (INT) ; Camporese Sérvulo, E.F. (UFRJ)
Resumo
Este trabalho objetivou avaliar a efetividade do biocida sulfato de tetrakis hidroximetil fosfônio (THPS) na Corrosão Microbiológica (CM) sobre aço inoxidável duplex 2205 em água de produção de petróleo (AP) com salinidade de 160 g/L de NaCl de plataforma offshore. Os ensaios foram conduzidos em um recipiente de vidro de 1 L com 800 mL da AP, onde foram dispostos os corpos de prova para testes microbiológicos, na presença e ausência tanto do THPS. Os ensaios microbiológicos consistiram em testes de toxicidade do THPS, quantificação celular dos grupos bacterianos e análise de superfície por microscopia eletrônica de varredura (MEV). Os resultados revelaram que o THPS foi mais efetivo contra as BRS enquanto que as análises de MEV mostraram a presença de pites na ausência de THPS no sistema.
Palavras chaves
Corrosão Microbiológica; Biocida (THPS); Bactérias
Introdução
A corrosão microbiológica é um processo de degradação mediado por microrganismo, frequentemente em superfícies de materiais metálicos. Isso vem causando prejuízo a diversos setores industriais. Com o objetivo de exterminar os prejuízos ocasionados (perdas e/ou contaminação de produtos, contaminação ambiental, trocas de peças, por exemplo) com a corrosão microbiológica os segmentos industriais têm investido grande montantes para solucionar e prevenir estes tipos de problemas (GENTIL, 2011). Dentre os métodos utilizados e que se tem investidos, seja com o objetivo de melhorar ou desenvolver outras metodologias, podemos citar proteção catódica, inibidores de corrosão, aplicação de revestimentos e utilização de biocidas (VIDELA, 2003). Dentre estes métodos, a aplicação de biocidas vem sendo bastante utilizada nos últimos anos por ser uma forma barata e de fácil aplicação. No entanto, salienta-se a importância de se conhecer o sistema onde os biocidas serão aplicados, para que se possa selecionar o melhor biocida e a dosagem correta, com o intuito de se atingir o maior espectro de microrganismos possível e assim resolver o problema acarretado na situação de onde foi aplicado. Para que se possa escolher o melhor biocida para determinado problema alguns fatores podem e devem ser levados em consideração. Dentre eles podemos citar: não deve ser tóxicos aos animais, fácil degradação, não ser corrosivo, ter amplo espectro de ação, fácil aplicação e eficaz em baixas dosagens. Dentre os biocidas utilizados, o sulfato de tetrakis hidróxido metil fosfônico (THPS) tem sido muito utilizado nos últimos anos por possuir boas propriedades e por ser fácil a sua aplicação. Na literatura é reportada a sua eficácia contra diversos microrganismos, tanto Gram positivos quanto Gram negativos. Este biocida também é conhecido popularmente como “biocida verde”, devido à sua baixa toxicidade aos animais, plantas superiores e seres humanos e à sua biodegradabilidade, superior aos biocidas convencionais (VIDELA, 1990; LARSEN; SANDERS; TALBOT, 2000). No entanto, não há relatos da sua atuação na presença de um grupo bacteriano, principalmente em altas concentrações de sais contendo o íon cloreto. E como se sabe, os microrganismos conseguem se desenvolver em diversos ambientes inóspitos, como por exemplos, baixo pH, temperatura elevada, alta salinidade. Face ao exposto, este trabalho teve como objetivo avaliar a efetividade do biocida THPS na corrosão microbiológica do aço duplex 2205 em sistema com elevada salinidade.
Material e métodos
Para que o presente trabalho fosse realizado foi utilizado corpos de prova (CPs) retangulares de aço inoxidável duplex 2205 com área total de 11 cm2. O biocida utilizado foi um comercial, THPS(sulfato de tetrakis hidroximetil fosfônio, apresentando as seguintes propriedades: líquido transparente (incolor) com densidade de 1,39 g mL-1 e pH=4,2. O fluido utilizado nos sistemas experimentais foi uma água de produção(AP) de uma plataforma de petróleo offshore, contendo 160 g/L de cloreto de sódio(NaCl). A concentração do THPS a ser aplicada no sistema experimental foi determinado pelo método da concentração mínima inibitória (CMI). Para tanto, alíquotas de cada grupo bacteriano(mencionados a seguir) foram colocadas em seu respectivo meio de cultivo em contato com diferentes concentrações do biocida(entre 0 – 200 ppm), conforme indicado por Gaylarde(1999). Os cultivos foram incubados e observados diariamente quanto ao crescimento, por um período total máximo de 28 dias. Quando não identificado crescimento microbiano, foi feita a transferência de alíquota de 1 mL para novo meio a fim de identificar se o efeito era bacteriostático. O sistema utilizado consistiu em um recipiente de vidro de 1 L de capacidade (estéril), contendo 800 mL de AP, onde foram dispostos os CPs, fixados à tampa por fios de nylon. As determinações quantitativas do monitoramento das diferentes populações de bactérias consideradas principais promotoras da CM (planctônicas e sésseis, sem e com aplicação de THPS) cuja concentrações iniciais estavam em torno de 106 NMP/mL foram feitas pela técnica do Número Mais Provável (NMP) (ABELHO, 2013), em meios apropriados conforme descrito a seguir: -Bactérias heterotróficas aeróbias(BHA) em caldo nutriente (g/L): Peptona de carne 5,0; Extrato de levedura 3,0; Dextrose 9,0 +160 g de NaCl e pH=7,0±2; Incubação: 2 dias; -Bactérias produtoras de ácido aeróbias(BAPA) e bactérias produtoras de ácido anaeróbias(BAnPA) em Caldo vermelho de fenol (g/L): Extrato de peptona 10; extrato de carne 1,0; vermelho de fenol 0,018; Glicose 10 + 160 g de NaCl e pH=7,4 ± 2. Para BAnPA, a condição de anaerobiose foi garantida através de purga de nitrogênio no meio; Incubação: 2 e 14 dias, respectivamente; -Bactérias redutora de sulfato (BRS) em meio POSTGATE E (g/L) (POSTGATE, 1984): KH2PO4 0,5; NH4Cl 1,0; CaCl2.6H2O 1,0 ; MgCl2.7H2O 2,0 ; FeSO4.7H2O 1,0 ; FeSO4.7H2O 1,0; Extrato de lêvedo 0,1; Ácido ascórbico 0,5; Agar-agar 1,9 + 160 g de NaCl; Ao meio também foram adicionados 7 mL de solução de lactato de sódio 50%; 4 mL de solução de resazurina 0,025%(m/v) e pH=7,6±2. Incubação: 28 dias; Para análise da superfície, os CPs (previamente desidratados e metalizados) foram examinados quanto à presença de biofilmes/pites por Microscopia Eletrônica de Varredura (MEV).
Resultado e discussão
Os dados obtidos nas análises da concentração mínima inibitória (CMI)
demonstraram que os grupos bacterianos BHA e BAPA tiveram comportamentos
semelhantes, sendo detectado crescimento somente após 3 dias quando
cultivadas na presença de 50 ou 100 ppm do tetrakis hidroximetil fosfônio
(THPS). Em concentrações inferiores a 50 ppm foi detectado turvamento
(crescimento) em 24 horas de incubação. Entretanto, para as BAnPA foi
detectado crescimento com 4 dias. No caso do grupo das BRS, a partir de 50
ppm não foi detectado crescimento, mesmo após 28 dias de incubação. Neste
trabalho, a concentração de 150 ppm do biocida foi escolhida para conduzir
as demais etapas dos experimentos. Esta escolha ocorreu devido esta
concentração ter sido capaz de inibir o crescimento de todos os grupos
bacterianos, sendo detectado efeito bactericida para BRS e bacteriostático
para as demais populações. Salienta-se que o efeito bactericida para todos
os grupos bacterianos somente foi alcançado quando se atingiu a concentração
de 200 ppm do THPS.
Na Tabela 1 podem ser observadas as concentrações celulares das principais
populações de bactérias envolvidas na corrosão microbiológica (CM), nas
fases planctônica e séssil, expressas em valores médios de NMP/mL e
NMP/cm2. Para avaliação dos biofilmes, CPs de aço duplex foram
imersos em água produzida (160 g/L NaCl) por um período máximo de 15 dias.
Na fase planctônica – sem aplicação de THPS (Tabela 1), à exceção das BRS,
houve aumento dos números das diferentes populações bacterianas em relação
aos valores iniciais inoculados no sistema (106 NMP/mL cada).
Note-se que há elevada densidade de BHAs na fase planctônica, indicando que
a colonização será rápida. Isto porque um elevado número de microrganismos
induz um número maior de sítios de adesão às superfícies sólidas (VAN
LOOSDRECHT et al, 2002). Além disso, espécies produtoras de material
polimérico extracelular (MPE) estão presentes neste grupo bacteriano o que
corrobora para a colonização e desenvolvimento de bactérias na superfície
metálica (LEWANDOWSK; BOLTZ, 2011). No caso das BRS, houve diminuição do seu
número independentemente do modo de condução do sistema. E, seu número
praticamente permaneceu constante, provavelmente devido ao metabolismo mais
lento e a competição pelas fontes nutricionais.
Os CPs foram colonizados pelas diferentes populações bacterianas (fase
séssil). Note-se que na fase séssil dos microrganismos – sem THPS todos os
grupos bacterianos também estavam presentes, tendo as BRS, novamente, em
menor número.
Os resultados (Tabela 1 - sistema com THPS 150 ppm) também revelaram que os
apesar do THPS ter diminuído a concentração celular das populações (em
comparação ao experimento sem aplicação de THPS) o mesmo somente foi efetivo
contra as BRS, o que corrobora com os resultados da CMI, onde este biocida
foi mais efetivo contra este grupo. Em nenhuma das fases microbianas
(planctônica e séssil) este grupo microbiano foi detectado durante a fase
experimental. Em outro estudo, Penna et al (2006), realizando ensaios em
condições dinâmicas com água do mar desaerada, verificaram que tratamento
com 150 ppm de THPS resultou em decréscimo de 2 e 3 ordens de grandezas para
BRS em 4 e 24 horas respectivamente. Para outros grupos microbianos
presentes no biofilme, as densidades celulares variaram entre 102
a 104 NMP/cm2.
No presente trabalho, os resultados mostram que o THPS foi mais efetivo no
controle de BRS. Para este biocida, a susceptibilidade das demais populações
sésseis foi tanto maior quanto maior a dose aplicada no sistema.
Os CPs de aço duplex antes de inseridos nas células experimentais e
decorridas 15 dias de exposição em água produzida também foram analisados
por microscopia eletronica de varredura (MEV). A técnica de MEV teve por
objetivo a obtenção de micrografias da superfície plana dos CPs metálicos e
após a formação dos biofilmes, sem e com aplicação de THPS a fim de avaliar
os aspectos gerais das superfícies dos CPs e dos materiais biológicos e
químicos (produtos de corrosão) a eles aderidos.
A Figura 1A mostra as fotomicrografias eletrônicas de varredura do biofilme
formado pela associação das distintas populações bacterianas sobre os CPs de
aço duplex expostos à água produzida, sem aplicação de biocida, decorridas
15 dias de exposição. Nota-se um biofilme maduro, sugerindo uma quantidade
elevada de células bacterianas aderidas à superfície do aço, corroborando
com os dados da Tabela 1 (Sem THPS). A elevada densidade de microrganismos
sésseis é um parâmetro de relevância para a ocorrência da corrosão
microbiológica, sobretudo quando coexistem espécies microbianas diversas
(KING; MILLER, 1971).
A heterogeneidade estrutural dos biofilmes pode gerar áreas com diferentes
concentrações de oxigênio, levando a: corrosão por aeração diferencial e
formação de pites (RAJASEKAR; TING, 2011). Também pode haver a
despolarização dos metais, em face da deposição de produtos de corrosão
sobre a superfície metálica, provocando mudanças dos fenômenos
eletroquímicos, como o potencial. Tem-se ainda que a atividade metabólica
dos microrganismos no biofilme pode levar a mineralização do material
aderido à superfície do metal, ocasionando o seu enobrecimento ou sua
degradação (ANGELL, 1999). Por fim, pode haver complexação do material
polimérico extracelular com íons metálicos, facilitando a fixação do
biofilme ao sólido (BEECH; SUNNER, 2004).
Nas imagens também se observa a presença de vários pites (Figura 1 C - sem
THPS e com microrganismos). A corrosão localizada por pites ocorre
principalmente pela produção de metabólitos agressivos, que causam
alterações na estrutura química da superfície metálica (RAJASEKAR; TING,
2011). Liang e et al (2014) estudaram o efeito das BRS na corrosão do aço
duplex 2205 em água do mar. Eles observaram por microscopia eletrônica de
varredura (MEV), uma distribuição não uniforme das células sobre a
superfície do metal. Adicionalmente, demonstraram a influência do sulfeto
gerado pelas BRS nas reações anódicas do metal, intensificando o processo
corrosivo. Fenômeno que também foi reportado por outros autores, dentre
eles, Antony et al (2008).
Os tratamentos da água produzida com THPS resultaram em impacto de
colonização das superfícies dos CPs de aço duplex (Tabela 1, Figura 1 B).
Analisando as imagens, observa-se que a aplicação do THPS teve impacto
direto na extensão da área recoberta pelo biofilme (Figura 1B).
Comparativamente ao ensaio sem THPS, o recobrimento das superfícies dos CPs
expostos à água produzida tratada com THPS foi menor. Provavelmente, isto se
deve a maior ação do THPS sobre as BRS. Porém, conforme constatado nos
ensaios da CMI, para alcançar igual desempenho contra as demais populações
bacterianas seria necessário aplicar doses elevadas deste biocida. Também
deve ser considerada a sua rápida degradação no ambiente, que resulta em
perda da atividade antimicrobiana (ZHAO et al, 2008).
A Figura 1 D apresenta superfícies de aço duplex expostas à AP com
microrganismos após tratamento com THPS. Neste sistema não foi detectada a
presença de pites na superfície. Neste caso, sugere-se que apesar do THPS
ter sido mais efetivo contra as BRS, o mesmo possibilitou a formação de
biofilme na superfície do metal, entretanto, não houve ataque da superfície
metálica. Isto confirma a participação das BRS na corrosão microbiológica.
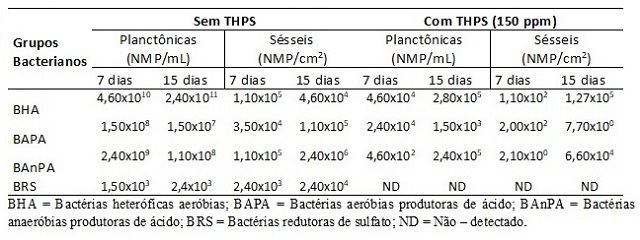
Concentração celular das populações bacterianas na fase planctônica e séssil em água produzida sem e com aplicação de THPS (150 ppm)

Fotomicrografias dos biofilmes formados sobre o CPs de aço duplex em água produzida decorridas 15 dias (A e C – Sem THPS; B e D - Com THPS).
Conclusões
Os resultados demonstraram que o THPS foi efetivo contra as BRS a partir da concentração de 50 ppm; O THPS inibiu o crescimento bacteriano de todos os grupos a partir de 150 (efeito bacteriostático) tendo efeito bactericida somente na concentração de 200 ppm; Durante o período experimental, não foi detectado a presença das BRS (150 ppm de THPS) e observou-se a ausência de pites nas superfícies metálicas, demonstrando assim a efetiva participação deste grupo na corrosão microbiológica.
Agradecimentos
Os autores agradecem à Fundação de Amparo à Pesquisa e Desenvolvimento Científico do Maranhão (FAPEMA) e a Coordenação de Aperfeiçoamento de Pessoal de Nível Superior (CAPES).
Referências
ABELHO, M. Protocolo de Microbiologia Ambiental parte 3: Microbiologia Aplicada. Escola Superior de Agrária. Instituto Politécnico de Coimbra, 2013. ANGELL, P., "Understanding microbially influenced corrosion as biofilm-mediated changes in surface chemistry", Curr. Opinion Biotechnol., 10, p. 269-272, 1999. ANTONY, P.J.; RAMAN, R.K.S.; MOHANRAM, R.; KUMAR, P.; RAMAN, R. Influence of termal aging on sulfate-reducing bactéria (SRB)-influenced corrosion behaviour of 2205 duplex stainless steel. Corrosion Science, p. 1858-1864, 2008. BEECH IB, SUNNER J. Biocorrosion: towards understanding interactions between biofilms and metals. Curr Opin Biotechnol;15.P.181–6, 2004. GAYLARDE, C. C. E MORTON, L.H.G. Deteriogenic biofilms on building and their control: a review. Biofouling, 14(1), 59-74, 1999. GENTIL, V. Corrosão. 5ªed. Livros Técnicos e Científicos Editora S.A., Rio de Janeiro, 2011. KING, R. A.; MILLER, J. D. A. Corrosion by the Sulphate-reducing Bacteria. Nature 233, 491 – 492, 1971. LARSEN J.; SANDERS P.F.; TALBOT R.E. Experience with the use of Tetrakis hydroxymethyl phosphonium Sulfate (THPS) for the Control of Downhole Hydrogen Sulfide. CORROSION. Paper 123. 2000. LEWANDOWSKI, Z.; BOLTZ, J. P. Biofilms in water and wastewater treatment. In: Peter Wilderer (ed). Treatise on Water Science, Oxford: Academic Press; v. 4, p. 529-570, 2011. LIANG, C.H.; WANG, H.; HUANG, N.B.; Effects og Sulphate-reducing Bacteria on Corrosion Behaviour of 2205 Duplex Stainless Steel. Journal of Iron and Steel Research, p.444-450, 2014. POSTGATE, J. R. The sulphate-reducing bacteria. 2ª ed. Press Sindicate of the University of Cambridge, New York, 1984. RAJASEKAR, A.; TING, Y.P. Role of inorganic and organic medium in the corrosion behavior of Bacillus megaterium and Pseudomonas sp. in stainless steel SS 304, Ind. Eng. Chem. Res. 50 p.12534–12541, 2011. VAN LOOSDRECHT, M. C. M.; HEIJNEN, J. J.; EBERL, H.; KREFT,; J. PICIOREANU, C. Mathematical modelling of biofilm structures. Antonie van Leeuwenhoek, v. 81. p. 245-256, 2002. VIDELA, H.A. Biological Corrosion Research in Latin America - Past, Present and Future. Biodeterioration Abstracts, p. 1-11, 1990. VIDELA, H.A. Biocorrosão, biofouling e biodeterioração de materiais, 1a ed. São Paulo: Ed. Edgard Blucher Ltda, p.148. 2003. ZHAO, J.W.; WEN, J.; GU, T.; CRUZ, k.; ARAMCO, S. Mechanistic modeling of anaerobic THPS biocide degradation under akaline conditions. Materials Performance, august, p. 62-69, 2009.











