Cinética da reação de transesterificação do biodiesel por ressonância magnética nuclear de alto campo
ISBN 978-85-85905-23-1
Área
Físico-Química
Autores
Borsato, D. (UEL) ; Galvan, D. (UEL) ; Aguiar, L.M. (UEL) ; Rohwedder, J.J.R. (UNICAMP) ; Killner, M.H.M. (UEL) ; Quadri, M.B. (UFSC) ; Ferreira, B.A.D. (UEL) ; Messias, G.B. (UEL) ; Chendynski, L.T. (IFPR)
Resumo
Foi realizado um estudo quantitativo dos tri- (TG), di- (DG), monoglicerídeos (MG) e Fatty Acid Methyl Esters (FAME) presentes na reação de transesterificação baseados em espectros de high–field Proton Nuclear Magnetic Resonance (HF 1H NMR). As equações propostas foram fundamentadas em dados espectrais que permitiram determinar a porcentagem molar dos diferentes tipos de compostos formados na reação. Os valores das constantes de velocidades estimadas e otimizadas pelo método de Levenberg-Marquardt foram k1 (3,356x10-4; 1,2001x10-4), k2 (1,1452x10-3; 5,1459x10-4), k3 (3,2602x10-3; 7,7052x10-4) e as velocidades reversas foram k4r (1,1306x10-4; 2,9999x10-4), k5r (1,1337x10-3; 3,2950x10-4), k6r (2,6875x10-4; 5,2250x10-4) m3/(s.mol) na concentração de 0,75% e 0,50% de NaOH, respectivamente.
Palavras chaves
Ressonância Magnética Nuc; COMSOL; cinética
Introdução
A principal reação química de obtenção do biodiesel é a de transesterificação, que ocorre com um óleo vegetal e/ou gorduras animais na presença de um álcool de cadeia curta. Esta reação é promovida por um catalisador homegêneo ou heterogêneo (ácido ou básico), com excesso de álcool para deslocar o equilíbrio no sentido da formação de produtos, gerando ésteres e glicerina (SHAHID; JAMAL, 2011). A reação de transesterificação de óleos e gorduras consiste de um conjunto de três etapas consecutivas e reversíveis. Primeiramente, as moléculas de triglicerídeos (TG) reagem com álcool, neste caso o metanol (MeOH) formando diglicerídeos (DG) que, por sua vez, é convertido em monoglicerídeo (MG) e, finalmente em glicerol (GL), em cada uma destas estapas da reação há formação de uma molécula de Fatty Acid Methyl Esters (FAME), onde k1-6 são as constantes de velocidade de formação e reversas. As reações são reversíveis, embora o equilíbrio químico favoreça a formação de glicerol e ésteres (NOUREDDINI; ZHU, 1997). O monitoramento da reação de transesterificação na grande maioria dos estudos é utilizando métodos cromatográficos, tais como: Cromatografia Líquida de Alta Eficiência em inglês High–performance liquid chromatography (HPLC) (NOUREDDINI & ZHU, 1997) e Cromatografica Gasosa em inglês Gas Chromatography – Flame Ionization Detector (CG–FID) (BAMBASE et al., 2007). Porém, estas técnicas apresentam algumas desvantagens quando comparadas aos métodos espectroscópicos de Ressonância Magnética Nuclear em inglês Nuclear Magnetic Resonance (NMR), como a necessidade de pré–tratamento da amostra, ser uma análise destrutiva, apresentar longo tempo de análise, não permitir o monitoramento online da reação, entre outras. A simulação do processo de produção de biodiesel através de modelagem é de grande importância, pois possibilita predizer o comportamento do sistema de produção, além de auxiliar na solução dos problemas relacionados ao projeto e otimização do processo, assim como avaliar a utilização de diferentes catalisadores inorgânicos durante a reação de transesterificação através de parâmetros cinéticos. Utilizando a simulação desta maneira tem a vantagem do baixo custo e tempo de processamento em comparação com a fabricação de dispositivos de teste, permitindo estudar várias variáveis (GALANTE, 2012). O presente trabalho propõe a análise qualitativa e quantitativa de todos os diferentes produtos da reação de transesterificação por high–field Proton Nuclear Magnetic Resonance (HF 1H NMR) e a determinação dos parâmetros cinéticos na plataforma do COMSOL Multiphysics®.
Material e métodos
As reações de transesterificação foram realizadas misturando 500 mL de óleo de soja, 140 mL de metanol (proporção 6:1 M) e 2,50 g ou 3,75 g de hidróxido de sódio (0,50% e 0,75% m/m da base em relação ao óleo), previamente dissolvido em metanol, com agitação mecânica de 150 rpm, durante 62 min. e mantendo a temperatura ambiente de 20±2 ºC. Foram retirados espectros (HF 1H NMR) e alíquotas da reação nos tempos de 3, 7, 10, 14, 18, 26, 34, 42, 50 e 62 min., o tempo de reação começou a contar com a adição da solução de NaOH:metanol no óleo de soja. Foram retiradas alíquotas de 15 mL do meio reacional em cada intervalo de tempo, adicionadas em um tubo contendo 1,5 mL de ácido acético glacial para neutralizar o NaOH utilizado como catalisador na reação. Sequencialmente, após a homogeneização, as amostras foram lavadas três vezes com água destilada, 50 mL de água para cada lavagem, e centrifugadas a 2300 rpm a temperatura ambiente. A fase orgânica remanescente foram secas em sulfato de sódio anidro, e centrifugadas a 4000 rpm por 10 min., para posterior análise em HF 1H NMR (Bruker–400 MHz). Para a aquisição dos espectros se utilizou 50 µL de amostra dissolvidas em 500 µL de CDCl3 com TMS. A análise dos dados de HF 1H NMR foram processados através de uma rotina escrita nos softwares Matlab® 2015a (MathWorks, USA). Para a seleção da área de integração representada pelo TG, 1,2–DG, 1,3–DG, 1–MG, 2–MG e FAME presentes na reação, também foram obtidas por uma rotina escrita no Matlab. As faixas de seleção das integrais consideradas foram seguindo estudos relatados por Nieva–Echevarría et al. (2014), com algumas adaptações. Para cada faixa de integração foi realizado um ajuste polinomial da curva afim de se obter a área do pico mais precisamente realizado pela função de integração numérica “trapezoidal” do software Matlab, sobre as diferentes regiões mencionadas. A simulação da reação de transesterificação foi realizada utilizando o software COMSOL Multiphysics® e as interfaces físicas "Chemical Reaction Engineering" e “Optimization Module”. As equações foram selecionadas em definições globais e as constantes de velocidades (kn) de formação e reversa da reação de transesterificação, foram estimadas e otimizadas pelo método de Levenberg-Marquardt, aplicando um modelo cinético de segunda ordem.
Resultado e discussão
As equações propostas derivadas de dados espectrais de HF 1H NMR usados para
quantificar os compostos da reação de transesterificação são apresentadas a
seguir:
C1-MG = 6 × (I1–MG / IAcy)
C2-MG = 6 × (I2–MG / IAcy)
C1,2-DG = 6 × (I1,2–DG / IAcy)
C TG = 3 × ((ITG – I1,2–DG) / IAcy)
C 1,3-DG = 1,2 × (I1,3–DG – (((2 × I1–MG) + (2 × I1,2–DG)) + 2 × (ITG –
I1,2–DG)) / IAcy)
Os perfis cinéticos gerados pela média das triplicatas das reações
utilizando as taxas de conversões obtidas pelas equações propostas por HF 1H
NMR são apresentados na Figura 1.
De acordo com a Figura 1, nas etapas iniciais da reação (entre
aproximadamente 0 a 15 min. (a) e 0 a 5 min. (b)), é possível observar que é
uma região controlado por transferência da massa, ou seja, lenta,
possivelmente pela temperatura que foram conduzidas as reações. Dos 15 min.
(a) e 5 min. (b) adiante, é possível observar uma região controlada
cineticamente, ou seja, rápida, principalmente na reação que contem 0,75%
m/m de catalisador. E por fim uma região lenta (aproximadamente 62 min. (a)
e 50 min. (b), que representa o equilíbrio da reação (NOUREDDINI & ZHU,
1997). O comportamento da reação de transesterificação baseado em análise de
HF 1H NMR foi semelhante quando comparados as técnicas consideradas de
referência para tal análise como HPLC (NOUREDDINI & ZHU, 1997) e CG–FID
(BAMBASE et al., 2007).
Observa–se ainda o aumento na concentração de FAME seguido por um decréscimo
na concentração de TG. Além de uma discreta formação dos intermediários 1,3–
DG, 1,2–DG, 1–MG e 2–MG com um aumento da concentração inicial ao longo do
tempo, seguida do decréscimo da concentração dos mesmos.
A simulação da reação de transesterificação foi implementada em uma dimensão
0D. Foi considerado as três reações reversíveis que permitiram a
determinação das constantes de velocidade para a produção de biodiesel
(Figura 2).
A Figura 2, apresenta o progresso da reação de transesterificação de óleo de
soja, avaliado durante um tempo de 3600 s na temperatura de 20 ºC. Nas
etapas iniciais da reação é possível observar uma mudança no perfil cinético
das reações, sendo que a reação com 0,75% de NaOH ocorre mais rapidamente.
Entre 0 e 2500 s, a produção de FAME foi rápida, entrando em equilíbrio em
aproximadamente 3600 s. O aumento na concentração de FAME foi seguido por um
aumento na concentração de GL, uma vez que foi libertada a partir de
moléculas de TG. Pode-se também notar a formação dos intermediários MG e DG,
devido a um pequeno aumento da concentração inicial ao longo da reação,
seguida do decréscimo da concentração próximos a 3600 s.
Os valores das constantes de velocidades estimadas e otimizadas pelo método
de Levenberg-Marquardt de formação foram k1 (3,356x10-4; 1,2001x10-4), k2
(1,1452x10-3; 5,1459x10-4), k3 (3,2602x10-3; 7,7052x10-4) m3/(s.mol) e as
constantes de velocidades reversas foram k4r (1,1306x10-4; 2,9999x10-4), k5r
(1,1337x10-3; 3,2950x10-4), k6r (2,6875x10-4; 5,2250x10-4) m3/(s.mol) para
as concentrações de 0,75% e 0,50% de NaOH, respectivamente. Valores de
constantes de velocidades foram superiores para as reações com 0,75% de NaOH
quando comparadas as reações com 0,5%, e todas as velocidades de formação
foram superiores as reversas para ambas as reações.
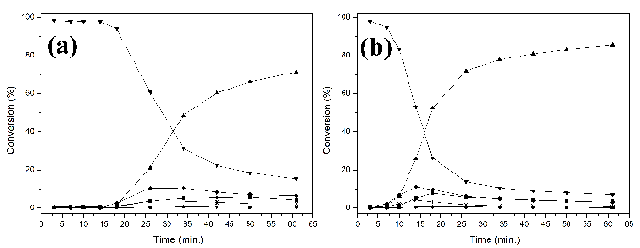
Perfil cinético da reação de transesterificação usando 0,50% (a) e 0,75% (b) de NaOH (m/m). Onde: ▼ TG, ♦ 1,3–DG, ❊ 1,2–DG, ● 2–MG, ■ 1–MG, ▲ FAME.
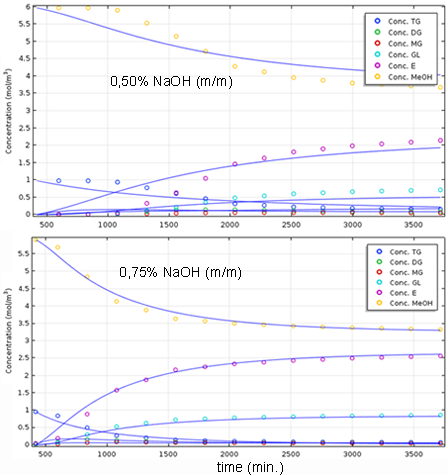
Distribuição de concentração (mol/m3) com base nas determinações experimentais por HF 1H NMR (○ experimental) pelo simulado (- simulado) da reação.
Conclusões
Este trabalho provou a utilidade de HF 1H NMR para estudar qualitativamente e quantitativamente a composição da mistura durante o progresso da reação de transesterificação. Em comparação com outras metodologias aplicadas, esta abordagem permite um estudo global da amostra, fornecendo informações detalhadas sobre todos os tipos de compostos presentes, de forma simples e rápida usando apenas um dispositivo. A simulação computacional, demostrou ser uma ferramenta eficiente e viável para a determinação dos parâmetros cinéticos da reação, permitindo avaliar diferentes variáveis de processos ao mesmo tempo, como matéria prima, álcool, catalisador e reator empregado na sua produção, através de parâmetros cinéticos determinados experimentalmente por HF 1H NMR.
Agradecimentos
A UEL, UNICAMP e CAPES pela concessão de bolsas.
Referências
BAMBASE JÚNIOR, M. E.; NAKAMURA, N.; TANAKA, J.; MATSUMURA, M. Kinetics of hydroxide–catalyzed methanolysis of crude sunflower oil for the production of fuel–grade methyl esters. Journal of Chemical Technology and Biotechnology, v. 82, p. 273–280, 2007.
GALANTE, R. M. Modelagem e simulação de um reator tubular contínuo para a produção de biodiesel. 2012. 146 f. Tese (Doutorado em Engenharia Química) – Programa de Pós Graduação em Engenharia Química, Universidade Federal de Santa Catarina. Florianópolis, 2012.
NIEVA–ECHEVARRÍA, B.; GOICOECHEA, E.; MANZANOS, M. J.; GUILLÉN, M. D. A method based on 1H NMR spectral data useful to evaluate the hydrolysis level in complex lipid mixtures. Food Research International, v. 66, p. 379–387, 2014.
NOUREDDINI, H.; ZHU, D. Kinetics of Transesterification of Soybean Oil. Journal of the American Oil Chemists' Society, v. 74, p. 1457–1463, 1997.
SHAHID, E. M.; JAMAL, Y. Production of biodiesel: A technical review. Renewable and Sustainable Energy Reviews, v. 15, p. 4732–4745, 2011.











