Síntese Estereosseletiva de Eninos a Partir de Reações de Acoplamento
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
Santos, C.L.A.A. (UFPE) ; Santos, J.A.M. (UFRPE) ; Silva, W.P. (UFPE) ; Silva, E.L.S. (UFPE) ; Freitas, J.C.R. (UFCG) ; Oliveira, R.A. (UFPE) ; Silva, T.G. (UFPE) ; Menezes, P.H. (UFPE)
Resumo
A Química Medicinal envolve diversos fatores como a descoberta de novas moléculas bioativas, a elucidação dos mecanismos de ação e as relações existentes entre as estruturas dos fármacos e suas atividades farmacológicas. Neste contexto, a hibridação molecular (HM) é uma estratégia clássica de conjugação de estruturas de compostos bioativos distintos em uma única molécula, sendo uma alternativa eficaz para a arquitetura de novos compostos. Este trabalho teve como foco central o planejamento e a síntese de compostos contendo duas unidades farmacofóricas: uma enona (bom aceptor de Michael) e um enino. O composto desejado foi obtido de maneira estereosseletiva a partir da reação de acoplamento entre um enulosídeo e um telureto vinílico utilizando um sistema catalítico envolvendo PdCl2 e CuI.
Palavras chaves
Enulosídeos; Teluretos vinílicos; Acoplamento
Introdução
Os eninos e enediínos são unidades estruturais presentes em antibióticos com potente atividade antitumoral como as calicheamicinas, esperamicinas, dinemicinas e a neocarzinostatina (KRAKA; CREMER, 2013). A importância dessa funcionalidade fez com que diversos grupos de pesquisa desenvolvessem os mais diferentes métodos para a preparação de compostos contendo essa unidade estrutural. Já as delta-lactonas alfa,beta-insaturadas são unidades estruturais encontradas em diversos produtos naturais como a fostriecina, citostatina e a leptomicina B (BARROS et al, 2014; TROST; DNOPF; BRINDLE, 2016). Estes compostos atuam como potenciais aceptores de Michael, em especial para os resíduos nucleofílicos de aminoácidos presentes em receptores naturais, permitindo que os mesmos se liguem a uma enzima-alvo (SANTOS et al, 2016). Como resultado, diferentes atividades biológicas são observadas para compostos contendo essa unidade estrutural Desse modo, a busca por compostos estruturalmente mais simples e que exibam propriedades biológicas semelhantes é um assunto bastante atual. Adicionalmente, a obtenção de novas moléculas contendo em sua estrutura estas duas unidades farmacóforicas ativas poderiam potencializar a atividade antitumoral destes compostos.
Material e métodos
Para síntese dos enulosídeos foi utilizado a metodologia descrita por Santos et al. (2016). Os teluretos vinílicos foram obtidos pelo método de Oliveira et al. (2010). Para a síntese dos eninos, em um balão de duas bocas sob atmosfera de Ar, foi adicionado PdCl2 (35 mg, 40 mol %), CuI (38 mg, 40 mol%). Em seguida foi adicionado MeOH seco (5 mL) e o telureto vinílico 8a (145 mg, 0,5 mmol). A mistura foi mantida sob agitação à temperatura ambiente durante 15 minutos e então foi adicionado o composto 5a (91 mg, 1 mmol) e Et3N (0,3 mL). A reação foi monitorada por CCD e após o término foi filtrada em um plug de sílica/celite. A mistura foi extraída com AcOEt (3 x 20 mL) e lavada com solução saturada de NaCl (30 mL). As fases orgânicas foram combinadas e secas sob MgSO4 anidro e concentradas in vacuo. O resíduo foi purificado por cromatografia em coluna de sílica gel utilizando hexano como eluente.
Resultado e discussão
A molécula-alvo foi dividida em dois fragmentos principais A e B: o
fragmento A é um enulosídeo, sintetizado a partir de reações sucessivas
empregando-se o tri-O-acetil-D-glucal, disponível comercialmente. O
fragmento B é um telureto vinílico com estereoquímica Z e pode ser obtido a
partir da reação de hidroteluração do alquino correspondente. O fragmento A
foi preparado a partir de uma sequência sintética desenvolvida por nosso
grupo de pesquisa. A reação de glicosidação empregando-se como precursor o
tri-O-acetil-D-glucal, 1 levou ao glicosídeo correspondente 2 em bom
rendimento e seletividade alfa. A posterior reação de hidrólise seguida
da oxidação quimiosseletiva levou ao enulosídeo desejado 3 (Fragmento A) em
um rendimento global de 80% após três etapas (Esquema 1).
O Fragmento B foi preparado a partir da reação entre o fenilacetileno, 4
disponível comercialmente, e um ânion telurolato, gerado in situ em meio
prótico a partir da adição de NaBH4 ao ditelureto de dibutila, 5. O telureto
vinílico Z, 6 foi obtido como produto exclusivo da reação (Esquema 2).
A reação de acoplamento entre os fragmentos A e B foi realizada a partir do
procedimento descrito por Zeni e colaboradores e levou ao produto desejado 7
em um rendimento de 61% com retenção de geometria da ligação dupla (Esquema
3).
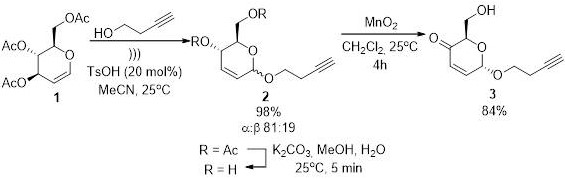
Síntese dos enulosídeos
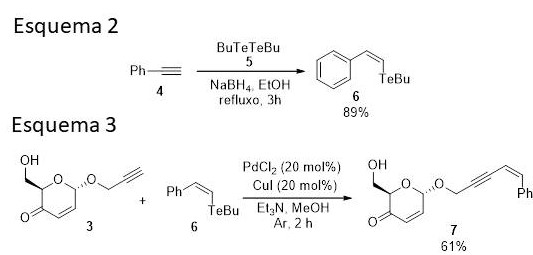
Esquema 2, Síntese dos teluretos vinílicos. Esquema 3, reação de acoplamentos entre os teluretos vinílicos e os enulosídeos.
Conclusões
A estratégia sintética empregada mostrou-se viável uma vez que os fragmentos A e B foram obtidos em bons rendimentos. A estratégia é flexível, permitindo mudanças no design de novos compostos ativos contendo duas porções farmacofóricas: uma enona (um bom aceptor de Michael) e um enino. Estudos da atividade antitumoral do composto sintetizado encontram-se em andamento em nosso laboratório.
Agradecimentos
FACEPE; CNPq, UFPE-dQF
Referências
BARROS, M.E.; FREITAS, J.C.R.; OLIVEIRA, J.M.; DA CRUZ, C.H.B.; DA SILVA, P.B.N.; DE ARAUJO, L.C.C.; MILITAO, G.C.G.; DA SILVA, T.G.; OLIVEIRA, R.A.; MENEZES, P.H. Synthesis and Evaluation of (-)-Massoialactone and Analogues as Potential Anticancer and Anti-inflammatory Agents. European Journal of Medicinal Chemistry, 76, 291-300, 2014.
KRAKA, E.; CREMER, D. Enediynes, Enyne-Allenes, Their Reactions, and Beyond. Wiley Interdisciplinary Reviews: Computational Molecular Science, 4(4), 285–324, 2013.
OLIVEIRA, J. M.; PALMEIRA, D. J.; COMASSETO, J. V.; MENEZES, P. H. Influence of different protecting groups on the regioselectivity of the hydrotelluration reaction of hydroxy alkynes. Journal of the Brazilian Chemical Society. 21, 362-366, 2010.
SANTOS, J.A.M.; SANTOS, C.S.; ALMEIDA, C.L.A.; SILVA, T.D.S.; FREITAS FILHO, J.R.; MILITAO, G.C.G. SILVA, T.G.; CRUZ, C.H.B.; FREITAS, J.C.R.; MENEZES, P.H. . Structure-based Design, Synthesis and Antitumoral Evaluation of Enulosides. European Journal of Medicinal Chemistry. 128, 192-201, 2017.
TROST, B.M.; DNOPF, J.D.; BRINDLE, C.S. Synthetic Strategies Employed for the Construction of Fostriecin and Related Natural Products. Chem. Rev. 116, 15035−15088, 2016.









