CARACTERIZAÇÃO DAS FORMAS POLIMÓRFICAS DA OLANZAPINA POR INFRAVERMELHO
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
Lobo, V. (UTFPR) ; Rhoden, R. (UTFPR) ; Rosa, M. (UNIOESTE)
Resumo
A olanzapina (OLZ) é um dos agentes antipsicóticos atípicos mais utilizados no tratamento de pacientes que não respondem ao tratamento neuroléptico clássico, sendo efetivo no tratamento de sintomas positivos e negativos da esquizofrenia e da desordem bipolar. Apresenta-se como um pó cristalino amarelo, sendo solúvel em n-propanol, ligeiramente solúvel em acetonitrila, pouco solúvel em metanol e etanol absoluto e praticamente insolúvel em água, podendo se cristalizar em pelo menos 60 formas polimórficas. As Formas I e II são as formas anidras mais comuns e disponíveis comercialmente, sendo a Forma II a termodinamicamente mais estável. No presente estudo três Insumos Farmacêuticos Ativos (IFAs) foram caracterizados e identificados utilizando a análise de Infravermelho.
Palavras chaves
análise estrutural; polimorfismo; princípio ativo
Introdução
A esquizofrenia, segundo a Organização Mundial da Saúde (2018), é um transtorno mental grave, caracterizado por profundas rupturas no pensamento, afetando a linguagem, a percepção e o senso de si. Pode ser caracterizada por sintomas positivos, como delírios e alucinações, e negativos, como embotamento afetivo, retraimento emocional e pensamento estereotipado (BRESSANA; PILOWSKY, 2003; TESTA, 2014). A esquizofrenia recebe significativa atenção dos pesquisadores, pois representa um dos maiores desafios da medicina porque sua fisiopatologia ainda não está bem definida e as medicações existentes não satisfazem completamente aos anseios terapêuticos (BRESSANA e PILOWSKI, 2003; FREITAS, 2012; TESTA, 2014). A OLZ faz parte do grupo de drogas nominadas de atípicas ou de segunda geração, cuja principal característica é promover a ação antipsicótica com um maior espectro de ação, apresentando maiores índices de eficácia, melhora cognitiva dos pacientes, e menor incidência dos efeitos extrapiramidais, tais como ganho de peso, sonolência e/ou sedação (LEUCHT et al., 2009; MOITA, MOURA e RÊGO, 2010; TESTA, 2014). Este fármaco pertence à classe das tienobenzodiazepinas, obtida a partir de modificações na estrutura química da clozapina, trazendo como vantagem a ausência de efeitos hematológicos (PERES FILHO et al., 2010; FREITAS, 2012). O desenvolvimento de formas farmacêuticas sólidas depende muito das propriedades físico-químicas do princípio ativo e dos excipientes. As propriedades físicas estão intimamente ligadas às especificações do produto final, como pureza, uniformidade, dissolução, estabilidade, aspecto e dureza. Elas estão frequentemente no centro dos problemas de fabricação que podem emergir inesperadamente durante o ciclo de vida do produto. A OLZ é um fármaco que apresenta complicações no processo de fabricação devido a sua habilidade de formar polimorfos, dentre eles formas hidratadas, anidras e solvatadas. A influência do polimorfismo na biodisponibilidade é considerada a mais importante consequência do fenômeno na área farmacêutica e ocorre quando existe dependência entre a velocidade de dissolução in vivo e a velocidade de absorção. Assim, a determinação de condições ótimas e controladas para obter formas farmacêuticas sólidas de propriedades conhecidas desse fármaco é importante para a indústria farmacêutica (MOURA, 2009; PERES FILHO et al., 2010; ARAUJO, 2012; CAVALLARI, 2013).
Material e métodos
Os IFAs utilizados para o estudo foram doados 3 amostras pela indústria de medicamentos genéricos, as quais foram identificadas como amostra A, B e C. Conforme informações do fornecedor tratavam-se das formas polimórficas I, II micronizada e I com partícula superior a 60 μm, respectivamente. Para identificação das formas polimórficas foi utilizado a substância química de referência OLZ (CAS 132539-06-1), com teor declarado de 99,6% do lote G0L368, da United States Pharmacopeia (USP, Rockville, EUA). A técnica de infravermelho foi realizada com a finalidade de comparar os espectros dos IFAs e identificar distintos modos vibracionais da OLZ I e OLZ II, através da comparação com o espectro do padrão farmacopeico. Os espectros foram obtidos por meio da análise direta da amostra sólida de OLZ I E OLZ II, utilizando o espectrômetro Frontier da Perkin-Elmer com o Universal ATR Sampling Accessory, os dados foram coletados a temperatura ambiente, com resolução de 4 cm-1, realizando 10 scans, na região entre 4000 e 650 cm-1, e os resultados foram processados através do software Spectrum ES licenciado por Perkin-Elmer.
Resultado e discussão
As análises por FT-IR permitem estudar a natureza vibracional das moléculas,
as quais podem mostrar evidências das propriedades cristalinas dos
compostos.
A análise vibracional de FT-IR pode ser realizada utilizando pastilhas de
KBr, em uma faixa de 4000 a 400 cm-1, contudo, requer alguns cuidados
essenciais para um bom resultado, tais como, KBr de grau espectroscópico,
preparo da amostra apropriado no momento da prensagem da pastilha (proporção
de KBr e amostra adequada e/ou mistura homogênea, pressão e tempo
apropriados) e principalmente dessecação adequada do KBr, sendo que se esta
etapa não for realizada de maneira correta, pode ser verificada a presença
de umidade (água) devido a marcante banda de vibração em aproximadamente
3400 cm-1, relativa à ligação OH. Já a técnica de ATR (Attenuated Total
Reflection), que segundo o Capítulo Geral da USP <197> [USP 41, 2018] é um
método alternativo ao da pastilha de KBr, pode ser feita com cristal de
ZnSe, germânio ou diamante e permite a leitura direta da amostra na faixa de
4000 a 650 cm-1, sem etapas de preparo, tal como da pastilha de KBr e sem os
seus inconvenientes, permitindo uma análise rápida, mais reprodutível e com
melhor resolução (PIERACIO, 2018).
A Figura 1 mostra o espectro de FT-IR do padrão farmacopeico de OLZ exibindo
bandas características em 3209 cm-1 para as ligações N-H, em 2934, 2837 e
2792 cm-1 para as ligações C-H, além das bandas em 1469, 1446, 1410, 1288,
1272 e 1260 cm-1, em 1582 e 1556 cm-1 para as ligações N=C e em 744 cm-1
para a ligação C-H dos sistemas aromáticos. O padrão farmacopeico
corresponde a forma estável (Forma II), de acordo com TIWARI, CHAWLA e
BANSAL (2007).
Na Figura 2a, as deformações dos grupos metil, metileno e C-H são
encontradas na região espectral entre 1500-1300 cm-1, nessa região foi
encontrada uma banda em 1517 cm-1, que caracteriza a forma polimórfica I. Já
na região entre 1300 e 1100 cm-1, são dominantes as ligações C-C e C-N, e
devido às sobreposições das bandas não é possível uma identificação adequada
de algumas características comuns as duas formas polimórficas estudadas
(AYALA et al., 2006; BHARDWAJ et al., 2013; POLLA et al., 2005; REUTZEL-
EDENS et al., 2003).
Abaixo de 1100 cm-1, as bandas são menos sobrepostas e estão relacionadas à
deformação e as torções dos anéis que dão origem a movimentos acoplados.
Através dessas vibrações pode-se identificar picos característicos da forma
I em 866 e 707 cm-1 (Figura 1) e picos da forma II em 760 cm-1 (Figura 2b)
(AYALA et al., 2006; BHARDWAJ et al., 2013; POLLA et al., 2005; TESTA, 2014;
WAWRZYCKA-GORCZYCA et al., 2007).
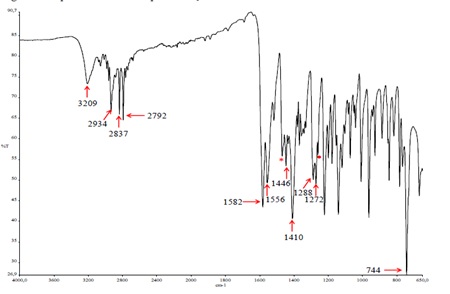
Espectro de IV do princípio ativo padrão.
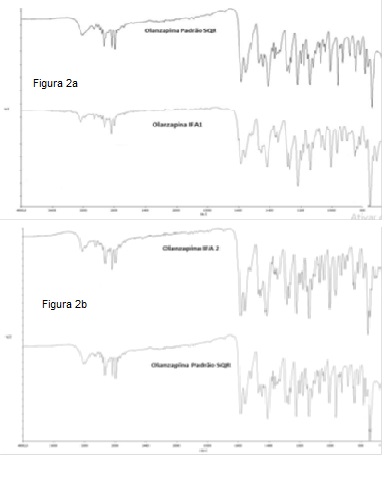
Espectros de IV dos compostos polimorfos I e II.
Conclusões
As análises de FT-IR comprovaram que as IFAs analisadas eram as formas I e II conforme informado pelo fornecedor. Quanto às formas polimórficas que um fármaco pode assumir apenas uma é a forma termodinamicamente estável a uma dada temperatura e pressão, as demais formas termodinamicamente instáveis tendem a se converterem com o tempo à forma mais estável. Com o estudo das formas polimórficas I e II da OLZ, pode-se verificar, e reafirmar, que a forma II é mais estável que a forma I, conforme citado na literatura consultada.
Agradecimentos
UTFPR. Indústria Farmacêutica Prati Donadduzi.
Referências
ARAUJO, G.L.B., PITALUGA JR. A., ANTONIO, S.G., SANTOS, C.O.P., MATOS, J.R. Polimorfismo na produção de medicamentos. Revista de Ciências Farmacêuticas básica e aplica, v.33, p. 27-36, 2012.
AYALA, A. P. et al. Solid state characterization of olanzapine polymorphs using vibrational spectroscopy. International Journal of Pharmaceutics, v. 326, n. 1–2, p. 69–79, 2006.
BHARDWAJ, R. M. et al. Exploring the experimental and computed crystal energy landscape of olanzapine. Crystal Growth and Design, v. 13, n. 4, p. 1602–1617, 2013.
BRESSANA, R.A.; PILOWSKY L.S. Hipótese glutamatérgica da esquizofrenia. Rev. Bras. Psiquiatr., v.25, n.3, p. 177-83, 2003.
CAVALLARI, C., SANTOS, B., FINI, A. Olanzapine Solvates. Journal of Pharmaceutical Sciences, v.102, p. 4046-4056, 2013.
FREITAS, M.R.; ROLIM, L.A.; SOARES, M.F.R.; ROLIM NETO, P.J.; ALBUQUERQUE, M.M.; SOARES SOBRINHO, J.L. Inclusion complex of methyl- beta-cyclodextrin and olanzapine as potential drug delivery system for schizophrenia. Carbohydrate Polymers, v.89, p.1095-1100, 2012.
LEUCHT, S.; CORVES, C.; ARBTER, D.; ENGEL, R.R., LI, C., DAVIS, J.M. Second –generation versus first generation antipsychotic drugs for schizophrenia: a meta-anaysis. Lancet. v.373, n.9657, p.31-41, 2009.
MOITA, G.C., MOURA, J.I.M. RÊGO, J.F., Determinação de olanzapina em formulações farmacêuticas por espectrofotometria: desenvolvimento e validação. Quim. Nova, v.33, n.00, p.1-7, 2010.
MOURA, J.R. Desenvolvimento e validação de metodologia analítica aplicável ao desenvolvimento farmacotécnico de comprimidos de olanzapina. Dissertação de Mestrado – Universidade Federal de Goiás, 2009.
ORGANIZAÇÃO MUNDIAL DA SAÚDE (OMS). Esquizofrenia.
PERES-FILHO, M.J.; GAETI, M.P.N; OLIVEIRA, S.R.; MARRETO, R.N.; LIMA, E.M. Thermoanalytical investigation of olanzapine compatibility with excipients used in solid oral dosage forms. Journal of Thermal Analysis and Calorimetry, v. 104, p. 255-260, 2011.
POLLA, G. I. et al. Thermal behaviour and stability in Olanzapine. International Journal of Pharmaceutics, v. 301, n. 1–2, p. 33–40, 2005.
REUTZEL-EDENS, S. M. et al. Anhydrates and Hydrates of Olanzapine: Crystallization, Solid-State Characterization, and Structural Relationships. Crystal Growth and Design, v. 3, n. 6, p. 897–907, 2003.
TESTA, C. G. Desenvolvimento de medicamento similar de olanzapina comprimidos revestidos. Rio de Janeiro. p. 189, 2014.
TIWARI, M.; CHAWLA, G.; BANSAL, A. K. Quantification of olanzapine polymorphs using powder X-ray diffraction technique. Journal of Pharmaceutical and Biomedical Analysis, v. 43, n. 3, p. 865–872, 2007.
US PHARMACOPEAIL CONVENTION USP. Usp United State Pharmacopeail Conv. Ed. 40, 2017.
WAWRZYCKA-GORCZYCA, I. et al. Crystal structure of olanzapine and its solvates. Part 3. Two and three-component solvates with water, ethanol, butan-2-ol and dichloromethane. Journal of Molecular Structure, v. 830, n. 1–3, p. 188–197, 30 mar. 2007.









