Nova geração de derivados ftalmido-tiazol: Síntese e Avaliação da atividade anti-T-cruzi
ISBN 978-85-85905-25-5
Área
Química Orgânica
Autores
Sousa, F. (UFPE) ; Santos, I. (UFPE) ; Freitas, L. (UFPE) ; Silva, V. (UFPE) ; Gomes, P.A. (UFPE) ; Santos, A.C. (UFPE) ; Holanda, M. (UFPE) ; Conceicação, J. (UFPE) ; Pereira, V. (FIOCRUZ) ; Leite, A.C. (UFPE)
Resumo
A doença de Chagas é a infecção causada pelo protozoário Trypanosoma cruzi. Apresenta uma fase aguda (doença de Chagas aguda – DCA) que pode ser sintomática ou não, e uma fase crônica, que pode se manifestar nas formas indeterminada, cardíaca, digestiva ou cardiodigestiva. (BRASIL, 2019). O tratamento da doença de chagas deve ser indicado por um médico, após a confirmação da doença. O remédio, chamado benznidazol (BZD). Diante disso, o objetivo do trabalho foi sintetizar inéditos ftalimido-tiazóis e avaliar sua atividade biológica. Como resultado três compostos mostraram-se promissores 4h IC50 4,48μM seguido do 4c IC50 6,07μM e 4b IC50 8,94μM todos apresentaram IC50 menores que o BZD. Diante disso, é de suma importância a realização de pesquisas para o tratamento da doença de chaga
Palavras chaves
Ftalimido-tiazól; Doença da Chagas; T-cruzi
Introdução
As doenças negligenciadas são um conjunto de doenças infecciosas que ocorrem em regiões tropicais e subtropicais de países com economias em desenvolvimento (Ricardo Valverde, FIOCRUZ, 2013). Dentre este conjunto de afecções, destacam-se a Doença de Chagas, causada pelo protozoário Trypanosoma cruzi. De acordo com Solange L. de Castro & Maria de Nazaré C. Soeiro (FIOCRUZ, 2017) o fármaco atualmente utilizado no tratamento da doença de chagas é o Benzinidazol mas este não é eficaz em estágios mais avançados da doença, no entanto, esse fármaco não é boa terapia para o tratamento da doença, pois desencadeia muitos efeitos colaterais, tais como, dor de cabeça e vômitos. Diante disso, fica evidente a necessidade de desenvolvimento de novos fármacos para o tratamento desta doença. As ftalimidas e tiazóis vem sendo alvo de muitas pesquisas, esses compostos possuem atividades promissoras anti-T.cruzi como demonstrado por (GOMES et al., 2016). Diante disso, o objetivo do trabalho foi sintetizar inéditos ftalimido-tiazóis e avaliar as suas propriedades anti-T.cruzi desses compostos.
Material e métodos
A síntese foi realizada no Laboratório de Planejamento em Química Medicinal (LpQM), cuja estrutura geral dos compostos sintetizados encontra-se mostrada na figura 1. Para tal, foi preciso placas de silica para realizar a Cromatografia de Camada Delgada (CCD), n-hexano e acetado como eluentes na proporção 7:3, câmara de ultravioleta para acompanhar a reação, rotavaporador para processos reacionários, além de condensadores e balões de fundo redondo para o uso do refluxo, câmara de ultrassom para algumas etapas de reação, além dos solventes etanol, acetona, diclorometano, dimetilformamida, dimetilsulfóxido e clorofórmio. Para a elucidação estrutural, foi feita análise de Ressonância Magnética Nuclear (RMN) 1H e 13C e Espectroscopia de Massa de Alta Resolução (EMAR). A atividade biológica foi feita em parceria com a Agência FIOCRUZ. As formas tripomastigotas (cepa Y) foram obtidas a partir da infecção in vitro (107 parasitos) da linhagem de células Vero, após estas obterem confluência em cultura. Para determinar o efeito antiproliferativo para formas tripomastigotas da cepa Y (4x106 parasitos/ml), mantidas em meio RPMI+1% de antibiótico+5% de SFB, foram semeadas em placas de 96 poços a 37ºC, juntamente com diferentes concentrações dos compostos (0,19; 1,56; 6,25; 25; 100 µg/ml) por 24h a atmosfera de 5% de CO2. Obteve-se como controle negativo da reação poços sem tratamento e a droga de referência utilizada como controle positivo foi o benzonidazol. Determinou-se a viabilidade parasitária por contagem direta em câmara de Neubauer e, a partir desses valores, obteve-se a IC50. Cada ensaio foi realizado em triplicata.
Resultado e discussão
Como resultado, a tabela 1 apresenta o CC50, IC50 e índice de seletividade (IS) para a linhagem
macrofágica RAW 264.7 na forma tripomastigota do T-cruzi, dos compostos sintetizados
Segundo a tabela, os mais ativos foram 4h IC50 4,48μM seguido do 4c IC50 6,07μM e 4b IC50
8,94μM se comprados com o Benzinidazol (BZD), o qual foi o fármaco usado como referencia com
IC50 14,96μM. Em termos de seletividade, o composto 4b foi cinco vezes mais seletivo que o
BZD, mostrando que o grupo 4-Me-O-Ph como substituinte no C4 do tiazól aumenta sua
seletividade. O composto 4c possui um como grupo substituinte o 3,4-diCl-Ph também no C4 e
mostrou –se quase quatro vezes mais seletivo. Por fim, 4h apresentou seletividade quase cinco
vezes mais seletivo, ele possui em sua estrutura duas substituições a primeira: um grupo fenil no
N3 do tiazol e a segunda: um grupo 4-MeO-Ph no C4 do tiazól, esses grupos também
contribuíram para o aumento da seletividade e consequentemente para o aumento de sua
atividade.
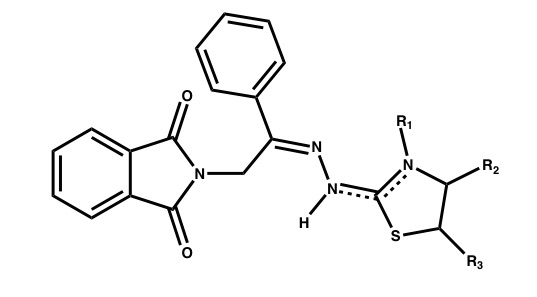
Estrutura dos compostos sintetizados 4a-j
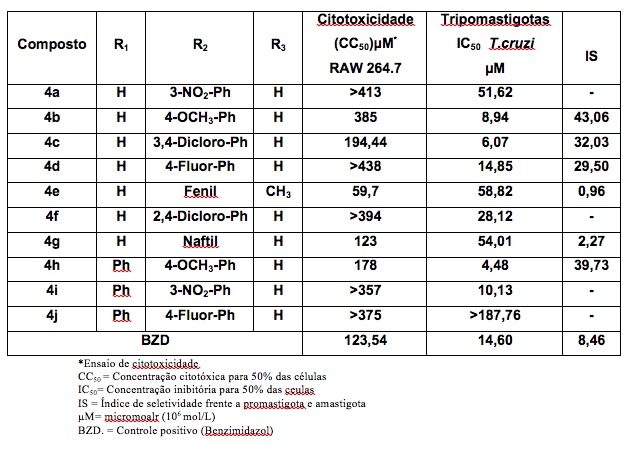
resultado das atividades biológicas dos compostos de 4a-j
Conclusões
Diante do exposto pode-se concluir que, os grupos substituintes 4-MeO-Ph e 3,4-diCl-Ph no C4 do tiazol em 4b e 4c respectivamente, aumentaram consideravelmente a atividade e a seletividade dos compostos, se compardo com o Benzimidazol. Foi demonstrado tambem que a substituição no N3 do anel do tiazól por um grupo fenil mostrou-se bastante promissor. Além disso, todos os compostos sintetizados apresentaram uma menor toxicidade. Assim, diante desses resultados, é de suma importância o investimento em pesquisas para o desenvolvimento de novos fármacos com os grupos ftalmida e tiazol como núcleo.
Agradecimentos
Ao Laboratório de Planejamento em Química Medicinal (LpQM) pelos experimentos feitos, à professora Dra Ana Cristina Lima Leite pela orientação e a todos os IC’s, Mestrandos e Doutorandos do LpQM.
Referências
DE MORAES GOMES, P. A. T. et al. Phthalimido-thiazoles as building blocks and their effects on the growth and morphology of Trypanosoma cruzi. European Journal of Medicinal Chemistry, v. 111, p. 46–57, 2016.
Ricardo Valverde, Doenças Negligenciadas, Agência FIOCRUZ, 2013 (acessado em 16/08/19)
Solange L de Castro & Maria de Nazaré C. Soeiro, Drogas Tripanossomicidas, Agência FICRUZ, 2017 (acessado em 16/08/19)









