PARTICIONAMENTO DA LACTOSE DO SORO DO LEITE ATRAVÉS DE UM SISTEMA AQUOSO DE DUAS FASES COMPOSTO POR POLÍMERO E SAL.
ISBN 978-85-85905-25-5
Área
Bioquímica e Biotecnologia
Autores
Santos, J.L.C.B. (UNIT) ; Souza, R.L. (ITP) ; Soares, C.M.F. (ITP) ; Pereira, M.M. (UNIT) ; Lima, A.S. (ITP)
Resumo
Neste trabalho analisou-se o particionamento da lactose utilizando um ATPS constituído por polietilenoglicol (de massas 300, 400, 600 e 1000 g.mol-1) e sais diferentes, em uma matriz real de soro do leite. O ponto de mistura escolhido foi de 60% de soro de leite, 20% de Polietilenoglicol (PEG) e 20% de sal, onde houve testes iniciais com o PEG400 e consequente otimização utilizando os demais PEG’s. Após a formação dos sistemas, as fases foram analisadas através da metodologia Lane-Eynon, onde verificou-se um particionamento preferencial da lactose para a fase de fundo, alcançando até 92% de eficiência de extração para esta fase. O presente sistema mostra-se uma metodologia barata e simples para extração da lactose do soro do leite podendo ser aplicada para o seu beneficiamento.
Palavras chaves
Lactose; ATPS; Particionamento
Introdução
Atualmente o Brasil é o terceiro maior produtor mundial de leite, conseguindo a produção de mais 24,4 bilhões de litros inspecionados no ano de 2018. Deste montante, aproximadamente 33,98% são utilizados para a produção de queijos (EMBRAPA, 2019). Para produzir um quilo de queijo, a indústria láctea utiliza aproximadamente 10 litros de leite, onde também são gerados cerca de 9 litros de um resíduo denominado soro do leite. Como subproduto, o soro do leite contém cerca de 50% dos nutrientes do leite, apresentando uma cor amarelo-esverdeada, com composição centesimal variada, mas que gira em torno de 93% de agua, 4,3-5,0% de lactose, 0,9% de proteínas e 1,6% de vitaminas, sais minerais e outros componentes (GONZÁLEZ, 1996). Devido ao elevado conteúdo de substâncias orgânicas presentes, apresenta um alto poder poluente, com uma demanda bioquímica de oxigênio (DBO) que varia de 27 a 60 kg·m-3 (PRAZERES et al, 2012). Desta forma, as instituições e pesquisadores tem efetuado esforços para criar alternativas eficientes e sustentáveis de aproveitamento do soro do leite e seus constituintes, pois a utilização industrial desse subproduto contribuirá para o enriquecimento e desenvolvimento de novos produtos alimentícios, ingredientes nutrifuncionais, farmacêuticos e bioquímicos (PELEGRINI et al, 2008). Um dos constituintes do soro do leite é a lactose, um dissacarídeo formado por galactose e glicose com nome cientifico de Galactose-β-1,4-glucose e massa molar de 343,2 g.mol-1. É um açúcar de sabor aprazível, que industrialmente é utilizado na produção de vários produtos, como pães, biscoitos, sorvetes, enlatados, fermentados; é empregado também como excipientes em medicamentos e na indústria químico-farmacêutica é precursora da lactulose, ácido láctico, polilactato, etanol, ácido lactobiônico, lactitol, β-galactosidases e outros (COLOGNESI et al, 2013). Devido a estes potenciais usos, faz-se necessário o aproveitamento da biomolécula presente no soro do leite e um adequado protocolo de extração que consiga um alto grau de pureza, agregando um maior valor econômico à mesma. Desde a década de 50 a comunidade cientifica estuda e utiliza Sistemas aquosos de duas fases (ATPS – Aqueous Two-Phase Systems, em inglês) para a extração e recuperação de compostos químicos, bioquímicos e materiais biológicos; as vantagens desta técnica incluem potencial de expansão, operação contínua, facilidade de integração de processos, baixa toxicidade de fase e biocompatibilidade (ASENJO et al, 2011). ATPS são formados quando compostos hidrofílicos, tais como alguns tipos de polímeros (polietilenoglicol - PEG, dextrano - DEX, polipropilenoglicol - PPG, etc.), sais (fosfatos, sulfatos, citratos, etc.), carboidratos ou líquidos iônicos (ILs) são combinados em certas concentrações críticas, resultando na formação de duas fases hidrofílicas. Estas fases hidrofílicas traduzem a potencialidade dos sistemas aquosos de duas fases em extração de biopotenciais, pois a maioria dos biocompostos necessitam de meios hidrofílicos para manterem suas propriedades intactas (BENAVIDES et al, 2008). Além disto, existe a possibilidade dos ATPS formarem um particionamento trifásico (TPP), onde além das duas fases usuais do sistema, temos a criação de uma fase adicional (interface), onde algum precipitado desejado se formará (VENTURA et al, 2017). Sistemas aquosos de duas fases compostos por PEG e sal já foram aplicados para recuperação de íons metálicos de soluções aquosas (ROGERS et al, 1996), recuperação de corantes alimentares de resíduos de plantas têxteis (HUDDLESTON et al, 1998), extração e recuperação da ovoalbumina da clara do ovo (PEREIRA et al, 2016), recuperação do plasmídeo pDNA. (TRINDADE et al, 2005). ATPS têm sido amplamente utilizados para a separação e recuperação de produtos biológicos como proteínas, anticorpos monoclonais, DNA, células e compostos de baixo peso, entre outros, com altas porcentagens de recuperação preservando a atividade dos bioprodutos (TORRES-ACOSTA et al, 2018). O presente estudo teve como objetivo analisar o particionamento da lactose oriunda do soro do leite, através de um sistema aquoso de duas fases, com o intuito do desenvolvimento de uma técnica alternativa barata e eficiente para o beneficiamento da molécula, de maneira sustentável, rápida e com potencial de uso industrial.
Material e métodos
Para a formação dos ATPS foram utilizados os sais de Citrato de Sódio dihidratado (C6H5Na3O7.2H2O), Fosfato de Potássio dibásico (K2HPO4), da Neon; Sulfato de Amônio ((NH4)2SO4), da Vetec; Sulfato de Sódio anidro (Na2SO4) e Carbonato de Sódio anidro (Na2CO3), da Synth; e Fosfato de Potássio tribásico (K3PO4), da Dinâmica. Polietilenoglicol de diferentes massas molares, sendo o de 300 g.mol-1 (PEG300) proveniente da Dinâmica, 400 g.mol-1 (PEG400) da Synth, 600 g.mol-1 (PEG600) e 1000 g.mol-1 (PEG1000) da Sigma Aldrich. O soro do leite foi obtido de um produtor da cidade de Nossa Senhora da Glória, Sergipe, e utilizado sem nenhum pré-tratamento. O experimento ocorreu a 25°C e 1 atm. Os sistemas foram montados com uma massa total de 10 gramas, distribuídos em 60% de soro de leite, 20% de PEG e 20% de sal, misturados em tubo centrífuga tipo falcon de 15mL. Após, houve a homogeneização utilizando um agitador de tubos Phoenix Ap-56 por 2 minutos; consequentemente os sistemas foram centrifugados por 20 minutos a 2000 rpm em uma CentriBio 80-2B para acelerar e completar a separação das fases. As fases foram separadas, pesadas e analisadas quanto a presença de lactose em açucares redutores utilizando a metodologia oficial do Ministério da Agricultura, Pecuária e Abastecimento (MAPA, 2014; LANE-EYNON, 1923). O soro do leite in natura também foi analisado segundo esta metodologia. Cada sistema foi analisado em duplicata e cada fase de cada sistema foi analisada também em duplicata. O particionamento da lactose foi mensurado utilizando a eficiência de extração, de acordo com a Equação 1, onde EE indica a eficiência da extração para a fase de fundo, mLT é a massa de lactose quantificada na fase de topo, mLI é a massa quantificada na interface e mLF a massa quantificada na fase de fundo. Equação 1: EE% = [(mLF)/∑(mLT, mLI, mLF)] X 100
Resultado e discussão
Os primeiros experimentos foram realizados utilizando o PEG400 e os sais listados. A escolha do PEG400 ocorreu, pois, o mesmo já apresenta inúmeros
estudos de particionamento envolvendo matrizes reais e complexas (PEREIRA et
al, 2016; DE SOUZA et al, 2013). Estes testes ocorreram com fim de testar o
ATPS e notar se haveria particionamento da lactose. Os sistemas dividiram-se
em três fases: uma fase de topo, rica em PEG; uma interface fina, ou fase de
meio; e uma fase de fundo rica em sal. Estes primeiros experimentos
permitiram mensurar a massa, em mg, da lactose em cada fase.
Os dados iniciais mostraram que há uma maior migração da molécula alvo para
a fase de fundo dos sistemas. Com os valores encontrados, pôde-se aplicar a
Equação 1 para encontrar a eficiência de extração para a fase de fundo, pois
ela foi a fase de maior preferência da lactose em todos os sistemas
estudados, como pode-se observar na Figura 1 (Gráfico A). Para o PEG 400, o
sistema que apresentou o particionamento mais preferencial foi o formado com
carbonato de cálcio, onde dos 269,92 mg (desvio padrão de 0,40) de lactose
presentes, 246,66 mg (desvio padrão de 6,26) foi para a fase de fundo; 7,78
mg (desvio padrão de 0,87) foram para a fase de topo e 11,72 (desvio padrão
de 6,41) mg para a interface. O sistema de menor preferência da lactose para
a fase de fundo foi o constituído por fosfato de potássio dibásico, onde
270,13 mg (desvio padrão de 0,69) da molécula foram adicionados e 162,12 mg
(desvio padrão de 4,50) foram para a fase de fundo.
Os resultados iniciais mostraram-se pertinentes para a aplicação dos ATPS no
particionamento da lactose. Seguiu-se então os testes com os demais PEG’s
(300, 600 e 1000 g.mol-1). Para estas avaliações, utilizou-se
apenas os sais de citrato de sódio e sulfato de sódio pois apresentaram
melhor facilidade de preparo do sistema, maior interface, fases mais
definidas e o fato de um ser orgânico e outro inorgânico. Foram feitos os
sistemas e analisadas as fases quanto a massa da biomolécula presente em
cada. Da mesma forma que anteriormente, notou-se a preferência do
particionamento da molécula alvo para a fase de fundo. A Figura 1 (Gráfico
B) evidencia a eficiência da extração para a fase de fundo.
Todos os dados obtidos mostraram um particionamento preferencial da lactose
para a fase de fundo no sistema PEG/sal testados. Verifica-se valores que
estão entre 47,69% ± 1,62 (PEG300/Citrato de sódio) até 92,77% ± 2,69
(PEG400/Fosfato de potássio) em eficiência de extração.
Esta preferência para fase de fundo pode ser explicada, essencialmente, por
dois motivos. O soro do leite contém proteína, que particiona
prioritariamente para a fase oposta a fase rica em sal (neste estudo, a fase
de topo), decorrência do efeito salting-out advindo dos sais
utilizados (ZASLAVSKY et al, 1982; MICHEL et al, 2015). Desta forma, a fase
de topo já está congestionada de moléculas, diminuindo o potencial químico
da fase; em contrapartida, a fase de fundo está com um potencial químico
maior, facilitando a alocação da lactose. O outro motivo apontado como
determinante para a extração da lactose para a fase de fundo é que a
biomolécula tem uma solubilidade menor em soluções de PEG, migrando para a
fase rica em sal (BRITO, 2007).
De modo sustentável, este processo pode ser parte de um protocolo maior,
onde além da formação dos ATPS, pode-se fazer o reciclo dos itens formadores
e a recuperação da lactose e demais biomoléculas através de operações
unitárias especificas, conseguindo assim um maior grau de aproveitamento do
soro do leite, conforme propomos na Figura 2.
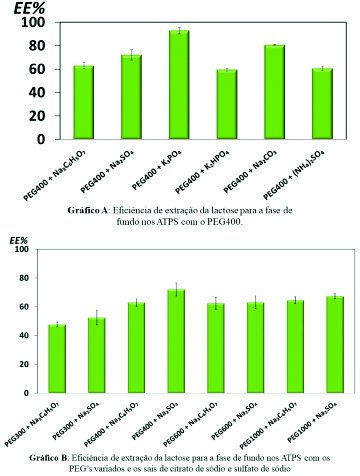
Eficiência de extração da lactose para a fase de fundo nos ATPS PEG/sal testados.
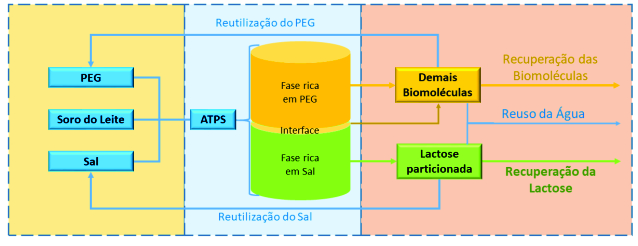
Protocolo conceitual de reuso dos itens formadores do ATPS e recuperação das biomoléculas.
Conclusões
O estudo teve como objetivo o aproveitamento da lactose advinda de um resíduo agroindustrial, o soro do leite, utilizando um sistema aquoso de duas fases composto de polietilenoglicol e sal. O particionamento preferencial da molécula para a fase de fundo dos ATPS estudados demonstra que o protocolo avaliado pode ser utilizado para este fim. O uso do sistema aquoso de duas fases para a extração neste caso foi validado através de técnica oficial do MAPA, com resultados satisfatórios e grande leque de opções, o que autentica a técnica para o caso. O protocolo mostrou-se de baixo custo, de fácil operação e com materiais com toxicidade baixa. A eficiência de extração majoritária para a fase rica em sal mostra-se promissor, com valores obtidos de até 92%. Um estudo posterior faz-se necessário para avaliar os parâmetros de aumento de escala e operações unitárias necessárias para o isolamento e cristalização da lactose.
Agradecimentos
Agradecemos a Unit/SE por o incentivo empreendido; ao Instituto de Tecnologia e Pesquisa – ITP por fornecer espaço e materiais; e à FAPITEC/SE por o apoio financeiro alocado.
Referências
ASENJO, J.A.; ANDREWS, B.A. Aqueous two-phase systems for protein separation: A perspective. Journal of Chromatography A; 1218, p. 8826-8835, 2011.
BENAVIDES, J.; AGUILAR, O.; LAPIZCO-ENCINAS, B.; RITO-PALOMARES, M. Extraction and Purification of Bioproducts and Nanoparticles using Aqueous Two-Phase Systems Strategies. Chem. Eng. Technol, v. 31, n. 6, p. 838–845, 2008.
BRITO, A. B. N. Estudo da cristalização da lactose em diferentes solventes. 2007. 152f. Tese (Doutorado em Engenharia Química). Universidade Federal de São Carlos, Centro de Ciências Exatas e Tecnologia, Programa de Pós-Graduação em Engenharia Química, São Carlos, 2007.
COLOGNESI, G. O.; et. al. Produção de etanol em concentrado de soro de queijo por Saccharomyces fragilis. Anais do Simpósio sobre Inovação da Indústria de Lácteos: 23 – 24 de maio de 2013. ITAL, Campinas, 2013.
DE SOUZA, E. C.; DINIZ, R. S.; COIMBRA, J. S. R.; LEITE, M. O.; SANTOS, G. R.; RODRIGUES, A. M. C.; SILVA, L. H. M. Measurements and Modeling of Liquid–Liquid Equilibrium of Polyethylene Glycol 400, Sodium Phosphate, or Sodium Citrate Aqueous Two-Phase Systems at (298.2, 308.2, and 318.2) K. J. Chem. Eng. Data. 58, 2008–2017, 2013.
EMBRAPA. Anuário leite 2019: Novos produtos e novas estratégias da cadeia do leite para ganhar competitividade e conquistar os clientes finais. São Paulo, 104p, 2019.
GONZÁLEZ SISO, M. I. The biotechnological utilization of cheese whey: a review. Great Britain: Published by Elsevier Science Limited. 1996.
HUDDLESTON, J. G.; WILLAUER, H. D.; BOAZ, K. R.; ROGERS, R. D. J. Chromatogr. B 711, 237, 1998.
LANE, J. H., EYNON, L. Journal of Society of Chemical Industry, 42, 32T, 1923.
MICHEL, B.; NEVES, M. T.; SOUSA, R. C. S. D.; CHAGAS, M. M. D.; MARTINS, B. A.; COIMBRA, J. S. R. Partição de proteínas de soro de leite em sistemas aquosos de duas fasess baseados em líquidos iônicos. Química Nova, 38, 1148-1152, 2015.
MINISTÉRIO DA AGRICULTURA, PECUÁRIA E ABASTECIMENTO – MAPA. Determinação de açúcares redutores em lactose, açúcares não redutores em sacarose e amido em produtos lácteos por oxidimetria. MET POA SLAV 33 02, de 01 de abril de 2014. Disponível em: <http://www.agricultura.gov.br/assuntos/laboratorios/legislacoes-e-metodos/arquivos-metodos-da-area-poa-iqa/met-poa-slav-33-02-determinacao-de-acucares-redutores-e-nao-redutores.pdf/view>. Acesso em: 02 de maio de 2019.
PELEGRINI, D.H.G.; CARRASQUEIRA, R.L. Aproveitamento do soro do leite no enriquecimento nutricional de bebidas. Brazylian Journal Food Technology, v.62, n.6, p.1004-11, 2008.
PEREIRA, M. M.; CRUZ, R. A. P.; ALMEIDA, M. R.; LIMA, Á. S.; COUTINHO, J. A. P.; FREIRE, M. G. Single step purification of ovalbumin from egg white using aqueous biphasic systems. Process Biochem. 51 (6), 781–791, 2016.
PRAZERES, A. R.; CARVALHO, F; RIVAS, J. Cheese whey management: A review. Journal of Environmental Management, v. 110, 48-68, 2012.
ROGERS, R. D.; BOND, A. H.; BAUER, C. B.; ZHANG, J.; GRIFFIN, S. T. J. Chromatogr. B 680, 221, 1996.
TORRES-ACOSTA, M. A.; MAYOLO-DELOISA, K.; GONZALEZ-VALDEZ, J.; RITO-PALOMARES, M. Aqueous two-phase systems at large scale: challenges and opportunities, Biotechnol. J., 14, 2018.
TRINDADE, I. P.; DIOGO, M. M.; PRAZERES, D. M. F.; MARCOS, J. C. J. Chromatogr., 1082, 176, 2005.
VENTURA, S.P.M.; e SILVA, F.A.; QUENTAL, M.V.; MONDAL, D.; FREIRE, M.G.; & COUTINHO, J.A.P. Ionic-Liquid-Mediated Extraction and Separation Processes for Bioactive Compounds: Past, Present, and Future Trends. Chemical Reviews, 117(10), 6984–7052, 2017.
ZASLAVSKY, B. Y.; MIHEEVA, V.; MESTECKINA, N. M.; ROGOZHIN, S. V. J. Chromatogr., 253, 149, 1982.









