Influência do 2-acetilfurano nas alterações estruturais da albumina sérica bovina e transferrina humana
ISBN 978-85-85905-25-5
Área
Bioquímica e Biotecnologia
Autores
Meira Menezes, T. (UFPE) ; Rodrigues de Barros, M.J. (UFPE) ; de Sá Pires Ferreira, D. (UFPE) ; Tavares Ventura, G. (UFRJ) ; Luiz Princival, J. (UFPE) ; Luiz Neves, J. (UFPE)
Resumo
Devido à grande ocorrência da formação do 2-acetilfurano em processos térmicos alimentícios envolvendo açúcares e proteínas, e diante do fato do potencial carcinogênico da classe de compostos dos furanos, este trabalho relata o estudo de interação entre o 2-acetilfurano e as proteínas BSA e a hTF, com o objetivo de constatar os tipos de ligação de tais proteínas quando em contato com o composto em questão.Para tanto, foram realizadas titulações utilizando o 1H RMN e a espectroscopia de fluorescência onde se determinaram parâmetros de interação. Os resultados mostram interações moderadas, fato que pode indicar relevante distribuição deste composto quando integrado no organismo humano, além de afetar a funcionalidade natural das proteínas.
Palavras chaves
2-acetilfurano; interação; proteínas
Introdução
O 2-acetilfurano constitui-se como um agente saborizador e aromatizador em alimentos, com ampla presença natural em cafés e pães (LEE, S. J. et al, 2017; POINOT, P. et al, 2008). Este tipo de composto é originado a partir de uma série de reações chamadas de reações de Maillard, caracterizada pela condensação de um carboidrato redutor e uma amina. Ao final da sequência de reações, ocorre a degradação dos açúcares redutores isoladamente, ou dos aminoácidos glicados, responsáveis por conferir sabor e aroma a determinados alimentos (WANG, Y. et al, 2009). Estes tipos de reações ocorrem com maior freqüência em alimentos que passam por processos térmicos, dando aspecto caramelizado nos mesmos (PURLIS, E., 2010). Entretanto, foi determinado por pesquisadores o efeito dos furanos na indução ao câncer em roedores (BURKA, L. T. et al, 1991). Segundo JESTOI et al (2009), os furanos propiciam a carcinogênese através da ligação do furano com genes específicos, produzindo um metabólito que se liga irreversivelmente a proteínas e nucleosídeos no organismo. Considerando que a albumina sérica e a transferrina humana são as mais presentes proteínas constituintes do sangue, este trabalho teve o objetivo de realizar o estudo de interação entre o 2-acetilfurano e as proteínas BSA (albumina sérica bovina) e a hTF (transferrina humana) para que seja possível constatar os tipos de interações de tais proteínas quando em contato com o composto em questão.
Material e métodos
A BSA, a hTF e o 2-acetilfurano foram adquiridos da sigma-aldrich e utilizados sem purificação prévia. Foram preparadas soluções das proteínas em tampão fosfato (0,01 M - pH 7,4) na concentração de 5 μM. Para a análise por 1H NMR, foi preparada uma solução de 1000 µL na concentração de 45 mM do composto em acetona deuterada e titulou-se nela as soluções tamponadas das proteínas em concentrações que vão de 0 a 42 µM. O estudo de fluorescência foi realizado em três temperaturas (293 K, 298 K, 303 K) titulando-se o composto em concentrações de 0 a 53,6 μM numa solução a 5 μM de proteína. A partir disso, os espectros foram processados e calcularam-se a constante de stern-volmer (KSV), a constante de associação (Ka), o número de sítios ligantes (n) e os parâmetros termodinâmicos das interações (ΔH, ΔS e ΔG).
Resultado e discussão
Os estudos de fluorescência indicam que a constante de stern-volmer diminuiu
com o aumento da temperatura, demonstrando mecanismo de supressão estático
para interações com as duas proteínas e o 2-acetilfurano, indicando a
formação de um complexo entre o composto e a proteína. As constantes de
associação (Ka) resultaram de moderada a forte interação na ordem
de 105 M-1 para a hTF e a BSA e o número de sítios
ligantes apresentou valor próximo de 1, indicando proporção proteína:ligante
de 1:1. Em relação aos parâmetros termodinâmicos, verificou-se que tais
interações são regidas por interações eletrostáticas, tendo em vista que o
ΔH calculado apresentou valor próximo de zero e ΔS positivo . O estudo de
NMR foi realizado com o intuito de determinar quais hidrogênios do 2-
acetilfurano são capazes de interagir significativamente com a BSA e a hTF
através da análise das mudanças no deslocamento químico do1H ao
longo da titulação. A estrutura do 2-acetilfurano e os hidrogênios
correspondentes às interações são dados na figura 1. A diferença entre o
deslocamento final e inicial (Δδ) foi calculada, onde notou-se que H2 foi o
hidrogênio mais atuante nas interações com a BSA, com deslocamento em
direção ao campo baixo e Δδ = 17,79 Hz, significando que H2 quando em
contato com a BSA interage em sua maior parcela com átomos mais
eletronegativos,ocasionando tal desblindagem observada no1H NMR.
Em segundo, o H1 apresentou Δδ = 9,74 e por fim, os hidrogênios que menos
interagem com a proteína são H3 e H4, contribuindo equivalentemente com Δδ
de 8,3 Hz. H1, H3 e H4 apresentaram deslocamento para a direção ao campo
alto (blindagem),sugerindo o contatos desses hidrogênios com átomos doadores
de elétrons.
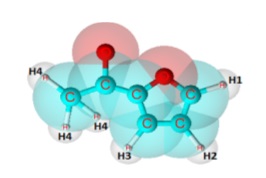
Estrutura Química do 2-acetilfurano
Conclusões
A partir dos resultados obtidos conclui-se que as interações entre o 2- acetilfurano e a BSA e hTF apresentaram intensa força de ligação, sendo assim pode-se inferir que tais interações podem alterar a funcionalidade das presentes proteínas.
Agradecimentos
Os autores agradecem a UFPE e a UFRJ.
Referências
BURKA, Leo T.; WASHBURN, Kelly D.; IRWIN, Richard D. Disposition of [14C] furan in the male F344 rat. Journal of Toxicology and Environmental Health, Part A Current Issues, v. 34, n. 2, p. 245-257, 1991.
JESTOI, Marika et al. Furan in the baby-food samples purchased from the Finnish markets–Determination with SPME–GC–MS. Food Chemistry, v. 117, n. 3, p. 522-528, 2009.
LEE, Su Jeong; KIM, Mina K.; LEE, Kwang-Geun. Effect of reversed coffee grinding and roasting process on physicochemical properties including volatile compound profiles. Innovative food science & emerging technologies, v. 44, p. 97-102, 2017.
POINOT, Pauline et al. Influence of formulation and process on the aromatic profile and physical characteristics of bread. Journal of Cereal Science, v. 48, n. 3, p. 686-697, 2008.
PURLIS, Emmanuel. Browning development in bakery products–A review. Journal of Food Engineering, v. 99, n. 3, p. 239-249, 2010.
WANG, Yu et al. Amino acid-dependent formation pathways of 2-acetylfuran and 2, 5-dimethyl-4-hydroxy-3 [2H]-furanone in the Maillard reaction. Food chemistry, v. 115, n. 1, p. 233-237, 2009.









