Isomerização da glicose empregando catalisadores baseados em Sn(IV) e Mo(VI)
ISBN 978-85-85905-25-5
Área
Química Inorgânica
Autores
Patricia Santos da Silva, E. (UFAL) ; Veríssimo dos Santos, T. (UFAL) ; Margareti Plentz Meneghetti, S. (UFAL)
Resumo
A isomerização da glicose em meio aquoso foi estudada utilizando catalisadores baseados em Sn(IV) e Mo(VI) comparativamente ao organometálico DBTO e reações sem catalisador. Avaliou-se as atividades catalíticas em termos de conversão e rendimento à frutose nas temperaturas de 50ºC e 70ºC com tempos de reação de 0,25 à 6h. Os catalisadores foram caracterizados por FTIR, TG/DTA e DRX. Os resultados demonstram que o fator principal que influencia a conversão da glicose são os sítios ácidos presentes nos catalisadores, já reportados na literatura. Pode-se constatar que o MoO3 e o SnO2/MoO3 conduziram a maiores conversões, mas o MoO3 apresentou melhores resultados em termos de rendimento à frutose. Foram identificados e quantificados também produtos como gliceraldeído e piruvaldeído.
Palavras chaves
Isomerização; Glicose; Catálise
Introdução
A partir da primeira crise do petróleo na década de 1970, foi incentivada a busca por fontes renováveis na tentativa de substituir ou complementar o uso dos combustíveis fósseis. Descobriu-se então que a biomassa é uma promissora alternativa para reduzir nossa dependência em relação ao petróleo, o gás natural e o carvão. O crescente interesse para convertê-la em insumos químicos de maneira sustentável, direciona atenção para o material lignocelulósico, rico em carboidratos, sendo esses, importantes blocos de construção para síntese de inúmeros produtos de interesse industrial e de alto valor agregado, por diversas rotas catalíticas (LI et al., 2017a; RAI et al., 2013). Dentre essas rotas, a isomerização da glicose à frutose é uma reação importante dentro do escopo das biorrefinarias (MOLINER, 2014), pois a partir da frutose, furfurais e ácidos orgânicos podem ser sintetizados, tornando a plataforma química versátil, aumentando o portfólio das moléculas intermediárias que por sua vez são convertidos em biocombustivéis, solventes, fármacos e polímeros que são úteis para a sociedade e biodegradáveis, ou seja, ambientalmente amigáveis (LI et al., 2017b; LIU et al., 2014). A glicose, devido sua abundância e da forma sustentável de sua obtenção, é preferida para a produção de hidroximetilfurfural (HMF), mas a cinética de transformação da glicose é menor do que a frutose, assim como a seletividade ao HMF é maior a partir da frutose (CLIMENT et al., 2014). Logo, a formação do HMF é facilitada com a obtenção da frutose porque a sua desidratação leva diretamente ao HMF (ROSATELLA et al., 2011). Deste modo, uma estratégia eficiente de conversão da glicose ao HMF se baseia na isomerização da glicose à frutose seguida pela desidratação desta ao HMF. Porém a indústria química é ainda hoje dependente dos recursos fósseis mas, uma perspectiva de longo prazo prevê que a biomassa se torne uma fonte de carbono para fabricação de insumos químicos, biocombustiveis e energia (LI et al., 2017b), com maior tendência de crescimento, atuando na diversificação da matriz energética mundial e na produção de novos materiais “verdes” que venham substituir os derivados petroquímicos (GALLEZOT, 2012). Vale salientar também que as fontes fósseis são esgotáveis e que a busca por fontes verdes estimula a pesquisa científica, o desenvolvimento rural, agrícola e regional, valoriza a biomassa como objeto de estudo e obtém incetivo econômico visto a diminuição da dependência do uso do petróleo (BOZELL; PETERSEN 2010; BOZEEL, 2008). A biomassa lignocelulósica apresenta grande potencial de exploração e valorização, especialmente para o Brasil, com enormes áreas cultiváveis e economia ativa no agronegócio. Esta fonte de carboidratos pode ser transformada em riqueza para o país se convertida em biocombustível e insumos químicos, dentro do conceito de biorrefinaria da biomassa lignocelulósica (SHUTTLEWORTH et al., 2014). Nesse contexto, a pesquisa científica tem desenvolvido catalisadores e processos tecnológicos que valorizam os princípios da Química Verde (PRADO et al., 2003; LENARDÂO et al., 2003), com destaque para os catalisadores químicos (homogêneos e heterogêneos) que são eficazes e com melhores atividades catalíticas (DELIDOVICH; PALKOVITS, 2016). Devido aos inconvenientes apresentados quando se utiliza catalisadores enzimáticos nestes tipos de reações como: baixo rendimento, alta pureza do reagente, preparo de soluções tampão para a enzima e faixa de temperatura limitada, torna os processos onerosos. Logo, como alternativa, a catálise química utiliza substâncias que apresentam faixa de temperatura operacional mais ampla, vida útil mais longa e melhores rendimentos para catalisar a isomerização da glicose (DESPAX et al., 2013; YU et al., 2012). Para isomerização da glicose são descritos na literatura vários tipos de catalisadores, tais como enzimas, bases e ácidos de Bronsted, resinas funcionalizadas com ácido sulfônico, zeólitas e óxidos metálicos (LI et al., 2017a). Sistemas catalíticos à base de estanho(IV) e molibdênio(VI) são estudados, devido as suas características ácidas e/ou básicas que podem ser interessantes na conversão da biomassa (DOS SANTOS, 2018). Neste trabalho, foi investigada a isomerização da glicose à frutose em meio aquoso utilizando duas temperaturas reacionais e empregando catalisadores baseados em Sn(IV) e Mo(VI), como óxido de molibdênio (MoO3), óxido de estanho (SnO2), o óxido misto (SnO2/MoO3) e o organometálico óxido de dibutilestanho (DBTO).
Material e métodos
O óxido de estanho foi obtido comercialmente da Sigma Aldrich com 99,9% de pureza e utilizado como fornecido. O MoO3 e o SnO2/MoO3 foram sintetizados por Dos Santos (2017). O primeiro através da calcinação a 550°C por 4h do precursor heptamolibdato de amônio ((NH4)6Mo7O24) e o segundo pelo método de impregnação por via úmida, onde foi preparado na proporção em massa SnO2:MoO3 de 75:25, correspondendo a 25% de MoO3 que foi impregnado ao SnO2. Tal catalisador SnO2/MoO3 foi designado SnMo25 segundo a porcentagem de MoO3 incorporado. Também foram utilizados, D-glicose, D- manose e D-frutose ambas da Sigma Aldrich com pureza maior que 99%. Os catalisadores foram caracterizados por espectroscopia de absorção na região do infravermelho por transformada de Fourier (FTIR), análises termogravimétricas (TG/DTA) e difração de raio-X (DRX), ambas metodologias são de Dos Santos (2018). Os espectros na região do infravermelho médio foram obtidos num espectrofotômetro de infravermelho modelo Varian 660-IR utilizando KBr como agente dispersante. Inicialmente os catalisadores e o KBr foram pesados, para a confecção das pastilhas e através delas foram submetidas à análise de FTIR. Parâmetros operacionais: faixa espectral de 400-4000 cm-1, 65 scans em modo transmitância, com resolução de 4 cm-1. Para o catalisador SnO2/MoO3, as análises termogravimétricas foram realizadas empregando um equipamento Shimadzu TGA– 50, sob atmosfera de gás N2 na faixa de temperatura de 25 a 1000°C, a uma velocidade de aquecimento de 10°C.min-1. A técnica de difração de raios-X usada na caracterização das amostras foi o método de pó. Nesse método os catalisadores pulverizados foram expostos a uma radiação monocromática. O equipamento utilizado foi da Shimadzu modelo XRD-6000 com uma fonte de radiação de CuK α com voltagem de 30 KV e corrente de 30 mA, com filtro de Ni. Os dados foram coletados na faixa de 2θ de 20º a 80º com velocidade de goniômetro de 2°/min com um passo de 0,02º. O tamanho dos cristalitos foi calculado pela equação da Lei de Bragg (d = k
Resultado e discussão
Nas análises de FTIR, para o SnO2 foram observadas
a presença de bandas em
497 cm-1 e em 662 cm-1 referentes ao estiramento da
ligação O-Sn-O e Sn-O,
respectivamente (ZHANGA et al., 2011; SAGADEVAN,
2015).
No caso do MoO3 foram observadas bandas em 481 cm-1
e 632 cm-1 que
representam estiramento das ligações O-Mo. Já as
absorções em 880 cm-1 e 819
cm-1 correspondem ao estiramento da ligação Mo-O-Mo
e em 993 cm-1 indica
estiramento da ligação Mo=O, dos polimolibdatos
(ALMEIDA et al., 2014; DOS
SANTOS, 2017). Os sinais de vibração do SnMo25
indicam que estão associadas
também ao estiramento das ligações Mo-O-Sn ou Mo-O-
Mo presente no MoO3,
porém os resultados de FTIR não distinguem essas
coordenações (ALMEIDA et
al., 2014; MALLESHAM et al., 2013; DATURI et al.,
2002).
O DBTO apresentou as seguintes bandas de vibrações
vibração: atribuídas em:
CH3 2960 cm-1; CH2 2930 cm-1; CH3 2870 cm-1; CH2
2853 cm-1; C-C 1594 cm-1;
δs CH2 1466 cm-1; δs CH3 1377 cm-1; C-O 1069 cm-1;
C-O 911 cm-1; ρas CH2 719
cm-1; O-Sn-O 553 cm-1. O DBTO apresenta duas
cadeias alquílicas coordenadas
ao Sn e suas bandas de deformação angular são
intensas (DOS SANTOS, 2015)
As análises de TG mostraram que o SnMo25 sofreu
decomposição térmica entre
780 e 850ºC referente à sublimação do MoO3 e em 900
a 940ºC houve perda de
polimolibdatos. Observou-se uma perda de 26,3%
indicando o teor de MoO3 em
SnO2/MoO3, o que concorda com a porcentagem
impregnada prevista (ALMEIDA et
al., 2014; HERSHFINKEL et al., 1994; DATURI et al.,
2002).
Os sinais de difração do SnO2: 110, 101, 200, 211,
220, 002, 310, 112, 301,
202 e 321 são relacionados aos planos da fase
tetraédrica. Observou-se que o
SnO2/MoO3 também apresenta essa fase,
característica do SnO2. Os sinais para
o sistema impregnado foram deslocados para maiores
ângulos e intensidades
quando comparados ao SnO2, que são associados à
nanoestrutura do SnO2/MoO3.
O deslocamento para ângulos menores, pode estar
relacionado à diferença de
raio iônico quando ocorre a impregnação, devido à
substituição de Sn4+
(~0.71 Å) por Mo+6 (~0.62 Å). Essa estrutura
aumenta a tensão entre as
ligações e os defeitos nos materiais. Supõe-se que
a forte interação entre
os óxidos aumenta o número de defeitos no material
e consequentemente,
indicativo da presença de sítios ativos. (MALLESHAM
et al., 2013).
Observou-se a formação da fase rútilo e α-MoO3 para
SnO2 e MoO3,
respectivamente, o que é confirmada pelos planos
cristalinos atribuídos às
linhas de reflexão: 110, 101, 201, 211, 220, 002,
310, 112, 301, 202, 321
que estão relacionados à fase rutilo do SnO2 (JCPDS
No. 41- 1445) e para o
MoO3 são observadas as linhas de reflexão: 110,
040, 021, 130, 111, 060, 200
e 002 (JCPDS No. 05-0508). Calculou-se o tamanho do
cristalito utilizando a
equação da Lei de Bragg a partir da linha de
reflexão 110. As amostras de
SnO2, MoO3 e SnMo25 apresentaram tamanho médio do
cristalito 7,1; 5,6 e 6,0
nm respectivamente.
Foi observado que o tamanho do cristalito é menor
após a impregnação com
íons Mo+6. A diminuição estaria associada à
distorção induzida pela dopagem
do íon Mo+6 na rede do SnO2, como já foi mencionado
(MALLESHAM et al.,
2013).
Avaliou-se os sistemas catalíticos a 50ºC, porém
não ocorreu a isomerização
da glicose à frutose, pois os cromotogramas obtidos
por CLAE, apresentaram
sinais pouco definidos e sobrepostos,
correspondente à frutose,
identificando apenas o início da isomerização, o
que impediu o uso dessa
temperatura para o estudo. Após esse teste, a
temperatura de 70ºC foi
escolhida e utilizada como parâmetro de condição
reacional, visto que a
literatura reporta boas conversões de glicose a
partir dessa temperatura com
diferentes sistemas catalíticos (GAILY et al.,
2010; MARIANOU et al., 2016;
CHHEDA et al., 2007; LIU et al., 2014).
Com esse aumento de temperatura, foi observada a
conversão da glicose à
frutose via isomerização através de análises no
CLAE (Figura 1). Observa-se
que as reações na ausência de catalisador e na
presença de SnO2 e DBTO,
apresentaram perfil cinético semelhantes com
valores próximos de conversões,
não ultrapassando 22%. A partir de 3h, os sistemas
apresentaram valores de
conversões constantes, comprovando que após esse
tempo o sistema entra em
equilíbrio.
O sistema misto SnMo25 mostrou maiores conversões
em relação ao SnO2 com
21,8%, DBTO com 21,3% e na ausência de catalisador
apresentando 21% ambos em
6h de reação. Isso pode ser explicado pelo aumento
da acidez de Lewis do
SnO2 com a impregnação de 25% de MoO3 (DOS SANTOS
et al., 2018). Já o DBTO
conduziu a melhores resultados quando comparado ao
SnO2. Nenhum sistema
ultrapassou os valores de conversão do MoO3 com
63%, seguido do SnMo25 com
47% ambos em 6 h de reação. Importante mencionar
que com a utilização do
SnMo25 e MoO3 foram observadas mudança de coloração
da mistura reacional,
que se tornou levemente azulada a partir de 2h de
reação. Uma explicação
para este fato, pode ser o crescimento de cristais
de polimolibdato, os
quais podem estar sendo lixiviados para o meio
reacional (MALLESHAM, 2013).
Foi verificado que a conversão da glicose também
está relacionada à
concentração de sítios ácidos nos catalisadores.
Catalisadores químicos
estão sendo muito utilizados para conversão da
biomassa em substituição aos
catalisadores enzimáticos devidos seus
incovenientes que já foram citados
neste trabalho. Mas, dentre esses catalisadores
químicos, a classe dos
heterogêneos (óxidos metálicos e óxidos mistos) tem
recebido atenção
(PARSHETTI et al., 2015).
Já é conhecido que a glicose pode se isomerizar a
frutose e epimerizar à
manose (MOLINER et al., 2010). Não foi descartada a
possibilidade da
formação de manose. Porém, análises realizadas em
CLAE dos padrões de D-
manose, D-frutose e D-glicose observou-se que a
frutose e a manose
apresentam sinais sobrepostos. Para uma separação
eficiente, seria
necessário à mudança de diversos parâmetros
relacionados à análise, com
combinações apropriadas (PAULI et al., 2011).
Os rendimentos de futose, na presença dos
catalisadores heterogenêos, são
apresentados na Figura 2.
Em geral, o rendimento a frutose aumentou
progressivamente com a evolução do
tempo reacional. Com o emprego do sistema SnO2 foi
obtido um máximo de 6,8%
de rendimento a frutose em 4h. Com os sistemas MoO3
e SnMo25 foi obtido
rendimento máximo de 24% em 3h e 24,7% em 6h,
respectivamente. As reações
com sistema homogêneo DBTO e sem catalisador não
exibiram isomerização de
glicose à frutose, portanto para esses casos não
foram realizados cálculos
de rendimento referentes a frutose.
Comparando valores de rendimento com seus valores
máximos de conversão da
glicose foi notado uma discrepância no balanço de
massa. Esse fenômeno pode
ser explicado pela formação de produtos insolúveis
e indesejados (materiais
poliméricos como huminas e oligômeros) nesse tipo
de reação, pela rota de
decomposição do hidroximetilfurfural (HMF),
reidratação da glicose, seguida
da polimerização da frutose. Tais produtos não são
identificados por CLAE,
pois ficam retidos nos filtros. Os produtos
insolúveis se tornam
indesejáveis porque há consumo de substrato e menor
rendimento ao produto
desejado, nesse caso a frutose. Sabe-se que longos
tempos de reação ou mesmo
a natureza do catalisador, pode levar à formação de
tais produtos em
diferentes quantidades (DOS SANTOS et al., 2018;
DOS SANTOS et al., 2015).
Também pode ocorrer formação de outros produtos
como o gliceraldeído e o
piruvaldeído, dos quais foram detectados na
conversão da glicose nas
condições reacionais empregadas, com rendimentos
máximos que variaram entre
0,1 e 3%. Esses compostos são formados por outras
vias mecanísticas como as
reações retro aldólicas (DOS SANTOS et al., 2015;
AIDA et al., 2007).
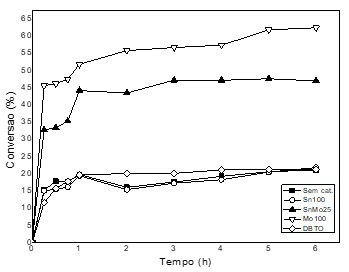
Conversões da glicose a 70 ºC na presença dos sistemas catalíticos SnO2, MoO3, SnMo25, DBTO e na ausência do catalisador
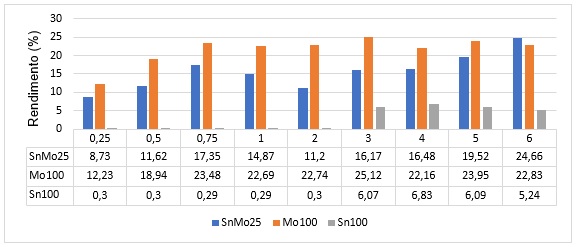
Efeito do tempo de reação no rendimento de frutose na isomerização de D-glicose em D- frutose empregando os sistemas catalíticos SnO2, MoO3 e SnMo25.
Conclusões
As técnicas de caracterizações contribuíram para um estudo detalhado dos materiais. Foi observada a isomerização a frutose para os sistemas SnO2, MoO3 e SnO2/MoO3 (SnMo25). O SnO2 promoveu rendimentos satisfatórios para frutose. Para o MoO3 e SnMo25 foi observado maiores conversões e rendimentos. Por outro lado, com o emprego do DBTO e para as reações sem catalisador não foi observada a isomerização à frutose. Além disso, produtos minoritários como gliceraldeído e piruvaldeído também foram identificados e quantificados. Os valores de rendimento à frutose podem ter sido afetados devido à produção de compostos insolúveis (oligômeros ou huminas) e possivelmente a ocorrência da epimerização da glicose à manose.
Agradecimentos
Agradecimentos ao Grupo de Catálise e Reatividade Química (GCaR-IQB-UFAL), em especial aos professores Mário Meneghetti e Simoni Meneghetti e a mestre Tathiane Veríssimo.
Referências
AIDA, T. M.; TAJIMA, K.; WATANABE, M., et al. Reactions of d-fructose in water at temperatures up to 400 ◦C and pressures up to 100 MPa. J. of Supercritical Fluids, 42, p. 110–119, 2007.
ALMEIDA, R. M.; SOUZA, F. T. C.; JÚNIOR, M. A. C.; ALBUQUERQUE, N. J. A.; MENEGHETTI, S. M. P.; MENEGHETTI, M. R.; Improvements in acidity for TiO2 and SnO2 via impregnation with MoO3 for the esterification of fatty acids, Catalysis Communications, 46, p. 179–182, 2014.
BOZELL, J. J.; Feedstocks for the Future - Biorefinery Production of Chemicals from Renewable Carbon. Clean - Soil, Air, Water, 36, 8, p. 641–647, 2008.
BOZELL, J. J.; PETERSEN, G. R.; Technology development for the production of biobased products from biorefinery carbohydrates—the US Department of Energy’s “Top 10” revisited. Green Chem., 12, 4, p. 539-554, 2010.
CHHEDA, J.; HUBER, G. W.; DUMESIC. J. A.; Liquid-Phase Catalytic Processing of Biomass-Derived Oxygenated Hydrocarbons to Fuels and Chemicals. Angew. Chem. Int. Ed., 46, p. 7164 –7183, 2007.
CLIMENT, M. J.; CORMA, A.; IBORRA, S. Conversion of biomass platform molecules into fuel additives and liquid hydrocarbon fuels. Green Chem., 16, p. 516– 547, 2014.
DATURI, M.; APPEL, G. L.; Infrared Spectroscopic Studies of Surface Properties of Mo/SnO2 Catalyst. Journal of Catalysis, 209, 427 – 432, 2002.
DELIDOVICH, I.; PALKOVITS, R.; Catalytic isomerization of biomass-derived aldoses: A review. ChemSusChem, 9, p. 547 – 561, 2016.
DESPAX, S.; ESTRINE, B.; HOFFMANN, N.; BRAS, J. L.; MARINKOVIC, S.; MUZART, J.; Isomerization of D-glucose into D-fructose with a heterogeneous catalyst in organic solvents. Catalysis Communications, 39, p. 35–38, 2013.
DOS SANTOS, J. B.; DE ALBUQUERQUE, N. J. A.; ZANTA, C. L. P. S.; MENEGHETTI, M. R.; MENEGHETTI, S. P.; Fructose conversion in the presence of Sn(iv) catalysts exhibiting high selectivity to lactic acid. RSC Adv., 5, p. 90952-90959, 2015.
DOS SANTOS, J. B.; Conversão catalítica de frutose e glicose em presença de catalisadores de Sn(IV), 2015. Tese (Doutorado em Química Inorgânica e Catálise), Universidade Federal de Alagoas, Maceió, AL, 2015.
DOS SANTOS, T. V.; Avaliação dos catalisadores SnO2, MoO3 e SnO2/MoO3 na conversão da frutose, 2017. Dissertação (Mestrado em Ciências), Universidade Federal de Alagoas, Maceió, AL, 2017.
DOS SANTOS, T. V.; AVELINO, D. O. da S.; MENEGHETTI, M. R.; MENEGHETTI, S. M. P.; Mixed oxides based on SnO2 impregnated with MoO3 A robust system to apply in fructose conversion. Catalysis Communications, 114, p. 120-123, 2018.
GAILY, M. H.; ELHASSAN, B. M.; ABASAEED, A. E.; AL-SHRHAN, M. Isomerization and kinetics of glucose into fructose. International Journal of Engineering & Technology v. 10, n. 3, p. 1-6, 2010.
GALLEZOT, P.; Conversion of biomass to selected chemical products, Chem. Soc. Rev., 41, p. 1538–1558, 2012.
HERSHFINKEL, M.; GHEBER, L. A.; VOLTERRA, V. ; Hutchison, J. L.;Margulis, L.; Tenne, R., Nested Polyhedra of MX2 (M = W, Mo; X = S, Se) Probed by High-Resolution Electron Microscopy and Scanning Tunneling Microscopy, J. Am. Chem. Soc., 116 , 1914–1917, 1994.
LENARDÃO, E. J.; FREITAG, R. A.; DABDOUB, M. J.; BATISTA, A. C.; SILVEIRA, C. C. “Green chemistry” – Os 12 princípios da química verde e sua inserção nas atividades de ensino e pesquisa. Quim. Nova, 26, 1, p. 123-129, 2003.
LI, H.; YANG, S.; SARAVANAMURUGAN, S.; RIISAGER, A.; Glucose isomerization by enzymes and chemo-catalysts: status and current advances, ACS Catal., 7, 4, p. 3010-3029, 2017.
LI, S.; JOSEPHSON, T.; VLACHOS, D. G.; CARATZOULAS, S.; The origin of selectivity in the conversion of glucose to fructose and mannose in Sn-BEA and Na-exchanged Sn-BEA zeolites. Journal of Catalysis, 355, p. 11-16, 2017.
LIU, C.; CARRAHER, J. M.; SWEDBERG, J. L.; HERNDON, C. R.; FLEITMAN, C. N.; TESSONNIER, J. P.; Selective Base-Catalyzed Isomerization of Glucose to Fructose, ACS Catal., 4, p. 4295−4298, 2014.
MALLESHAM, B.; SUDARSANAM, P.; RAJU, B.; REDDY, B. M.; Design of highly efficient Mo and W-promoted SnO2 solid acids for heterogeneous catalysis: acetalization of bio-glycerol, Green Chem., 15, p. 478-490, 2013.
MARIANOU, A. A.; MICHAILOF, C. M.; PINEDA, A.; ILIOPOULOU, E. F.; TRIANTAFYLLIDIS, K. S.; LAPPAS, A. A.; Glucose to fructose isomerization in aqueous media over homogeneous and heterogeneous catalysts. ChemCatChem, 8, p. 1100 – 1110, 2016.
MOLINER, M.; State of the art of Lewis acid-containing zeolites: lessons from fine chemistry to new biomass transformation processes, Dalton Trans., 43, p. 4197-4208, 2014.
PARSHETTI, G. K.; SURYADHARMA, M. S.; PHAM, T. P. T.; MAHMOOD, R.; BALASUBRAMANIAN, R., Heterogeneous catalyst-assisted thermochemical conversion of food waste biomass into 5-hydroxymethylfurfural. Bioresource Technology, 178, p. 19–27, 2015.
PAULI, E. D.; CRISTIANO, V.; NIXDORF, S. L.; Método para determinação de carboidratos empregado na triagem de adulterações em café, Quim. Nova, 34, 4, p. 689-694, 2011.
PRADO, A. G. S., Química verde, os desafios da química do novo milênio, Quim. Nova, 2003, 26, p. 738-744.
RAI, N.; CARATZOULAS, S.; VLACHOS, D. G.; Role of Silanol Group in Sn-Beta Zeolite for Glucose Isomerization and Epimerization Reactions, ACS Catal., 3, 10, p. 2294–2298, 2013.
ROSATELLA, Andreia A.; SIMEONOV, Svilen P.; FRADE, Raquel F. M.; AFONSO, Carlos A. M. 5-Hydroxymethylfurfural (HMF) as a building block platform: Biological properties, synthesis and synthetic applications. Green Chem., 13, p. 754–793, 2011.
SAGADEVAN, S.; PODDER, J. Optical and Electrical Properties of Nanocrystalline SnO2 Thin Films Synthesized by Chemical Bath Deposition Method. Soft Nanoscience Letters, 5, 55-64, 2015.
SHUTTLEWORTH, P. S.; DE BRUYN, M.; PARKER, H. L.; HUNT, A. J.; BUDARIN, V. L.; MATHARU, A. S.; CLARK, J. H. Applications of nanoparticles in biomass conversion to chemicals and fuels. Green Chem., vol. 16, p. 573–584, 2014
YU, S.; KIM, E.; PARK, S.; SONG, I. K.; JUNG, J. C.; Isomerization of glucose into fructose over Mg–Al hydrotalcite catalysts, Catalysis Communications, 29, p. 63–67, 2012.
ZHANGA, B.; TIANB, B, Y.; ZHANGA, J.X.; CAIA, W. The FTIR studies of SnO2:Sb(ATO) films deposited by spray pyrolysis. Materials Letters, 65, 1204–1206, 2011.









