ESTUDO ESPETROFOTOMÉTRICO DE INTERAÇÃO DO COMPOSTO BENZO(A)ANTRACENO-7,12 DIONA 7-OXIMA COM dsDNA CALF THYMUS
ISBN 978-85-85905-25-5
Área
Química Analítica
Autores
Sousa, D.B.P. (UFMA) ; Marques, P.R.B.O. (UFMA) ; Nunes, G.S. (UFMA) ; Carvalho Neta, R.N.F. (UEMA)
Resumo
O DNA é uma biomacromolécula que oferece diversos sítios de ligação para uma variedade de outras moléculas. Estas ligações podem acarretar mudanças na estrutura do DNA e em suas funções.A determinação de como esta ligação entre o intercalador e o DNA está efetuada constitui uma ferramenta de avaliação qualitativa e quantitativa deste processo de associação. A espectrofotometria UV-Vis tem por princípio a interação da luz com a matéria, uma vez definidos os espectros característicos para compostos de interesse, alterações nesses espectros podem evidenciar alterações na estrutura dos mesmos, o que pode evidenciar formação de complexos. O presente trabalho estudou a interação entre DNA Calf thymus e o benzo(a)antraceno-7,12 diona 7-oxima por técnica de espectrofotometria UV- Vis
Palavras chaves
HPA; Espectrofotometria UV-VI; DNA Calf Thymus
Introdução
O DNA é uma biomacromolécula que oferece diversos sítios de ligação para uma variedade de outras moléculas. Estas ligações podem acarretar mudanças na estrutura do DNA e em suas funções. Existem três tipos básicos de processos de interação de moléculas/íons com o DNA: interação eletrostática, ligação com sulcos e intercalação. Os três processos podem ser observados ao mesmo tempo. As moléculas grandes possuem preferência pelos sulcos maiores do DNA, sendo os sulcos menores, bem como os espaços planares disponíveis entre a dupla hélice, preferidos pelos ligantes pequenos [IHMELS, H., OTTO D., 2005].O processo de intercalação envolve uma pequena mudança de conformação na molécula de DNA, desenrolando e/ou alongando a mesma, podendo resultar em mudança na estrutura das moléculas de ribose, entre os carbonos C2' e C3', que pode aumentar os espaços entre os fosfatos e diminuir a densidade de carga ao longo da dupla hélice. A intercalação de uma molécula pequena impede que este processo ocorra novamente com outra molécula, por razões estéricas, ou mesmo pela redução do potencial eletrostático no sítio de intercalação. O processo de intercalação, com relação às pontes de hidrogênio entre as bases, pode ocorrer de modo axial, paralelo ou perpendicular.A determinação de como esta ligação entre o intercalador e o DNA está efetuada constitui uma ferramenta de avaliação qualitativa e quantitativa deste processo de associação. A variações nas propriedades de absorção e emissão de luz podem auxiliar na elucidação destes processos (MARTINEZ, 2005; PIVIDORI, 2002; IHMELS; OTTO, 2005).
Material e métodos
Foi utilizado o DNA Calf Thymus, obtido da Sigma-Aldrich. O material foi pesado diretamente em tubo eppendorf, e diluído com EDTA 1 mmolL. As soluções de tampão fosfato (pH 7,2) foram preparadas em água deionizada e armazenadas em geladeira,a 4 ºC. O benzo(a)antraceno-7,12 diona 7-oxima foi SIGMA. As medidas espectrofotométricas foram efetuadas em um espectrofotômetro UV/Vis (Thermoscientific, Orion AquaMate 8000) com cubeta de quartzo de 1 cm de caminho óptico. Inicialmente foi efetuada uma caracterização dos compostos em estudo, seguida dos estudos de interação.O estudo inicial da interação entre o DNA e composto HPA foi realizado com soluções de concentração fixa de DNA (26 μg/ml), variando-se a concentração dos BZA em uma faixa específica. Inicialmente mediu-se a absorção da solução de DNA livre, em seguida adicionou-se o BZA e fez-se nova medida de absorção da solução mista, observando as mudanças no sinal analítico obtido. O BZA foi dissolvido em acetonitrila e diluído em tampão fosfato, em ultrassom. Posteriormente foi efetuada a análise do sinal analítico do BZA. Para avaliação da relação estequiométrica entre DNA e o composto HPA foi utilizado o método da variação contínua.
Resultado e discussão
O aumento da concentração de DNA apresentou uma ótima relação linear para
com o aumento da absorbância no sistema, tendo como equação da reta:
Abs=0,0062 + 0,0111[DNA/μg/mL], com R=0,998. A razão 260/280 nm
foi de 1,85, o que indica que o DNA livre de proteínas. Para o BZA foram
observadas duas regiões de absorção (264 e 430 nm). Foi então efetuada a
variação de sinal analítica em função da concentração do analito, que
apresentaram relação de linearidade nos dois comprimentos de onda.O estudo
de interação DNA/BZA foi efetuado fixando a concentração de DNA e variando
a de BZA. Observou-se uma oscilação de sinal na região de 258 nm, tendo um
efeito hipocrômico até próximo do ponto equimolar e em seguida um efeito
hipercrômico, até o dobro da concentração equimolar e seguinte queda. Estes
efeitos podem evidenciar ligações e interações entre os dois compostos em
estudo. Posteriormente foi efetuado o método das variações contínuas, que
sugeriu a formação de um complexo de uma fração molar (DNA) próxima de 0,1,
o que pode representar uma relação 9 moléculas de BZA para cada monômero de
DNA.
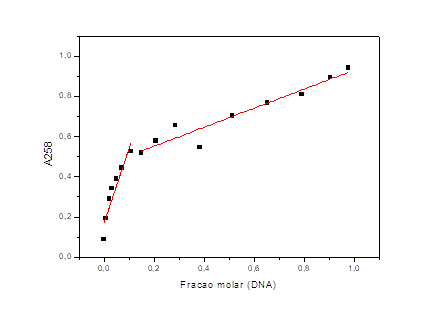
Relação de formação de complexo DNA/BZA obtido pelo método das variações contínuas. Indica a formação de um complexo 9:1
Conclusões
o DNA se apresentou com comportamento linear quando avaliado pela técnica de espectrofotometria. O composto apresentou pico característico de absorção na região de 258 nm. Foram observados efeitos hipo e hipercrômicos no sistema. O método das variações contínuas indicou a formação de um complexo 9:1, ou seja, 9 moléculas de BZA para cada monômero de DNA. Mas inda não foi possível indicar o tipo de ligação existente entre os compostos.
Agradecimentos
Referências
IHMELS, H., OTTO D. Intercalation of organic dye molecules into double-stranded DNA: general grinciples and recent developments. Top Curr Che,. 258: 161–204, 2005.
MARTÍNEZ, R., CHACON-GARCIA, L. The search of DNA-intercalators as antitumoral drugs: what it worked and what did not work. Curr. Med. Chem., 12, 127-151, 2005.
PIVIDORI, M. I. Nuevos Genosensores amperométricos: diseño y construccion. 2002, 505f. Tese (Doutorado em Ciências Químicas)-Universidade Autônoma de Barcelona, Bellaterra, 2002.









