Análise dos parâmetros físico-químicos e centesimais do fermentado alcoólico de seriguela (Spondias purpurea L.)
ISBN 978-85-85905-25-5
Área
Química Analítica
Autores
Cunha Coelho, R. (IFPI) ; Chaves, C. (IFPI) ; Silva, J. (IFPI) ; Sousa, P. (IFPI) ; Pinto, L. (IFPI)
Resumo
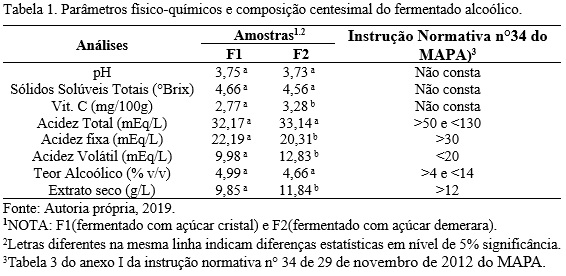
O desenvolvimento de um fermentado alcoólico de seriguela traz uma alternativa promissora evitando o desperdício de frutas durante a safra de forma a agregar valor a esta matéria-prima. O objetivo deste trabalho foi comparar os resultados das analises físico-químicas do fermentado alcoólico de seriguela produzido com açúcar cristal (F1) e outro feito com açúcar demerara (F2). Verificou-se, para as duas formulações analisadas (F1 e F2), que os valores de acidez total (32,17 e 33,14), extrato seco (9,85 e 11,84) e fixa (22,19 e 20,31) ficaram abaixo do estabelecido pela normativa n° 34 do Ministério da Agricultura, Pecuária e Abastecimento. Apenas acidez volátil (9,98 e 12,83) e teor alcoólico (4,99 e 4,66) apresentaram valores dentro do estabelecido.
Palavras chaves
Fermentado alcoólico; Spondias purpurea L; Análise físico-químicas
Introdução
A produção de fermentados alcoólicos é um dos mais antigos processos, possivelmente iniciado com a produção de vinho e cerveja há milhares de anos (VENTURINI FILHO, 2010). De acordo com a legislação brasileira, o fermentado de fruta é definido como uma bebida com graduação alcoólica que varia entre 4 a 14% em volume a (20 °C) e deve ser obtido pela fermentação alcoólica do mosto da fruta sã, fresca e madura de uma única espécie, do respectivo suco integral ou concentrado, ou polpa. O fermentado será denominado fermentado da fruta que deu origem (ex.: fermentado de laranja, fermentado de morango, entre outros). A bebida poderá ser gaseificada quando for adicionado dióxido de carbono (BRASIL, 2009). Diversas frutas têm boas características sensoriais para vinhos e, aliada à necessidade de se ampliar as suas produções e consumo em diversos países, a produção destes “vinhos” alternativos, tem sido bastante pesquisada e incentivada (SILVA et al., 2008) . Fermentados são resultado da atividade de microrganismos benéficos, classificados como produtores de alimentos, principalmente leveduras e bactérias. As leveduras têm papel fundamental na produção de variados e tradicionais produtos alimentícios fermentados no mundo inteiro (AIDOO; ROB NOUT; SARKAR, 2006). O regulamento técnico para fixação dos Padrões de Identidade e Qualidade (PIQ) para fermentado de fruta dispõe que os ingredientes utilizados na produção do fermentado de fruta são, mosto de fruta sã, fresca e madura; podendo ser usados como ingredientes opcionais água e açúcar, neste caso, exclusivamente, a sacarose. Para que o fermentado alcoólico ou vinho seja considerado de qualidade é necessário que suas características físicas e físico-químicas estejam enquadradas no preconizado pelas legislações vigentes devendo apresentar limpidez, ausência de corpos estranhos ou em suspensão, com teor alcoólico adequado e ausência de corantes e aromatizantes artificiais (BRASIL, 2008). A Seriguela (S. purpurea L.) é uma árvore frutífera tropical em exploração pelo seu valor comercial na região norte e nordeste do Brasil, tendo como período de safra os meses de dezembro a março e apresenta crescente expansão do mercado consumidor devido a suas qualidades nutritivas e organolépticas (SOARES, 2011). Os frutos, com rendimento em torno de 50% de sua polpa, além de serem consumidos in natura é amplamente utilizado na fabricação de sucos, sorvetes, licores, vinho, geléia, compotas e refrigerantes (BRITO 2010). O Processamento de frutos para obtenção de produtos gera em torno de 30 a 40% de resíduos que são constituídos por casca, caroço ou sementes e bagaço que, em muitos casos, são considerados custos operacional para as empresas ou fonte de contaminação ambiental (MARTINS, 2002; SILVA, 2013). O objetivo deste trabalho foi comparar os resultados das analises físico-químicas do fermentado alcoólico de seriguela produzido com açúcar cristal (F1) e outro feito com açúcar demerara (F2).
Material e métodos
As análises físico-químicas e composição centesimal foram realizadas no laboratório de Bromatologia do Instituto Federal de Educação Ciência e Tecnologia do Piauí - IFPI, Campus Teresina Central, em Teresina-PI. Foram realizadas análises de acordo com as recomendações do Instituto Adolfo Lutz (2008). Foram feitas acidez total (221/IV), acidez fixa (222/IV), acidez volátil (223/IV, pH (201/IV), sólidos solúveis totais (315/IV), teor alcoólico (217/IV), vitamina C (365/IV) e extrato seco (218/IV). A acidez total foi determinada utilizando o método titulométrico, onde uma alíquota da amostra foi titulada com solução de hidróxido de sódio (marca Dinâmica) 0,1 mol [L][/-1] até obter-se a coloração rósea. Para determinar a acidez fixa, primeiramente a amostra precisou ser evaporada. O produto obtido da evaporação foi titulado rapidamente com solução de hidróxido de sódio padronizada, até coloração rósea persistente por 30 segundos. A acidez volátil foi determinada pela diferença entre a acidez total e a fixa. Os resultados foram expressos, em mEq/L. As medidas de pH foram feitas através do método potenciométrico utilizando-se pHmetro de bancada da marca Hanna, previamente calibrado. O procedimento, para a medida do pH, consistirá em inserir o eletrodo do aparelho diretamente nas amostras, efetuando-se a leitura no visor do equipamento. A leitura de sólidos solúveis totais foi determinada pela leitura direta em refratômetro digital de bancada (Modelo NOS DR 500), previamente aferido com água destilada e os resultados foram expressos em ºBrix. A graduação alcoólica (% em volume) foi obtida pela tabela de conversão da densidade relativa a 20 °C/20 °C determinada no destilado alcoólico da amostra. O método consiste em ajustar a temperatura da amostra a 20 °C e medir 100 ou 250 mL. Posteriormente, realiza a destilação simples. Alternativamente, pode-se transferir a amostra para o conjunto de destilação e proceder conforme as instruções de uso do equipamento. Em seguida, recolhe-se o destilado anteriormente usado, já contendo 10 mL de água e imerso em banho de água e gelo. Destila-se cerca de ¾ do volume inicial, então deve ajustar a temperatura a 20 °C, mergulhando o balão volumétrico em banho de água e gelo, aferindo o volume com água a 20 °C em agitação. Em seguida, deve-se determinar a densidade relativa do destilado a 20 °C, com o uso de picnômetro ou densímetro digital automático ou outro aparelho como hidrômetro ou densímetro calibrado. A determinação do teor de vitamina C foi obtida por titulometria com solução de DCFI (2,6 diclocro-fenol-indofenol) a 0,02% (marca NEON) até coloração róseo-clara permanente. Os resultados foram expressos em mg de ácido ascórbico/100 g da amostra. A análise de extrato seco total foi realizada coletando 25 g da bebida em uma cápsula de porcelana. A amostra foi evaporada em banho-maria (equipamento LUCADEMA) seguida de secagem em estufa (Marca Heraeus instruments) 100±5°C por 30 min.
Resultado e discussão
Os resultados dos parâmetros físico-químicos do fermentado alcoólico
encontram-se na Tabela 1, bem como os limites estabelecidos pela Instrução
Normativa nº 34, que estabelece a complementação dos padrões de identidade e
qualidade para as bebidas alcoólicas, comercializadas em todo o território
nacional (BRASIL, 2012).
Embora a Legislação Brasileira não estabeleça limites de pH para os
fermentados de frutas, este parâmetro foi analisado nas duas formulações de
fermentados produzidos, cujos valores apresentados de pH foram de 3,75 para
F1 e 3,73 de para F1. Valores semelhantes de pH são recorrentes na
literatura, para fermentados de outras frutas: 3,51 fermentado de morango de
(ANDRADE et al., 2014), de acerola com 3,58 (SEGTOWICK et al., 2013) e 3,9
(LIMA et al., 2015) ,estes valores são mais elevado que o pH de 2,94 do
fermentado de seriguela feito por Muniz (2002). Alguns aspectos como
crescimento bacteriano, solubilidade de proteínas, efeito do dióxido de
enxofre, efetividade da bentônica e reações de escurecimento, estão
diretamente relacionados ao pH. Limites de pH entre 3 e 4 aumentam a
resistência à contaminação bacteriana (AQUARONE et al., 2001).
Quanto ao teor de açúcares remanescentes, expressos em °Brix, os fermentados
de seriguela diferiram bastante, dos fermentados de fermentados de goiaba
branca com 9,6°Brix (BATISTA, 2016) e ao de caqui com 10,0°Brix (NUNES;
TOMÉ; FRAGIORGE, 2009) e semelhante aos fermentados de caju com 3,6°Brix
(TORRES NETO et al., 2006), de jabuticaba 5,0 ºBrix (SANTOS et al., 2016).
Brandão (2013) afirma que o teor final de sólidos solúveis varia para cada
fermentado de fruta, uma vez que depende do teor inicial, da quantidade de
levedura e da temperatura do meio. Muniz (2002) ao elaborar um fermentado de
Seriguela, observou que houve aumento de 4º Brix nos primeiros dois dias,
permanecendo estável até o sétimo dia da fermentação, observando somente a
partir do sétimo dia, houve uma redução acentuada no teor de sólidos
solúveis totais, estabilizando-se em 5º Brix após 12 dias de fermentação.
Parâmetro atividade de água mostrou-se estatisticamente igual nas duas
formulações e observou-se que os diferentes tipos de açúcares não
influenciaram nessa análise já que representa a água disponível para reações
bioquímicas e/ou enzimáticas.
Os valores de vitamina C obtidos neste estudo foram de 2,77 mg de ácido
ascórbico/100 ml após a fermentação para o tratamento F1 e 3,28 para F2
sendo estes diferentes estatisticamente. Resultados superiores foram obtidos
na bebida alcoólica mista de laranja com beterraba de Gonçalves et. al.
(2016), apresentando 20 mg de ácido ascórbico/100 mL de mosto e 19,67 mg de
ácido ascórbico/100 mL de bebida após a fermentação para o tratamento T1 e
de 22 mg de ácido ascórbico/100 mL de mosto e 21,70 mg de ácido
ascórbico/100 mL de bebida após a fermentação para o tratamento T2 .
A vitamina C é considerada uma vitamina hidrossolúvel e termolábil, sendo
rapidamente oxidada quando exposta ao ar. Por esse motivo ela é usada como
índice de qualidade nutricional de produtos derivados de frutas e vegetais,
porque quando comparada a outros nutrientes, esta vitamina é mais sensível à
degradação durante o processamento e subsequente estocagem (DANIELI et al.,
2009).
A acidez total do fermentado em estudo, está abaixo do limite mínimo
determinado pela legislação brasileira para fermentados de frutas, que
estabelece limites entre 50 a 130 mEq/L (BRASIL, 2009), os valores
encontrados foram de 32,17 mEq/L para F1 e 33,14 para F2. Estes valores
foram semelhante ao de alguns fermentados, como, de cajá, 29,00 mEq/L (DIAS
et al. 2003), o de cagaita com 47,78 mEq/L (OLIVEIRA et al., 2010) e muito
inferiores ao fermentado de jabuticaba com 185,0 mEq/L (SILVA et al., 2008).
Vários fatores podem ter contribuído para o baixo valor de acidez total
encontrado no presente trabalho, como: a diluição dos ácidos presentes na
polpa de seriguela durante a diluição da mesma no preparo do mosto.
A acidez fixa encontrado no estudo foi de 22,19 mEq/L para a f1 e 20,31
para f2 valores estes que diferem significamente dos fermentados do suco e
da polpa da acerola, 130,67 mEq/L e 96,22 mEq/L (SEGTOWICK et al., 2013),
respectivamente, da goiaba branca, 55,39 mEq/L (BATISTA, 2016). A acidez
fixa é a diferença entre a acidez total e a acidez volátil, ou seja, é o
conjunto de ácidos não voláteis presentes no fermentado, como os ácidos
málico, tartárico, cítrico, láctico, succínico entre outros os ácidos
orgânicos (BATISTA, 2016).
O resultado para acidez volátil para fermentado de Seriguela foi de 9,98
para F1 e 12,83 mEq/L, F3. Estes valores estão acima aos apresentados pelo
fermentado de cajá de 5,5 mEq/L (DIAS; SCHWAN; LIMA, 2003). De acordo com
Hashizume (2001), uma alta acidez volátil é indicativa de contaminação
microbiana advinda da falta de assepsia no processo devendo ser a mais baixa
possível.
Os valores de acidez volátil dos fermentados encontram-se dentro do padrão
estabelecido pela legislação brasileira para fermentados de frutas, que
indica o valor máximo de 20 mEq/L (BRASIL, 2012).
O teor alcoólico do fermentado de Seriguela produzido foi de 4,99 v/v para
F1 e de 48,7 v/v para F2, ficando com teor alcoólico abaixo ao da bebida
alcoólica de Seriguela feita por Muniz et. al (2002) que apresentou teor
alcoólico 10,0 v/v, assim como também do fermentado de abacaxi com 12,3% v/v
(OLIVEIRA et al., 2012).
Considerando a Legislação Brasileira que trata de fermentados de fruta
estabelece limite de teor alcoólico na faixa de 4 a 14% º GL, o mesmo
apresentou-se de acordo com a faixa proposta por esta Legislação (BRASIL,
2010). O teor alcoólico, aliado ao pH e a acidez, confere a bebida
fermentada estabilidade química e microbiológica.
Os valores encontrados para o extrato seco total para F1 foi de 9,85 g [L]
[/-1] diferindo estatisticamente do valor encontrado na formulação F2 que
foi de 11,84 g [L][/-1] e são baixos quando comparados com os valores da
normativa 34 do MAPA e inferior ao fermentado de jaca 96,80 g [L][/-1] e
89,52 g [L][/-1] respectivamente. A variação entre os valores de extrato
seco pode ser em função das etapas de clarificação realizadas (uso de
agentes de sedimentação e filtração) desde a preparação do mosto até o
envase do fermentado ou pode ser devida à possível caramelização dos
açúcares no processo de secagem, que impede a completa evaporação das
amostras.
Conclusões
As amostras apresentaram pH, sólidos totais solúveis, acidez total e teor alcoólico estatisticamente semelhantes. O pH ficou na faixa recomendado pela literatura para diminuir a proliferação de microrganimos. Entre os parâmetros estabelecidos pela Instrução Normativa nº 34 as duas formulações tiveram acidez total, acidez e extrato seco inferiores ao permitido. Os parâmetros teor alcoólico e acidez volátil das duas formulações apresentaram valores dentro do permitido na legislação citada. O fermentado feito com açúcar demerara apresentou valores de vitamina C, acidez volátil e extrato seco maiores que o fermentado feito com açúcar cristal.
Agradecimentos
Ao IFPI por disponibilizar os laboratórios para que fosse possível realizar as análises.
Referências
AIDOO, Kofi E.; ROB NOUT, M. J.; SARKAR, Prabir K. Occurrence and function of yeasts in Asian indigenous fermented foods. FEMS Yeast research, Malden, USA, v.6, n.1, p. 30-39, 2006. Disponível em: <https://academic.oup.com/femsyr/article/6/1/30/548560>. Acesso em 01/08/2019.
ANDRADE, Murilo Barbosa et al. Fermentação alcoólica e caracterização de Fermentado de Morango. BBR-Biochemistry and Biotechnology Reports, v. 2, n. 3esp, p. 265-268, 2014.
AQUARONE, Eugenio.; LIMA, U. A.; BORZANI, W. Biotecnologia Industrial. São Paulo: Edgar Blucher LTDA, 2001.
BATISTA, Ângela Maria. Desenvolvimento do fermentado alcoólico do fruto goiaba branca (Psidium guajava) cv. Kumagai – Myrtaceae. Dissertação (Mestrado em Ciência e tecnologia dos alimentos), Instituto Federal de Educação, Ciência e Tecnologia do Triângulo Mineiro - IFTM, Campus Uberaba, 2016.
BRASIL. Ministério da Saúde. Agência Nacional de Vigilância Sanitária. Resolução RDC nº 269, de 22 de setembro de 2005. Regulamento técnico sobre a ingestão diária recomendada (idr) de proteína, vitaminas e minerais. Diário Oficial da República Federativa do Brasil,Poder Executivo, Brasília, DF, 17 dez. 2005.
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento Secretaria de defesa Agropecuária. Portaria nº 64, de 23 de abril de 2008. Regulamentos técnicos para a fixação dos padrões de identidade e qualidade para fermentado de fruta, sidra, hidromel, fermentado de cana, fermentado de fruta licoroso, fermentado de fruta composto e saquê. Brasília, DF: BRASIL, 2008.
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Decreto nº 6.871, de 04 de junho de 2009. Regulamenta a Lei nº 8.918, de 14 julho de 1994. Dispõe sobre a padronização, a classificação, o registro, a inspeção, a produção e a fiscalização de bebidas. Diário Oficial da República Federativa do Brasil, Brasília, DF, 05 jun. 2009. Seção 1.Disponívelem:http://gpec.aduaneiras.com.br/gpex/gpex.dll/infobase/atos/decreto/decreto6871 09/dec%20068 71 09 01.pdf> . Acesso em: 12 nov. 2018.
BRASIL. Ministério da Agricultura, Pecuária e Abastecimento. Instrução Normativa n°34, de 29 de novembro de 2012. Complementação dos padrões de identidade e qualidade para as seguintes bebidas alcoólicas fermentadas: fermentado de fruta, fermentado de fruta licoroso, fermentado de fruta composto, sidra, hidromel, fermentado de cana e saquê ou sake. Diário Oficial da União, Brasília, DF, 30 de nov. de 2012.
DANIELI, F. et al. Determinação de vitamina C em amostras de suco de laranja in natura e amostras comerciais de suco de laranja pasteurizado e envasado em embalagens Tetra Pak. Rev Inst Cienc Saúde, v. 27, n.4, p. 361-365, 2009. Disponível em: <https://www.unip.br/presencial/comunicacao/publicacoes/ics/edicoes/2009/04_out_dez/V27_n4_2009_p361-365.pdf>. Acesso em 11/08//2018.
DIAS, Disney Ribeiro et al. Elaboration of a fruit wine from cocoa (Theobroma cacao L.) pulp. International Journal of Food Science and Technology, , Oxford, v. 42, n. 3, p. 319-329, 2007.Disponível em: https://onlinelibrary.wiley.com/doi/full/10.1111/j.136 2621.2006.01226.x.
DIAS, Disney Ribeiro SCHWAN, R. F.; LIMA, L. C. O. Metodologia para elaboração de fermentado de cajá (Spondias mombin L.). Ciência e Tecnologia de Alimentos, v. 23, n. 3, p. 342-350, 2003. Disponível em: http://www.scielo.br/scielo.php?pid=S0101-20612003000300008&script=sci_abstract&tlng=pt>. Acesso em 04/07/2019.
INSTITUTO ADOLFO LUTZ (IAL). Métodos físico-químicos para análise de alimentos. 4 ed. São Paulo: Instituto Adolfo Lutz, 2008.
MARTINS, S.T.; MELO, B. Spondias (cajá e outras). Instituto de Ciências Agrárias, Universidade Federal de Uberlândia, MG,2002. Disponível em: http//www.fruticultura.iciag.ufu.br/cajá.html. Acessado em: 04 de jul. de 2019.
MUNIZ, Celli Rodrigues; et al. Bebidas fermentadas a partir de frutos tropicais. Boletim do Centro de Pesquisa de Processamento de Alimentos, v. 20, n. 2,p.309-322, 2002.
NUNES, G. D. G.; TOMÉ, P. H. F.; FRAGIORGE, E. J. Elaboração e análise sensorial do vinho de caqui (Diospyrus kaki L.) cv. Fuyu. FAZU, v.6, n.1, p.44-49, 2009.
OLIVEIRA, M. E. S. Elaboração da bebida alcoólica fermentada de cagaita (Eugenia dysenterica, DC) empregando leveduras livres e imobilizadas. (Dissertação de Mestrado) curso de microbiologia agrícola, 86 f., Universidade Federal de Lavras – Lavras/MG, 2010.
OLIVEIRA, Lucas Athayde et al. elaboração de bebida fermentada utilizando calda residual da desidratação osmótica de abacaxi (ananas comosus l.) preparation of fermented beverage using residual syrup of osmotic dehidration of pineaple (ananas comosus l.). Revista Brasileira de Tecnologia, v. 6, n. 01, p. 702-712, 2012.
SANTOS, Yvana Maria Gomes dos et al. Elaboração e caracterização de fermentado alcoólico de jabuticaba (Myrciaria Jaboticaba (Vell) Berg) – XXI Congresso Brasileiro de Engenharia Química – COBEQ / Fortaleza-CE, 2016.
SEGTOWICK, Edilene Cléa Dos Santos; BRUNELLI, Luciana Trevisan; VENTURINI Filho, Waldemar Gastoni. Avaliação físico-química e sensorial de fermentado de acerola. Brazilian Journal of Food Technology. v. 16, n. 2, p. 147-154, 2013.
SILVA, P. H. A.; FARIA, F. C. de; TONON, B.; MOTA, S. J. D.; PINTO, V. T. Avaliação da composição química de fermentados alcóolicos de jabuticaba (Myrciaria jabuticaba). Química nova, São Paulo (SP), v. 31, n. 3, p. 595-600, 2008
SOARES, Ana Aline Justino. Avaliação físico-química e bromatológica da polpa de Spondias purpúrea L (Seriguela) na região do semiárido central paraibano. Dissertação (Mestrado em Ciências Florestais)-Universidade Federal de Campina Grande, Patos. p.65, 2011.
VENTURINI FILHO, Waldemar Gastoni. Bebidas alcoólicas: ciência e tecnologia.Volume 01.São Paulo: Editora Blucher,p.85, 2010.









