ESTUDO DE CINÉTICA E EQUILÍBRIO DE ADSORÇÃO DO CORANTE VERMELHO DE METILA POR RESÍDUO INDUSTRIAL PROVENIENTE DA FABRICAÇÃO DO SILÍCIO METÁLICO
ISBN 978-85-85905-25-5
Área
Ambiental
Autores
Nunes, C.S. (UNIVERSIDADE FEDERAL DO PARÁ) ; Castillo, A.S. (UNIVERSIDADE FEDERAL DO PARÁ) ; Vilhena, K.S.S. (UNIVERSIDADE FEDERAL DO PARÁ)
Resumo
Vários fatores podem influenciar o processo de adsorção, tais como: temperatura, características de adsorvente e adsorvato, pH, potencial de carga zero, cinética e equilíbrio da reação. O vermelho de metila é um corante usado na indústria têxtil e seu descarte inadequado gera impactos ambientais na contaminação de rios e mares. Na busca por adsorventes alternativos que minimizem tais danos destaca-se o resíduo proveniente da fabricação do silício metálico. Este estudo avalia a cinética e equilíbrio de adsorção do resíduo siderúrgico frente ao corante vermelho de metila, aplicando os modelos de cinética de adsorção de pseudo-primeira ordem, pseudo-segunda ordem e Elovich, isotermas de equilíbrio, além de determinar o ponto de carga zero para o resíduo na granulometria inferior a 0,075 mm.
Palavras chaves
Adsorção; Vermelho de metila; Resíduo
Introdução
O aumento das atividades antrópicas vem contribuindo para a contaminação dos recursos hídricos, dentre essas atividades, destaca-se a indústria têxtil. Esse setor é responsável por produzir a maior quantidade de corantes sintéticos e também seu uso e descarte. Dentre os diversos ramos da indústria têxtil, a produção de peças jeans é de grande expressão. O Brasil é o segundo maior produtor de jeans e terceiro maior consumidor (ABIT, 2018). O despejo de águas residuais provenientes dessas fábricas têxteis sem tratamento nos ambientes aquáticos resulta em efeitos tóxicos sobre a fauna e flora aquática. A existência de corantes nos corpos hídricos, dificulta a passagem da luz solar, alterando o processo de fotossíntese e diminuindo a solubilidade de oxigênio. (LALNUNHLIMI; KRISHNASWAMY, 2016). De acordo com Guaratini e Zanoni (2000) existem diversas classes de corantes, dentre esses estão os pertences ao grupo azo. Esse tipo de corante possui em sua constituição a ligação dupla entre dois átomos de nitrogênio (-N=N-) originando o grupamento azo (cromóforo) que é substituído em anéis aromáticos e é altamente resistente à biodegradação. Os corantes azo vêm sendo estudados por serem muito utilizados no mundo todo e por seus possíveis efeitos tóxicos à saúde humana como tumores na bexiga, fígado rins e surgimento de asma (CHUNG, 2016). Métodos como adsorção, coagulação, processos oxidativos e separação por membranas são alguns dos utilizados para retirar corantes tóxicos dos efluentes industriais (RAMOS, 2017). O processo de adsorção tem sido muito empregado para tratamento de águas contaminadas, devido ser um processo de alta eficácia e simples, onde o corante é retirado da fase aquosa e aderido para um sólido, ou seja, para o material adsorvente (CARDOSO, 2010). São requisitos essenciais para a obtenção de informações durante a análise do processo de adsorção o estudo dos fenômenos de equilíbrio e cinética de adsorção, isso porque a adsorção ocorre até que o equilíbrio seja alcançado e a velocidade de adsorção pode influenciar a taxa de remoção do adsorvato. Desta forma os fenômenos de adsorção são influenciados diretamente por fatores como a área superficial, propriedades e características químicas do adsorvente e do adsorvato, condições operacionais, pH do meio, temperatura, dosagem e potencial de carga zero (NASCIMENTO et al, 2014). Diversos materiais alternativos e de baixo custo têm despertado o interesse científico na utilização como adsorventes, destacando-se as argilas, resíduos agroindustriais, zeólitas, leveduras, bagaço de cana de açúcar e compósitos (RAMOS, 2017). Dentre os materiais alternativos usados como adsorventes para a remoção de corantes, encontram-se os resíduos siderúrgicos, que são materiais disponíveis em grandes quantidades e, muitas vezes, sem aproveitamento direto (SANTOS, 2013). A produção do silício metálico ocorre por meio da fusão redutora de quartzo (minério de silício), carvão vegetal e cavaco (madeira) em fornos elétricos do tipo arco submerso. Durante esse processo é produzido um resíduo, conhecido como cinza volante, que é constituído de partículas grossas originadas por combustão e que são retidas em um ciclone pré-separador que reduz a carga de pó ou partículas quentes do gás que chega ao filtro. Esse material é produzido pela empresa Dow localizada em Breu Branco, Estado do Pará (SOUZA, 2015). Nesta pesquisa foi realizado o estudo de cinética e equilíbrio de adsorção do corante azoico vermelho de metila pelo resíduo retido no ciclone pré- separador (cinza volante) durante a produção do silício metálico. Este estudo avaliou a capacidade do resíduo de remoção do corante vermelho de metila de soluções aquosas sob diferentes condições experimentais, tais como: pH, tempo de contato, temperatura e velocidade de agitação do sistema adsorvente. Com o intuito de entender os mecanismos de adsorção para futuras aplicações em escala industrial os dados experimentais obtidos foram analisados em função da capacidade de remoção do corante e aplicados os modelos lineares de cinética de adsorção de Pseudo-primeira ordem, Pseudo-segunda ordem e Elovich. Foi avaliado também o potencial de carga zero para o resíduo. Este estudo tem como finalidade buscar uma possível utilização deste resíduo para o tratamento de efluentes industriais contendo corantes.
Material e métodos
Obtenção do resíduo e análise granulométrica: O resíduo testado como adsorvente foi fornecido pela empresa Dow, situada no município de Breu Branco, Pará. No ensaio de separação granulométrica, uma amostra de massa total de 500 g foi seca em estufa por 24 horas até permanecer constante, e resfriada em dessecador. O material seco foi submetido a peneiramento mecânico durante 5 minutos e o material retido em cada peneira foi pesado. A fração de granulometria inferior a 0,075mm selecionada para os ensaios. Máximo de Absorbância e Curva de Calibração: A concentração do vermelho de metila durante os experimentos foi determinada a partir da elaboração de curva-padrão. Para isso foi preparada uma solução estoque do corante na concentração inicial de 100 mg/L obtida pela dissolução do corante sólido em 60% de água destila e 40% álcool. A partir dessa solução foram preparadas as demais diluições nas concentrações variando entre 2,5; 5,0; 10,0; 15,0 e 20,0 mg/L. Em espectrofotômetro (FEMTO 800-Xi) realizou-se a varredura da solução estoque na faixa espectral entre 350 a 650 nm para determinação da absorbância máxima. Posteriormente, construiu-se a curva de calibração a partir das soluções do corante nas concentrações conhecidas de 2,5 a 20 mg/L. Determinação do Ponto de carga zero: Os sistemas foram preparados com 0,02 g do adsorvente e 20 mL de solução eletrolítica de NaCl 0,1 mol/L. O pH das soluções foi ajustado de 3 a 11 com soluções de HCl e NaOH 0,1 mol/L. Após homogeneização em mesa agitadora a 120 RPM durante 1 hora e temperatura de 25°C. Após o procedimento as amostras foram filtradas e o pH final das soluções foi medido. Todos os ensaios descritos anteriormente foram feitos em batelada e em duplicata. Ensaio de Cinética: O estudo de cinética de adsorção foi realizado variando o tempo de contato do corante (adsorvato) com o resíduo (adsorvente). Em frascos de erlenmeyer 50mL foram adicionados 8 mL de solução do corante na concentração de 20 mg/L e 0,04 g do resíduo. As amostras foram submetidas à agitação constante em mesa tipo Kline, com rotação de 120 RPM, temperatura de 25ºC e pH 4. O tempo de agitação variou em 5, 10, 15, 20, 30, 60, 90 e 120 minutos. Após isso, o sólido foi separado por centrifugação e o líquido obtido foi analisado em espectrofotômetro a 520 nm (máximo de absorbância) para determinação da concentração residual do corante (VM). Ensaio de equilíbrio: Neste experimento foram testadas as soluções de VM nas concentrações de 5,0; 10,0; 15,0; 20,0; 25,0 e 30,0 mg/L. A influência da velocidade de agitação também foi avaliada em 80, 120 e 140 RPM. A massa utilizada foi de 0,04 g e o tempo de ensaio foi de 75 minutos. Os sistemas foram preparados em frascos de Erlenmeyer de 50 mL contendo 8 mL da solução aquosa do corante e tamponada a pH 4 (condição determinada anteriormente como melhor condição de ensaio). Ao final do experimento as amostras foram centrifugadas e uma alíquota da solução foi analisada em espectrofotômetro a 520 nm
Resultado e discussão
Para os ensaios de adsorção optou por utilizar a menor granulometria do
resíduo obtida após a análise granulométrica, que foi aquela inferior e
0,0075mm. Sabe-se que a menor granulometria poderia favorece a adsorção já
que esse fenômeno é considerado um fenômeno de superfície e o aumento da
área superficial pode aumentar a capacidade de adsorção (FOO, 2010).
Primeiramente, foi identificado o comprimento de onda no qual o corante
estudado apresenta o máximo de absorção, para isso foi realizada a varredura
entre 350 e 650 nm em espectrofotômetro UV-VIS (FEMTO – 800Xi) da solução
estoque, encontrou-se o máximo de absorção no comprimento de onda de 520 nm.
Com o propósito de verificar a relação entre absorbância e concentração do
corante vermelho de metila durante os experimentos de cinética e equilíbrio,
foi elaborada a curva de calibração para o referido corante a partir das
absorbâncias medidas em função das seis concentrações conhecidas analisadas.
A curva de calibração obtida demostrou boa linearidade com R² igual a
0,9747. Este parâmetro é um fator importante pois quanto mais próximo de 1
for o coeficiente de correlação (R²) melhor é a qualidade do ajuste
(explicação) da reta descrita pela regressão linear da absorbância em
relação à concentração (AMSTALDEN, 2010).
Com intuito de otimizar o processo adsortivo foi realizada a determinação do
Ponto de Carga Zero (PCZ) para o resíduo. O PCZ é uma característica
importante dos materiais adsorventes e indica o valor de pH do meio líquido
no qual um sólido apresenta carga eletricamente nula na sua superfície. De
acordo com Tagliaferro (2011) a adsorção de cátions é favorecida quando o pH
> pHPZC pois a carga na superfície do material é negativa,
enquanto que a adsorção de ânions é favorecida em pH < pHPCZ pois
a superfície está carregada positivamente. Na Figura 1 é mostrado o
resultado da análise do PCZ, pode-se observar que o pHPCZ no qual
a carga superficial é nula ocorre em 9,29, colocando-se o resíduo em meios
com o pH abaixo desse valor favorecem a adsorção de ânions (superfície +) e
acima de 9,29 os cátions são adsorvidos mais facilmente (superfície -).
O ensaio de cinética de adsorção está relacionado com a velocidade de
remoção do corante da solução pelo adsorvente em relação ao tempo. A
velocidade de adsorção pode ser afetada por diferentes fatores, dentre eles
podemos citar: temperatura, pH, concentração inicial do adsorvato, agitação
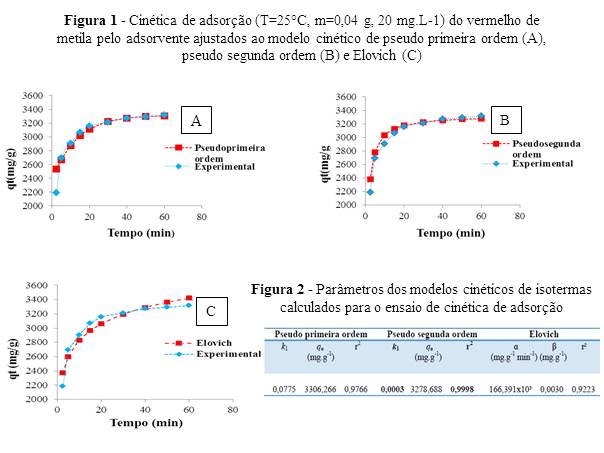
e tamanhos das partículas (NASCIMENTO et al, 2014). A Figura 2 (A, B e C)
apresenta as curvas obtidas para os modelos de cinética de adsorção
aplicados aos dados experimentais. Observa-se que a adsorção do vermelho de
metila pelo resíduo é extremamente favorável devido à isoterma apresentar
forma convexa, como descrito na literatura (NASCIMENTO et al, 2014). Foi
observado nos estudos de cinética de adsorção que, no intervalo de tempo de
0 a 10 minutos, a adsorção do corante variou de 2200 mg/g a 2800 mg/g,
respectivamente, o que indica uma grande capacidade adsortiva neste
intervalo de tempo. Nota-se ainda que a partir de 40 minutos, a isoterma de
adsorção apresentou comportamento assintótico. Os dados experimentais foram
tratados aplicando-se modelos lineares de equações de pseudo-primeira ordem
(A), pseudo-segunda ordem (B) e o modelo de Elovich (C).Apesar dos três
modelos apresentarem resultados ajustados àqueles do comportamento
experimental. As curvas (A, B e C) da Figura 2 demonstram que há maior
concordância entre os dados experimentais e os teóricos do modelo de pseudo
segunda-ordem, indicando este é o modelo que melhor descreve o mecanismo de
velocidade de adsorção. Na Tabela 1 são mostrados os parâmetros obtidos para
os modelos aplicados. O modelo de pseudo-segunda ordem apresentou o valor de
R2 igual a 0,9998 e constante de velocidade k2 de
0,0003, o que indica uma boa aplicabilidade desse modelo para explicar o
comportamento do ensaio de cinética adsorção.
A obtenção de uma isoterma de adsorção é um processo que envolve o contato
entre um adsorvente e um adsorvato, em soluções de diferentes concentrações
conhecidas. Quando o sistema alcança o equilíbrio químico, após certo tempo,
tem-se a concentração de equilíbrio (Ce) e a capacidade de adsorção
do adsorvente no equilíbrio (qe). A isoterma do tipo linear apresenta
uma relação direta entre da massa do adsorvato retida no adsorvente (qe
, mg/g) com a concentração do adsorvato na solução (Ce). Com base
nessa relação, considera-se que quanto maior for a quantidade do adsorvato,
maior será a quantidade adsorvida (FLORIDO, 2011). As isotermas desejadas
idealmente e favoráveis ao processo de adsorção apresentam formas convexas,
pois grandes quantidades adsorvidas podem ser obtidas com baixas
concentrações do adsorvato em solução e a situação inversa é observada nas
isotermas côncavas (NASCIMENTO, 2014).
Os resultados referentes aos ensaios de equilíbrio de adsorção são mostrados
na Figura 3. No gráfico são comparadas as curvas experimentais de adsorção
que relacionam a massa adsorvida de corante (qe) por massa de
adsorvato, resultado expresso em mg/g, para as três velocidades de rotação
testadas. A quantidade adsorvida foi calculada pela seguinte relação: qe
= [(Ci-Ce)/m] x 100. Os resultados demonstraram que o
máximo de adsorção do corante vermelho de metila foi de 4,937 mg do
corante/g de resíduo e foi obtido no ensaio com velocidade de agitação de 80
RPM. Resultados aproximados foram obtidos para as demais condições, de 120 e
140 RPM, sendo que nesta última o comportamento foi mais diferenciado em
relação aos dois primeiros.
Na Figura 4 são mostradas as curvas de eficiência de remoção (%R) do
vermelho de metila nas diferentes concentrações. A eficiência de remoção foi
calculada como: %R = (Ci-Ce/Ci) x 100, onde Ci é
a concentração inicial e Ce corresponde à concentração no equilíbrio,
que a partir dos dados obtidos no ensaio de cinética foi alcançado no tempo
máximo de 75 minutos. Para realização deste ensaio foi avaliada a influência
da velocidade de agitação do sistema no processo adsortivo e observou-se que
nas velocidades de 80 e 120 RPM a eficiência na remoção do corante foi mais
elevada, chegando a 82,29% e 80,23%, respectivamente. Verificou-se que o
aumento da velocidade de agitação para 140 RPM reduziu a eficiência de
remoção para patamares entre 60 e 70% ou seja, verificou-se que ao aumentar
a velocidade de agitação houve redução da taxa de transferência do corante
VM para as partículas do resíduo.
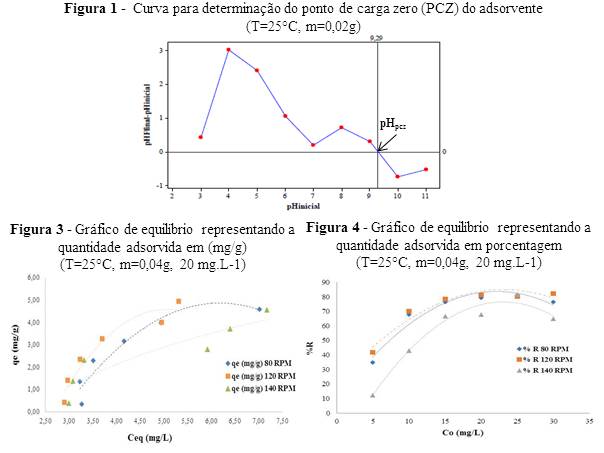
Figura contendo os gráficos de equilíbrio, % remoção e Ponto de Carga Zero.
Gráficos de cinética de adsorção e parâmetros do modelo
Conclusões
Os resultados do estudo de cinética de adsorção demonstraram que o mecanismo que melhor descreve a cinética de adsorção experimental do corante vermelho de metila pelo resíduo se baseia em um modelo de pseudo-segunda ordem. Tanto no experimento de cinética quanto nos de equilíbrio as curvas experimentais apresentaram forma convexa o que indica que o processo de adsorção é favorável para a granulometria testada. Os resultados dos experimentos de adsorção em função das velocidades de rotação demonstraram que em velocidades entre 80 e 120 RPM há capacidade adsortiva superior, chegando a 82% quando comparada com 140 RPM cujo máximo foi de 81%. Em relação ao ponto de carga zero, foi observado que no pH selecionado (pH = 4) é favorecida a adsorção de corantes aniônicos na superfície do sólido. O ensaio em pH 4 permitiu favorecer o processo de adsorção já que neste pH o corante apresentava-se na forma aniônica. A partir dos resultados obtidos pode-se considerar que o resíduo apresenta potencial para ser utilizado como adsorvente. Contudo ensaios futuros, como em coluna de leito fixo, devem ser executados para avaliar outros comportamentos.
Agradecimentos
Os autores agradecem à empresa Dow por fornecer o resíduo utilizado neste estudo, ao Laboratório de Química Multidisciplinar - LAQUIM e à Universidade Federal do Pará - UFPA pelo apoio no desenvolvimento desta pesquisa.
Referências
ABIT ( Associação Brasileira da Indústria Têxtil e de Confecção) perfil do setor têxtil brasileiro (2014). https://www.abit.org.br/cont/perfil-do-setor. Acesso em: 01 de Agosto de 2019.
AMSTALDEN, L. C. Validação e protocolos em análises químicas. Conselho Regional de Química – IV Região (SP). Laboratório T&Analítica – Campinas, 2010.
CARDOSO N. F. Remoção do Corante Azul de Metileno de Efluentes Aquosos Utilizando Casca de Pinhão in Natura e Carbonizada como Adsorvente. Universidade Federal do Rio Grande do Sul-Instituto de química-programa de pós graduação em química. 2010.
CHUNG, K. T. The significance of azo reduction in the mutagenesis and carcinogenesis of azo dyes. Mutation Research, Amsterdam, v. 114, p. 269–281, 1983.
FLORIDO, P. L.; Tese de Doutorado, Universidade Federal do Rio de Janeiro, 2011.
FOO, K. Y.; HAMEED, B. H. Insight into modeling of adsorption isotherm systems. Chemical Engineering Journal 2010, 156, 2.
GUARATINI e ZANONI. Corantes têxteis. Departamento de Química Analítica - Instituto de Química – UNESP- Araraquara-SP. Química Nova SCIELO , N° 23 p. 76, 1999. http://www.scielo.br/pdf/qn/v23n1/2146.pdf. Acesso em: 01 de Agosto de 2019.
LALNUNHLIMI, S.; KRISHNASWAMY, V. Decolorization of azo dyes (Direct Blue 151 and Direct Red 31) by moderately alkaliphilic bacterial consortium. Brazilian Journal of Microbiology, v. 47, p. 39-46, 2016.
NASCIMENTO , F. R.; LIMA A. C, A.; VIDAL B. C; MELO Q. D. ; RAULINO C. S. G. ADSORÇÃO: aspectos teóricos e aplicações ambientais. Repositório UFC. p. 1-258. 2014.
RAMOS, J. P.; PAVÃO, M. F. U.; BARRA, E. C.; VILHENA, K. S. S.; GOUVEIA, F. P. Potencial de Adsorção do Resíduo Proveniente do Processo de Obtenção do Silício Metálico. Revista Virtual de Química, 2017, 9 (2), 751-763, 2017.
SANTOS, E. M. A., et al. Reator anaeróbio tipo UASB conjugado com processo Fenton para remoção de cor e demanda química de oxigênio de água residuária sintética de indústria têxtil. Engenharia Sanitária e Ambiental, vol. 22, p. 285–92. Scielo, doi:10.1590/s1413-41522016148154, 2016.
SANTHI T. Removal of methyl red from aqueous solution by activated carbon prepared from the Annona squmosa seed by adsorption. Chemical Engineering Research Bulletin. p.12. Researchgate, 2010.
TAGLIAFERO G. V.; PEREIRA P. H.*; RODRIGUES A. L.; PINTO C. L. Cadmium, lead and silver adsorptio in hydrous niobium oxide prepared by homogeneous solution method. Quím. Nova vol.34 no.1 São Paulo. Scielo, http://dx.doi.org/10.1590/S0100-40422011000100020 , 2011.









