PREPARAÇÃO DE ÉSTERES E AMIDAS AROMÁTICAS VIA MEIO AQUOSO MAIS SUSTENTÁVEL
ISBN 978-85-85905-25-5
Área
Ensino de Química
Autores
Rezende, D.V.A. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Rezende, B.A. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Oliveira, M.V.M. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Silva, A. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Cintra, C.A. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Santos, J.G. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Santos, J.M. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT)) ; Batalini, C. (UFMT/LAPQUÍM/CUA - PONTAL DO ARAGUAIA (MT))
Resumo
Ésteres e amidas constituem funções orgânicas clássicas em Química Orgânica. Tradicionalmente, em aulas práticas dessa disciplina, essas substâncias são preparadas utilizando ácidos inorgânicos fortes como catalisadores e sistema de aquecimento (refluxo). Este trabalho ressalta um caminho sintético alternativo e bem mais brando para a preparação de ésteres e amidas aromáticas, através do método de Schotten-Baumann, em meio aquoso básico e temperatura ambiente. Três ésteres e duas amidas aromáticas foram assim preparadas e caracterizadas por ponto de fusão, cromatografia em camada delgada (CCD), ultravioleta-visível (UV-VÍS) e espectroscopia no infravermelho. Esta metodologia denotou um caminho sintético econômico, pouco agressivo à natureza e rendimentos reacionais satisfatórios.
Palavras chaves
Amidas; Ésteres; Síntese orgânica
Introdução
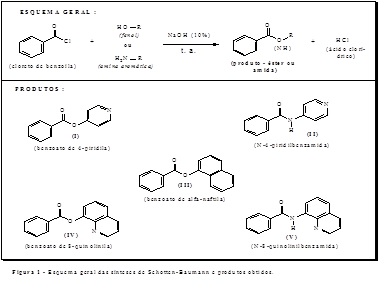
É muito comum a inserção de práticas laboratoriais envolvendo síntese orgânica nas disciplinas de Química Orgânica nos cursos universitários do país. A preparação de ésteres e amidas, seja para a obtenção de aromas artificiais, fármacos e derivados são exemplos de sínteses bem comuns e que são exploradas no meio acadêmico. Entretanto, geralmente essas sínteses envolvem um meio reacional agressivo, tanto para o meio ambiente, quanto para o experimentador, uma vez que são utilizados catalisadores constituídos de ácidos inorgânicos fortes (ácido sulfúrico - H2SO4 ou ácido fosfórico - H3PO4) e sempre acompanhados de aquecimento (MARCH & SMITH, 2007). Uma rota alternativa para a preparação de ésteres e amidas aromáticas, em um meio reacional bem mais ameno, vem sendo utilizado com sucesso nas aulas experimentais de Química Orgânica II dos cursos de Licenciatura em Química e Bacharelado em Farmácia da UFMT/CUA: constitui na clássica reação de Schotten-Baumann, conduzida em meio aquoso básico e temperatura ambiente (SOARES et al., 1988). Nessa reação, cloretos de ácido aromático podem combinar com fenois e aminas aromáticas para gerarem ésteres e amidas aromáticas. Este trabalho segue essa estratégia sintética mais racional e objetivou preparar, purificar e caracterizar três ésteres aromáticos: benzoato de 4-piridila (I), benzoato de alfa-naftila (III) e benzoato de 8- quinolinila (IV) e duas amidas aromáticas: N-4-piridilbenzamida (II) e N-8- quinolinilbenzamida (V) (figura 1).
Material e métodos
Utilizou-se a mesma metodologia para as sínteses das cinco substâncias aromáticas (MARVEL & LAIZER, 1941; SOARES et al., 1988). Em um erlenmeyer de 250 mL, suspendeu-se 12,0 mmols dos fenois 4-hidroxipiridina, alfa-naftol e 8-hidroxiquinolina e 12,0 mmols das aminas 4-aminopiridina e 8- aminoquinolina em 100 mL de solução aquosa de hidróxido de sódio (NaOH) a 10% (m/v), à temperatura ambiente e sob agitação com barra magnética e após 20 minutos, 60,0 mmols de cloreto de benzoíla foram adicionados à solução. A reação foi mantida por mais 40 minutos sob as mesmas condições e os sólidos resultantes foram filtrados em funil de Büchner, lavados várias vezes com água destilada e os cristais foram secos em dessecador contendo sílica gel, sem a presença de vácuo. Os ésteres (I) e (IV) foram recristalizados em água destilada, enquanto o éster (III) em 1-butanol. As duas amidas aromáticas (II) e (V) foram recristalizadas em metanol. Os valores de pontos de fusão foram conseguidos manualmente em tubo de ensaio de 30 cm de altura e 3,0 cm de diâmetro, preenchido com glicerina, acoplado a um termômetro. Para as análises de cromatografia em camada delgada (CCD) foram empregadas placas prontas de sílica gel G 60 como fase estacionária e clorofórmio como fase móvel, observando as manchas que caracterizam as substâncias em câmara escura com lâmpada de ultravioleta-visível e também em cuba de vidro contendo cristais de iodo (COLLINS et al., 1997). Espectros de ultravioleta- visível (UV-VÍS) foram obtidos em espectrômetro Varian, modelo Cary 50 Scan e espectros de infravermelho foram obtidos em espectrofotômetro com transformada de Fourier, modelo Perkin Elmer Spectrometer 100, resolução de 4 cm-1, na região compreendida entre 4000-600 cm-1 (PAVIA et al., 2010; SILVERSTEIN et al., 2006).
Resultado e discussão
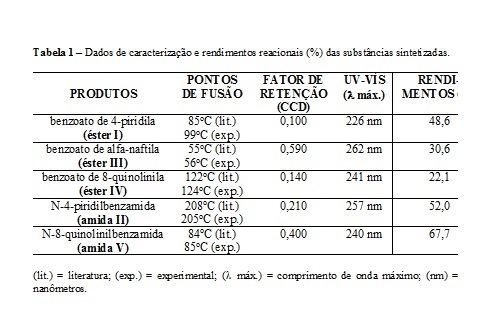
Na tabela 1 encontram-se os rendimentos reacionais, após recristalização e
alguns dados de caracterização dos ésteres e amidas sintetizadas. Os
rendimentos das reações revelaram-se de médio a bom, com perdas esperadas
após a recristalização. Quanto às cores dos cristais, o éster (I) apresentou
cor cinza, a amida (V) cor marrom e as demais (II), (III) e (IV) geraram
cristais brancos. Com exceção do éster (I), os pontos de fusão experimentais
estão em boa concordância com os exibidos na literatura. Todas as
substâncias apresentaram uma única mancha CCD. Os dados de UV-VÍS das amidas
(tabela 1) apresentam comprimento de onda máximo bem característico e esses
dados não foram encontrados na literatura. O mesmo se pode sublinhar sobre
os dados de infravermelho, cujos principais estiramentos encontrados foram:
Éster (I): C=O (1678 cm-1), C=C aromático (1600 - 1400
cm-1), C-O (1289
cm-1 e 982 cm-1); Éster (III): C = O (1733
cm-1), C=C aromático (1600-1400 cm-1), C-O (1221 e
1089 cm-1); Éster (IV): C=O (1730 cm-1), C=C aromático
(1600 cm-1
- 1400 cm-1), C-O (1229 cm-1 e 1096 cm-1);
Amida (II): N-H (3343 cm-1), C-H
(3037 cm-1), C=O (1676 cm-1), N-H (1506
cm-1) e C-N (1293 cm-1); Amida (V):
N-H (3352 cm-1), C-H (3054 cm-1), C=O
(1671cm-1), N-H (1526 cm-1) e C-N
(1325 cm-1).
Conclusões
A substituição de métodos clássicos de preparação de ésteres e amidas aromáticas por uma rota alternativa, num ambiente mais limpo, simples e econômico, dentro da disciplina de Química Orgânica, demonstrou eficácia e maior segurança para os alunos-experimentadores. Os rendimentos reacionais foram satisfatórios e a caracterização das substâncias apresentou boa concordância com a literatura e com as estruturas propostas.
Agradecimentos
À UFMT - Campus Universitário do Araguaia e aos membros do LAPQUÍM.
Referências
COLLINS, C. H.; BRAGA, G. L.; BONATO, P. S. Introdução a Métodos Cromatográficos, 7 ed., Campinas (SP): Ed. da UNICAMP, 1997.
MARCH, J.; SMITH, M. B. Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 6 ed., Wiley-Interscience, 2007.
MARVEL, C. S.; LAIZER, W. A. Organic Syntheses, Coll. v. 1, p. 99; v. 9, p. 16, 1941.
PAVIA, D. L.; LAMPMAN, G. M.; KRIZ, G. S.; VYVYAN, J. R. Introdução à Espectroscopia, trad. 4 ed. norte-americana, São Paulo (SP): Cengage Learning, 2010.
SILVERSTEIN, R. M., WEBSTER, F. X.; KIEMLE, D. J. Identificação Espectrométrica de Compostos Orgânicos, 7 ed., Rio de Janeiro (RJ): LTC, 2006.
SOARES, B. G.; SOUZA, N. A.; PIRES, D. X. Teoria e técnicas de preparação, purificação e identificação de compostos orgânicos, Rio de Janeiro (RJ): Guanabara, 1988.









