Pd-M1-M2/C modificado por Sc, Ni e Ga para atuar em célula à combustível em meio alcalino
- Home
- Trabalhos
ÁREA
Química de Materiais
Autores
de A. Valadão, L.H. (UFES) ; Ribeiro, J. (UFES)
RESUMO
Este trabalho preparou e investigou eletrocatalisadores baseados em Pd modificados com Ni, Sc e Ga para atuar em células a combustíveis alcalinas. A caracterização físico-química por difração de raios X mostrou que os eletrocatalisadores são compostos basicamente pela liga de Pd cúbica de face centrada, com parâmetro de rede, a, (3,889 Å - 3,891 Å). A voltametria cíclica mostrou um perfil característico de eletrocatalisadores baseados em Pd com uma grande carga capacitiva que pode estar associada aos óxidos dos metais modificadores do material (Ni, Sc e Ga). O estudo de cronoamperometria mostrou que o melhor eletrocatalisadores é o ternário composto de Pd50Ni25Ga25/C seguido pelo ternário Pd50Sc25Ga25/C. O teste de CO-stripping mostrou um EonsetCO próximo a 0,6 V vs. ECS.
Palavras Chaves
Paládio; Célula a combustível; Escândio
Introdução
Algo nítido na sociedade moderna é a sua crescente necessidade por fontes de energia que sejam eficientes e viáveis – econômica e fisicamente - para as mais diversas funções, e que sejam, ao mesmo tempo, sustentáveis e não poluentes. Essa necessidade tem impulsionado a busca pelo desenvolvimento de tais fontes no cenário mundial da pesquisa científica. E dentro desse cenário, uma tecnologia relativamente recente tem sido cada vez mais proeminente, por se encaixar bem nesses requisitos: as células à combustível. As células à combustível, basicamente, são células eletroquímicas galvânicas, e, portanto, transformam a energia livre de Gibbs associada a uma reação de oxirredução em energia elétrica. Elas se diferenciam das pilhas comuns, principalmente, por utilizarem combustíveis continuamente fornecidos (armazenados externamente) para a célula, ao invés de haver um suprimento limitado contido no interior do sistema. E esses combustíveis podem ser de vários tipos e identidades, como o hidrogênio (gasoso), o metanol ou o etanol (líquidos), por exemplo, cada um com suas vantagens e desvantagens. [1-2] No caso das células de etanol, esses catalisadores costumam ser baseados em ligas de Pd ou de Pt com outros metais de transição, como Sn, Ru ou Ni, em proporções variadas, e o vigente projeto tem como foco de estudo justamente uma dessas duas classes de catalisadores, os de Pd. Dentro dessa categoria, o trabalho em questão visa a síntese de ligas binárias e ternárias do Pd com Sc, Ga e Ni, juntamente com a caracterização físico e eletroquímica dessas, avaliando seus potenciais para a utilização em células de etanol direto.
Material e métodos
Síntese dos catalisadores: Foram sintetizados cinco eletrocatalisadores: Pd50Ni50/C, Pd50Ni25Ga25/C, Pd50Sc50/C Pd50Sc25Ga25/C e Sc/C, sendo que o “C” precedido por uma barra indica que o catalisador é suportado em carbono e os índices inferiores indicam as proporções molares da fração metálica. A proporção de carbono para metais é de 60:40, em massa, no catalisador formado, teoricamente. O catalisador Pd50Sc50/C, porém, foi sintetizado duas vezes, ambas da mesma forma, e as duas amostras deste serão diferenciadas em sua representação por um asterisco. A amostra representada, dessa forma, por Pd50Sc50*/C foi submetida apenas aos testes de caracterização físico-química, enquanto a amostra representada simplesmente por Pd50Sc50/C foi submetida apenas aos testes de caracterização eletroquímica. Todos os catalisadores seguiram o mesmo processo de síntese, variando-se apenas nas quantidades absolutas de reagentes, na ordem de adição dos sais precursores e nos intervalos de tempo em certas etapas. As quantidades relativas de metal (total), ácido cítrico (AC) e etilenoglicol (EG), que reagem para formar o catalisador, são, em proporção molar, 1:4:16. Todos foram sintetizados desta forma: misturou-se ácido cítrico (Sigma- Aldrich) e etilenoglicol (Di-nâmica Química Contemporânea LTDA), sendo que o EG é adicionado com excesso de 5 mL, contribuindo para a completude da reação e para a formação do meio reacional. Adicionou-se os sais precursores metá- licos – isto é, Pd(NO3)2·2H2O; Ni(NO3)2·6H2O; Ga(NO3)3·xH2O; ScCl3·xH2O (todos da Sigma-Aldrich) – e o carbono Vulcan XC72 (Carbot), tratado previamente com ácido nítrico. As quantidades de cada reagente foram calculadas de forma a se obter 100 mg de cada catalisador e estão apresentadas na Tabela 1.
Resultado e discussão
Exceto pelo do Sc/C, todos os padrões de difração de raios X apresentam picos
referentes a estrutura cúbica de face centrada do paládio por volta de 40,1°,
46,5°, 68,1° e 82°, referentes aos planos (1 1 1), (2 0 0), (2 2 0) e (3 1 1)
[3]. O padrão de difração de raios X do Sc/C expõe alguns picos relativos ao
escândio e, principalmente, alguns relativos ao óxido de escândio. Porém,
todos eles possuem intensidades relativamente muito baixas, se comparados aos
picos citados anteriormente.
Na amostra de Pd50Ni50/C, o pico relativo ao plano (1 1 1), de maior
intensidade, apresenta um deslocamento de apenas 0,02° em relação ao paládio
puro. Há um deslocamento de 0,16° (em relação ao paládio puro) no pico
relativo ao plano (2 0 0), e de 0,11° no referente ao plano (3 1 1). Existe a
formação de liga, entre o Pd e o Ni, mas essa formação de liga não se dá de
forma tão eficaz, visto que os deslocamentos, particularmente o do pico mais
intenso, não são tão significativos.
Exceto pelo do Pd50Sc50/C, todos os voltamogramas de catalisadores contendo Pd
apresentam os picos catódicos na região entre -0,6 V a -0,4 V (especialmente
próxima a -0,45 V), atribuídos à redução de PdO, e exceto também pelo
Pd50Ni50/C, demonstram boa reprodutibilidade após as etapas de hidratação e
condicionamento, além de haver uma melhora na definição dos picos, atestando a
eficácia e suficiência dessas etapas como ativadoras/limpadoras dos sítios
ativos dos catalisadores considerados. O Pd50Ni50/C, todavia, é excetuado
apenas pela diminuição na definição do pico mencionado, relativo à redução do
óxido de paládio. Este pico é melhor caracterizado na etapa de hidratação.
A Figura 2 apresenta a cronoamperometria dos catalisadores Pd50Ni25Ga25/C,
Pd50Ni50/C, Pd50Sc25Ga25/C e Sc/C.
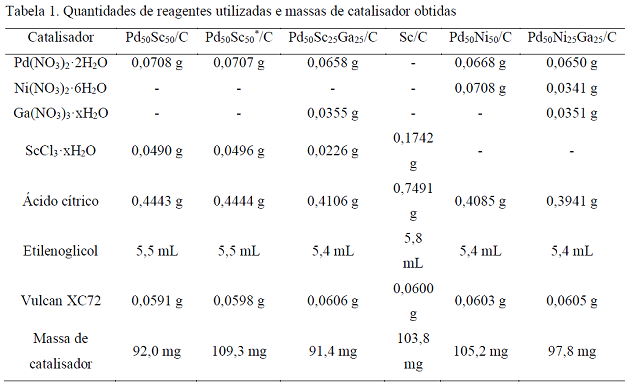
Quantidades de reagentes utilizadas e massas de catalisador obtidas
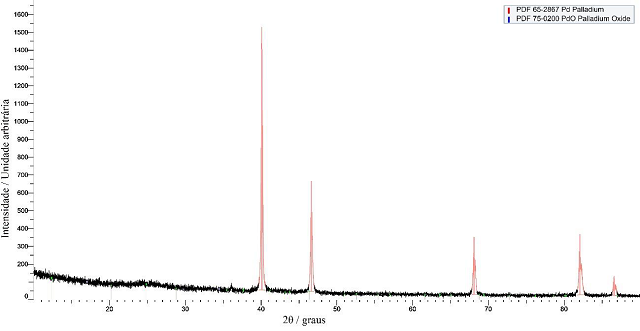
Padrão de difração de raios X para o catalisador Pd50Sc25Ga25/C.
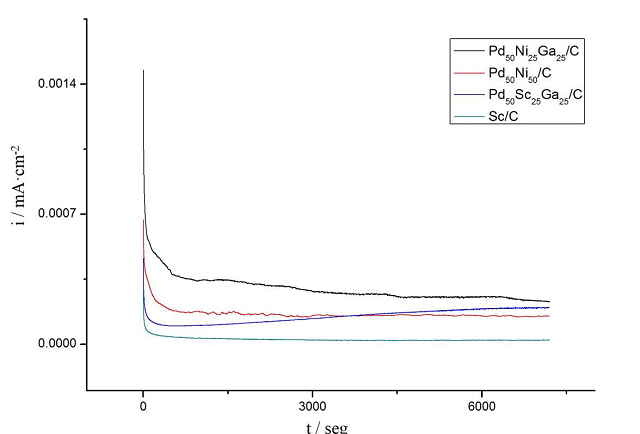
Cronoamperogramas dos catalisadores Pd50Ni25Ga25/C, Pd50Ni50/C, Pd50Sc25Ga25/C e Sc/C.
Conclusões
As amostras contendo Sc (exceto a de Sc/C), particularmente a de Pd50Sc25Ga25/C, apresentaram as maiores densidades de corrente, o que pode ser consequência da baixa quantidade de óxidos presentes nessas amostras, ao contrário das amostras de Ni, que apresentaram intensidades menores e maior quantidade de óxido formado, o que diminuiria a quantidade de sítios ativos disponíveis de Pd. Catalisadores contendo Sc apresentaram comportamento curioso em alguns ensaios eletroquímicos, sendo portanto, uma elemento promissor na modificação de eletrocatalisadores baseados em Pd.
Agradecimentos
Os autores agradecem a FAPES, CAPES e CNPq pelo suporte financeiro.
Referências
[1] PAGANOTO, G. T. Fabricação de catalisadores de PtSn/C modificados com Ni e Ga para a oxi-dação de etanol. 2016. Dissertação (Mestrado em Química) – Programa de Pós-graduação em Química, Universidade Federal do Espírito Santo, Vitória, 2016.
[2] EVANGELISTA, T. C. S. Síntese, caracterização e avaliação do desempenho eletroquímico de catalisadores do tipo PtSnGaBi/C frente à oxidação do etanol para atuação em células a combustível. 2016. Monografia (Bacharelado em Química) – Departamento de Química, Universidade Federal do Espí-rito Santo, Vitória, 2016.
[3] ZHANG, Z.; XIN, L.; SUN, K.; LI, W. Pd–Ni electrocatalysts for efficient ethanol oxidation reaction in alkaline electrolyte. International Journal of Hydrogen Energy, v. 36. n. 20. p. 12686-12697, out. 2011.


