Efeitos da fonte de íons Brometo sobre a síntese de Nanopartículas de Carbeto de Ferro
- Home
- Trabalhos
ÁREA
Físico-Química
Autores
Machado, D.T. (IQSC-USP) ; Varanda, L.C. (IQSC-USP)
RESUMO
Carbetos de Ferro possuem excelentes propriedades físico-químicas, são empregados em armazenamento e hipertermia magnética e como catalisadores para reações de evolução de hidrogênio, hidrogenação de COx e Fischer-Tropsch. São sintetizados em fornos, onde óxidos de ferro são reduzidos ao estado metálico seguido pela carburação de compostos orgânicos na superfície metálica. Neste trabalho nanopartículas de carbetos de ferro foram sintetizadas via decomposição térmica do Fe(acac)3 a 340°C, em meio de oleilamina com indução por diferentes fontes de íons brometo. Obteve-se nanopartículas mistas de Fe5C2 e Fe3C, de formato esferoidal entre 80-410 nm, revestidas por carbono e com comportamento ferromagnético mole influenciado pelo tamanho.
Palavras Chaves
Nanopartículas; Carbetos; Metais de Transição
Introdução
Carbetos de ferro pertencem a classe dos compostos binários denominados carbetos de metais de transição, são formados pela junção de átomos de carbono e metais de transição com elétrons de valência “sd”¬, apresentam alta dureza, elevados pontos de fusão e ótimas propriedades catalíticas e de condução elétrica e térmica(GREENWOOD; EARNSHAW, 1997; KOSOLAPOVA, 1995). Atualmente, nanopartículas (NP) de carbetos de ferro são utilizadas em aplicações biomédicas, como hipertermia magnética, materiais de contraste para ressonância, plataforma de transporte e entrega de drogas(BORDET et al., 2019; MEFFRE et al., 2012; YU et al., 2017), e como catalisadores em reações Fischer-Tropsh(HONG et al., 2015; WEZENDONK et al., 2018; YANG, C. et al., 2012), hidrogenação de COx(BORDET et al., 2016; LI et al., 2019) e evolução de hidrogênio(LI et al., 2018, 2019). Em relação à estrutura cristalina, carbetos de ferro apresentam fases distorcidas de maior simetria semelhantes a rede cristalina metálica, onde átomos de carbono ocupam sítios octaédricos ou tetraédricos localizados entre os átomos metálicos, promovendo distorção na rede(CARBON N. Y., 1997; GOLDSCHMIDT, 1967; KOSOLAPOVA, 1995). Estudos do sistema binário ferro- carbono mostram a existência fases diversas com diferentes estruturas cristalinas e estequiometrias, as quais podem ser separadas naquelas onde o átomo de carbono ocupa o sítio tetraédrico (θ-Fe3C, χ- Fe5C2 e Fe7C3) ou o sítio octaédrico (ε’-Fe2.2C e ε-Fe2C). A composição mais estável é a fase θ-Fe3C, conhecida como cementita, é formada por uma célula unitária ortorrômbica contendo 12 átomos de ferro e 4 átomos de carbono. A fase χ-Fe5C2, conhecida como carbeto de Hagg, possui célula unitária monoclínica e pode ser convertida na fase θ- Fe3C em temperaturas próximas a 360°C. As fases ε’- Fe2.2C e ε-Fe2C possuem células unitárias tipo hexagonal, são fases instáveis e muito parecidas por possuírem a mesma estrutura com uma pequena variação de estequiometria. Por fim, a fase Fe7C3 pode possuir célula unitária ortorrômbica ou hexagonal, sendo obtida em condições de extrema pressão(JUNG; THOMSON, 1993; LAI et al., 2018; NAGAKURA, 1959; YANG, C. et al., 2012). A redução carbotérmica é o método mais empregado na produção industrial de carbetos de ferro bulk devido ao maior controle das condições de síntese e composição do produto. Neste processo, óxidos de ferro (Fe2O3, Fe3O4 e FeO) são incialmente reduzidos a ferro metálico em temperaturas elevadas (>700°C) por gases redutores (H2 ou CO) e/ou fontes de carbono (grafite, carvão, CO, benzeno ou hidrocarbonetos gasosos de baixa massa molar). A segunda etapa, carburação, é iniciada assim que há fase metálica presente, as fontes de carbono adsorvem na superfície metálica recém-formada que catalisa sua quebra em átomos de carbono livre, os quais difundem para os interstícios da estrutura metálica formando a fase carbeto(KOSOLAPOVA, 1995; PARK et al., 2001; SHEN, 2015; STEPHENS; WILLIAMSON; HAGER, 1993). Diferentemente dos sistemas bulk, sistemas de NP de carbeto de ferro foram obtidos apenas na última década através da decomposição de compostos metal-orgânicos em alquiaminas de cadeia longa. Yang e colaboradores produziram nanopartículas de Fe5C2 via decomposição térmica a 350°C do precursor metálico tóxico e volátil Fe(CO)5 no solvente octadecilamina e na presença do agente indutor brometo de hexadeciltrimetilamônio. De acordo com estes autores, durante a síntese ocorre a decomposição do precursor (~180°C) originando NP de óxidos de ferro que, com aquecimento, são reduzidas ao estado metálico (~270°C) e catalisam a desidrogenação do grupo amina a cianeto. Em temperaturas próximas a 350°C, as NP de ferro promovem a pirólise destes cianetos originando hidrocarbonetos insaturados e cianetos de menor cadeia, que servem como fonte de carbono para formação da fase carbeto. A presença do íon brometo mostrou-se essencial para a formação da fase carbeto, sem este íon NP de ferro metálico de baixa cristalinidade são obtidas e facilmente oxidadas, impedindo a etapa de carburação da fase metálica(YANG, C. et al., 2012). Neste trabalho, propomos a síntese de NP de carbeto de Ferro em meio de oleilamina, uma alquilamina primária de cadeia longa e insaturada comumente utilizada na síntese de nanopartículas metálicas (BARANOV et al., 2019; MOURDIKOUDIS; LIZ-MARZÁN, 2013), através da decomposição térmica do precursor metálico Fe(acac)3, o qual apresenta maior solubilidade em solventes orgânicos e menor toxicidade em relação ao Fe(CO)5 (BECK et al., 2011; VARANDA; JAFELICCI, 2006).
Material e métodos
Reagentes: Oleilamina(70,0%, Sigma Aldrich), Acetilacetonato de Ferro(III)(97,0%, Sigma Aldrich, Fe(acac)3), 1,2- Hexadecanodiol(90,0%, Sigma Aldrich, HDD), Brometo de Hexadeciltrimetilamônio(98,0%, Merck, CTAB), Brometo de Amônia(99,8%, Riedel-de Haën, NH4Br) e Brometo de Níquel(99,0%, Sigma Aldrich, NiBr2). Síntese das Nanopartículas de Carbeto de Ferro: 10 ml de Oleilamina e 0,6 mmol Fe(acac)3 foram adicionados em um balão de 3 bocas de 125 ml, um condensador de Graham foi acoplado ao balão e mantido a 70°C por um banho de água. O balão foi posicionado sobre uma manta de aquecimento acoplada a um controlador de temperatura, regulado por um termopar imerso na solução. Foram acionados um baixo e constante fluxo de nitrogênio e agitação magnética, o sistema foi aquecido (10°C.min-1) até 340°C e mantido nesta temperatura por 2 horas então, foi resfriado até a temperatura ambiente onde as nanopartículas foram precipitadas e lavadas em centrífuga diversas vezes com isopropanol e, por fim, foram dispersas e armazenadas em hexano para posterior caracterização. Nas variações do procedimento padrão foi adicionado 1,8 mmol de HDD ou 1,8 mmol de HDD e 0,05 mmol de CTAB, NH4Br ou NiBr2. Caracterizações: ”Difratômetria de raios X” foi realizada num difratômetro Bruker D8 Advance operando com radiação λ=0,15418 nm. As amostras foram depositadas num substrato de silício e a identificação das fases foi feita com o do banco de dados “Crystallography Open Database”(COD - CRYSTALLOGRAPHY OPEN DATABASE, [s. d.]). A ”Microscopia Eletrônica de Transmissão” foi realizada num JEOL, modelo JEM 2100 operando a 200 kV, e empregada para avaliar a morfologia, tamanho e distribuição de tamanhos das nanopartículas. As amostras foram depositadas sobre uma grade de cobre recoberta com o polímero Formvar®. O tamanho foi determinado pela contagem de aproximadamente 130 nanopartículas, o diâmetro médio (D), o desvio-padrão (s) e o grau de polidispersividade (σ = s/D) foram obtidos com o ajuste da função LogNormal, considerou-se o limite de monodispersividade como 10%(HUNTER, 2001). A ”Espectroscopia Raman” foi empregada para análise estrutural da camada de carbono que reveste as nanopartículas. Foi realizada num Horiba LabRAM HR Evolution, operando com laser de 473 nm a 1% da potência no intervalo de 1000-2000 cm-1. Os dados experimentais foram ajustados por uma soma de 5 funções de Lorentz, denominadas D*, D, D", G e D'(CLARAMUNT et al., 2015; SELVARAJAN et al., 2019). A ”Magnetômetria de Amostra Vibrante” foi realizada em um magnetômetro convencional e utilizada para determinar as propriedades magnéticas. Uma massa na ordem de 5 mg foi utilizada para as medidas, as quais foram realizadas a temperatura de 25 °C com campo magnético variando de -15 kOe à 15 kOe.
Resultado e discussão
Na Figura 1(A) são apresentados a estrutura dos reagentes utilizados e o
esquema resumido do processo de síntese. Diferentemente do Fe(CO)
5 que possuí o metal no estado de oxidação 0, o precursor
metálico Fe(acac)3 apresenta o metal no estado de oxidação +3 e
deve ser reduzido ao estado +0 para originar a fase metálica e, consequente,
permitir a carburação dos compostos orgânicos para originar a fase carbeto.
Além disto, o solvente utilizado Oleilamina 70% contêm impurezas que variam
a cada lote e alteram algumas de suas propriedades físico-químicas tais como
cor, ponto de ebulição e capacidade redutora(BARANOV et al., 2019;
MOURDIKOUDIS; LIZ-MARZÁN, 2013). As duas primeiras sínteses foram propostas
a fim de se avaliar a capacidade redutora do sistema, na primeira delas
(FeC) a decomposição do Fe(acac)3 foi promovida apenas em
Oleilamina enquanto na segunda (FeC_HDD), a decomposição foi realizada na
presença de Oleilamina e do agente redutor 1,2-Hexadecanodiol.
Posteriormente, três sínteses com agente redutor e fontes de íons brometo
variadas - CTAB(FeC_HDD_CTAB), NH4(FeC_HDD_NH4) e
NiBr2(FeC_HDD_NiBr2) - foram propostas para se
estabilizar a fase carbeto e avaliar os efeitos destas fontes sobre as
propriedades físico-química das NP. Na figura 1(B) são apresentados os
difratogramas de raios X de todas as amostras, bem como dos padrões de
difração das fases FeO(COD 9009766), Fe5C2(COD
1521831) e Fe3C(COD 1008725). Nas duas primeiras amostras são
observados picos de difração localizados em 2θ equivalentes a 36,1°, 42,0° e
60,5° referentes a fase FeO e além dela, quando o agente redutor foi
utilizado, picos de difração referentes a uma mistura das fases
Fe5C2 e Fe3C são observados em 2θ
equivalentes a 37,3°, 39,5°, 40,6°, 42,8°, 43,5°, 44,6°, 45,8°, 49,1° e
58,1°. A maioria dos picos referentes a estas fases não estão resolvidos
devido a localização próxima e a capacidade de resolução do equipamento,
sendo possível inferir a presença das fases carbeto através da análise do
difratograma na região de 2θ entre 47° e 51°. Nesta região são observados e
resolvidos picos exclusivos de cada fase, sendo observados reflexões
referentes a fase Fe5C2 em 47,3°, 47,6°, 50,1° e 50,3°
originados pelas reflexões dos planos (211), (600), (511) e (312), e
referentes a fase Fe3C em 48,5°, 48,6° e 49,2° originados pelas
reflexões dos planos (022), (131) e (221). A adição do HDD aumentou a
capacidade redutora do sistema, auxiliando na formação de NPs de Fe metálico
que posteriormente originam a fase carbeto. Apesar disto, as NP de Fe
formadas sem a presença de íons brometo no meio reacional são reativas e se
oxidam com facilidade(LACROIX et al., 2011; YANG, Z. et al., 2017), pois o
íon melhora a cristalização da fase metálica e auxilia na estabilização da
fase carbeto ao diminuir dinamicamente a disponibilidade de sítios de
nucleação, permitindo a formação de partículas com melhor
cristalinidade(LACROIX et al., 2011; YANG, C. et al., 2012; YANG, Z. et al.,
2017). Nas três amostras sintetizadas na presença de íons brometo não há
picos referentes a fase FeO e não se observa diferenças significativas entre
os difratogramas de raios X, os quais indicam a formação de uma mistura das
fases Fe5C2 e Fe3C. Estas três amostras
foram caracterizadas por microscopia eletrônica de transmissão a fim de se
obter informações sobre formato, tamanho e distribuição de tamanhos das NP,
Figura 2(A). Nas amostras sintetizadas com CTAB, NH4 e
NiBr2 são observados, respectivamente, partículas de formato
esferoidal com diâmetro médio(D) de 187, 409 e 83 nm, desvio padrão(s) de
44, 115 e 23 nm e polidispersividade(σ) de 23,5%, 28,1% e 27,7%, indicando
que as sínteses levaram a uma larga distribuição de tamanho e nenhum dos
sistemas pode ser considerado monodisperso. A substituição do CTAB pelo sal
NH4Br resultou em partículas de maior diâmetro, este efeito
provavelmente é consequência do impedimento estérico da molécula de CTAB, a
qual possuí cadeia carbônica de 16 átomos o que dificulta a aproximação,
aglomeração e crescimento das partículas. A introdução do íon Ni(II) via
NiBr2 promoveu a redução do diâmetro das NP, este íon possui
menor potencial de redução que o íon Fe(III) e, desta forma, é reduzido
primeiro dando início ao processo de nucleação de partículas Ni que atuam
como sementes para o crescimento das NP de ferro. Conhecido como nucleação
heterogênea, este processo resulta em partículas com menor tamanho do que
processos que não utilizam estes tipos de sementes(FIÉVET et al., 2018). As
NP se encontram aglomeradas devido ao caráter magnético e são semelhantes a
um Core-Shell pois se encontram revestidas por uma camada composta por
elemento de baixa massa atômica, posto o baixo contraste em comparação ao
suporte de carbono do grid. O processo de formação da fase carbeto necessita
da deposição de átomos de carbono na superfície metálica, o revestimento
observado é, provavelmente, resquício do processo de síntese formado por uma
fase rica em carbono. A espectroscopia Raman foi utilizada para analisar
essa pequena camada de revestimento, Figura 2(B), é uma técnica simples e
não destrutiva empregada na análise de materiais a base de carbono já que
apresentam um espectro simples com poucas bandas – denominadas D*, D, D”, G
e D’ - de elevada intensidade. A razão entre a intensidade das bandas D e G
(ID/IG) serve como uma medida da extensão dos defeitos
estruturais, mas há controvérsias na literatura sobre o modo como é
calculado já que este desconsidera o efeito das bandas D*, D’’ e D’, citadas
em trabalhos recentes. A banda D* é originada por ligações sp2-
sp3 nas bordas de uma rede hexagonal e está localizada em 1100-
1200 cm-1. A banda D é associada ao modo vibracional de
respiração A1g de uma rede hexagonal com defeitos no plano basal
e está localizada próximo a 1350 cm-1, é induzida por desordem
estrutural da rede em sistemas ligações do tipo sp2. A banda D”
está localizada em 1500-1550 cm-1 e é induzida defeitos
associados a estruturas amorfas com ligações sp2, o que pode
incluir pequenas moléculas funcionalizadas. A banda G e está localizada
próxima a 1585 cm-1, é induzida pelo estiramento dos átomos de
carbono sp2 e associada com primeiro modo vibracional Raman
E2g permitido de materiais com características grafíticas. Por
fim, a banda D’ está localizada próximo a 1620 cm-1 e é atribuída
defeitos cristalinos na rede grafítica hexagonal como anéis carbônicos com
diferentes quantidades de átomos(ALBERS et al., 2019; CLARAMUNT et al.,
2015; FERRARI, 2007). A presença das cinco bandas indica que a camada de
carbono formada possuí características de uma rede grafítica hexagonal
sp2(G) com elevado grau de desordem
(ID/IG>1) induzida por defeitos de borda(D*), no
plano basal(D), moléculas funcionalizadas(D”) e anéis carbônicos com
diferentes quantidades de átomos(D’). Estes dados indicam que uma camada com
maior desordem é obtida quando se utiliza CTAB, sua atuação como agente de
superfície e sua longa cadeia carbônica podem contribuir para a maior
desordem observada. Por fim o comportamento magnético foi determinado,
Figura 2(C). As amostras apresentam comportamento ferromagnético do tipo
mole com aumento na abertura da curva de histerese e redução da magnetização
de saturação conforme menor tamanho das NP(NiBr2
<CTAB<NH4Br), efeito este decorrente da nanoescala(CAIZER, 2016).
Foram obtidos valores de magnetização de saturação de 88, 120 e 134
emu.g-1, remanência de 12, 9 e 7 emu.g-1 e
coercividade de 320, 210 e 145 Oe.
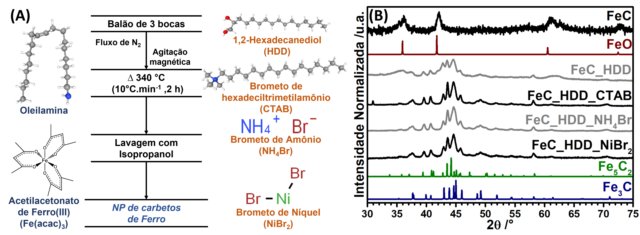
(A)Reagentes empregados e esquema resumo do procedimento de síntese. (B) Difratograma de raios X de todas as amostras.
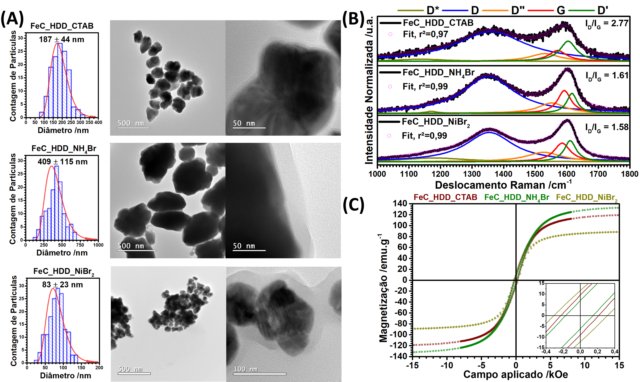
(A)Distribuição de tamanhos e micrografias de transmissão, (B)Espectro Raman e (C)Comportamento magnético das amostras sintetizadas com íons brometo.
Conclusões
Nanopartículas esferoidais de Fe5C2 e Fe3C foram sintetizadas via decomposição térmica do precursor metálico acetilacetonato de Ferro(III), em meio de Oleilamina e induzida for diferentes fonte de íons brometo (brometo de Hexadeciltrimetilamônio, brometo de Amônia e brometo de Níquel). Ajustes no sistema com agentes redutores e íons brometos tornam-se necessários devido a características intrínsecas do precursor metálico empregado, o agente redutor 1,2-Hexadecanodiol foi efetivo na redução do metal e a presença de íons brometo mostrou-se essencial para a estabilização da fase carbeto. A adição de pequena quantidade de íons Ni(II), via brometo de Níquel, levou ao menor tamanho de partículas(83±23nm) devido à sua ação na etapa de nucleação, enquanto o uso do brometo de Hexadeciltrimetilamônio mostrou efeito similar sobre o tamanho(187±44nm), mas devido ao seu efeito como agente de superfície. O sal brometo de Amônia não obteve um bom desempenho no controle do tamanho das partículas(409±115nm) apesar de induzir a formação da fase carbeto. As NP possuem uma camada de revestimento de carbono de características de rede hexagonal grafítica com elevado grau de desordem induzida por defeitos de borda, no plano basal, molécula funcionalizadas e anéis carbônicos com diferentes quantidades de átomos. Todas as NP apresentaram comportamento ferromagnético do tipo mole com elevada magnetização de saturação, os efeitos da nanoescala sobre o comportamento magnético são evidenciando pela redução da magnetização de saturação e maior abertura da curva de histerese conforme menor diâmetro médio das partículas.
Agradecimentos
Ao Instituto de Química de São Carlos da Universidade de São Paulo (IQSC-USP) , à FAPESP, à CAPES e ao CNPq (processo 130476/2018-8) pela infraestrutura e bolsa concedida.
Referências
ALBERS, R. F. et al. A general one-pot synthetic strategy to reduced graphene oxide (rGO) and rGO-nanoparticle hybrid materials. Carbon, [s. l.], v. 143, p. 73–84, 2019. Available at: https://doi.org/10.1016/j.carbon.2018.10.087
BARANOV, D. et al. Purification of Oleylamine for Materials Synthesis and Spectroscopic Diagnostics for trans Isomers. Chemistry of Materials, [s. l.], v. 31, n. 4, p. 1223–1230, 2019. Available at: https://doi.org/10.1021/acs.chemmater.8b04198
BECK, W. et al. Formation Mechanism via a Heterocoagulation Approach of FePt Nanoparticles Using the Modified Polyol Process. The Journal of Physical Chemistry C, [s. l.], v. 115, n. 21, p. 10475–10482, 2011. Available at: https://doi.org/10.1021/jp201830m
BORDET, A. et al. Magnetically Induced Continuous CO 2 Hydrogenation Using Composite Iron Carbide Nanoparticles of Exceptionally High Heating Power. Angewandte Chemie International Edition, [s. l.], v. 55, n. 51, p. 15894–15898, 2016. Available at: https://doi.org/10.1002/anie.201609477
BORDET, A. et al. Water-Dispersible and Biocompatible Iron Carbide Nanoparticles with High Specific Absorption Rate. research-article. ACS Nano, [s. l.], v. 13, n. 3, p. 2870–2878, 2019. Available at: https://doi.org/10.1021/acsnano.8b05671
CAIZER, C. Nanoparticle Size Effect on Some Magnetic Properties. In: ALIOFKHAZRAEI, M. (org.). Handbook of Nanoparticles. Cham: Springer International Publishing, 2016. p. 475–519. Available at: https://doi.org/10.1007/978-3-319-15338-4_24
CARBON. In: CHEMISTRY OF THE ELEMENTS. [S. l.]: Elsevier, 1997. p. 268–327. Available at: https://doi.org/10.1016/B978-0-7506-3365-9.50014-6
CLARAMUNT, S. et al. The Importance of Interbands on the Interpretation of the Raman Spectrum of Graphene Oxide. The Journal of Physical Chemistry C, [s. l.], v. 119, n. 18, p. 10123–10129, 2015. Available at: https://doi.org/10.1021/acs.jpcc.5b01590
COD - CRYSTALLOGRAPHY OPEN DATABASE. [S. l.], [s. d.]. Available at: http://www.crystallography.net/cod/. Acesso em: 26 ago. 2021.
FERRARI, A. C. Raman spectroscopy of graphene and graphite: Disorder, electron-phonon coupling, doping and nonadiabatic effects. Solid State Communications, [s. l.], v. 143, n. 1–2, p. 47–57, 2007. Available at: https://doi.org/10.1016/j.ssc.2007.03.052
FIÉVET, F. et al. The polyol process: a unique method for easy access to metal nanoparticles with tailored sizes, shapes and compositions. Chemical Society Reviews, [s. l.], v. 47, n. 14, p. 5187–5233, 2018. Available at: https://doi.org/10.1039/C7CS00777A
GOLDSCHMIDT, H. J. Interstitial Alloys. Boston, MA: Springer US, 1967. Available at: https://doi.org/10.1007/978-1-4899-5880-8
GREENWOOD, N. N.; EARNSHAW, A. (org.). Carbon. In: Chemistry of the Elements. Second Edied. [S. l.]: Elsevier, 1997. p. 268–327. Available at: https://doi.org/10.1016/B978-0-7506-3365-9.50014-6
HONG, S. Y. et al. A new synthesis of carbon encapsulated Fe 5 C 2 nanoparticles for high-temperature Fischer–Tropsch synthesis. Nanoscale, [s. l.], v. 7, n. 40, p. 16616–16620, 2015. Available at: https://doi.org/10.1039/C5NR04546K
HUNTER, R. J. Foundations of Colloid Science. 2nd ed.ed. Oxford ; New York: Oxford University Press, 2001. ISSN 09277757.
JUNG, H.; THOMSON, W. J. Dynamic X-Ray Diffraction Study of an Unreduced Iron Oxide Catalyst in Fischer-Tropsch Synthesis. Journal of Catalysis, [s. l.], v. 139, n. 2, p. 375–382, 1993. Available at: https://doi.org/10.1006/jcat.1993.1033
KOSOLAPOVA, T. Y. Carbides. Boston, MA: Springer US, 1995. Available at: https://doi.org/10.1007/978-1-4684-8006-1
LACROIX, L.-M. et al. Stable Single-Crystalline Body Centered Cubic Fe Nanoparticles. Nano Letters, [s. l.], v. 11, n. 4, p. 1641–1645, 2011. Available at: https://doi.org/10.1021/nl200110t
LAI, X. et al. The high-pressure anisotropic thermoelastic properties of a potential inner core carbon-bearing phase, Fe7C3, by single-crystal X-ray diffraction. American Mineralogist, [s. l.], v. 103, n. 10, p. 1568–1574, 2018. Available at: https://doi.org/10.2138/am-2018-6527
LI, S. et al. Fe5C2 nanoparticles as low-cost HER electrocatalyst: the importance of Co substitution. Science Bulletin, [s. l.], v. 63, n. 20, p. 1358–1363, 2018. Available at: https://doi.org/10.1016/j.scib.2018.09.016
LI, S. et al. Iron Carbides: Control Synthesis and Catalytic Applications in CO x Hydrogenation and Electrochemical HER. Advanced Materials, [s. l.], v. 31, n. 50, p. 1901796, 2019. Available at: https://doi.org/10.1002/adma.201901796
MEFFRE, A. et al. A Simple Chemical Route toward Monodisperse Iron Carbide Nanoparticles Displaying Tunable Magnetic and Unprecedented Hyperthermia Properties. Nano Letters, [s. l.], v. 12, n. 9, p. 4722–4728, 2012. Available at: https://doi.org/10.1021/nl302160d
MOURDIKOUDIS, S.; LIZ-MARZÁN, L. M. Oleylamine in Nanoparticle Synthesis. Chemistry of Materials, [s. l.], v. 25, n. 9, p. 1465–1476, 2013. Available at: https://doi.org/10.1021/cm4000476
NAGAKURA, S. Study of Metallic Carbides by Electron Diffraction Part III. Iron Carbides. Journal of the Physical Society of Japan, [s. l.], v. 14, n. 2, p. 186–195, 1959. Available at: https://doi.org/10.1143/JPSJ.14.186
PARK, E. et al. Characterization of phases formed in the iron carbide process by X-ray diffraction, mossbauer, X-ray photoelectron spectroscopy, and raman spectroscopy analyses. Metallurgical and Materials Transactions B, [s. l.], v. 32, n. 5, p. 839–845, 2001. Available at: https://doi.org/10.1007/s11663-001-0071-1
SELVARAJAN, P. et al. Potential of Raman spectroscopy towards understanding structures of carbon-based materials and perovskites. Emergent Materials, [s. l.], v. 2, n. 4, p. 417–439, 2019. Available at: https://doi.org/10.1007/s42247-019-00052-6
SHEN, Y. Carbothermal synthesis of metal-functionalized nanostructures for energy and environmental applications. Journal of Materials Chemistry A, [s. l.], v. 3, n. 25, p. 13114–13188, 2015. Available at: https://doi.org/10.1039/C5TA01228G
STEPHENS, F. A.; WILLIAMSON, D. L.; HAGER, J. P. Monitoring iron carbide production from iron ore by quantitative Mössbauer spectroscopy. Nuclear Instruments and Methods in Physics Research Section B: Beam Interactions with Materials and Atoms, [s. l.], v. 76, n. 1–4, p. 354–356, 1993. Available at: https://doi.org/10.1016/0168-583X(93)95236-X
VARANDA, L. C.; JAFELICCI, M. Self-Assembled FePt Nanocrystals with Large Coercivity: Reduction of the fcc-to-L1 0 Ordering Temperature. Journal of the American Chemical Society, [s. l.], v. 128, n. 34, p. 11062–11066, 2006. Available at: https://doi.org/10.1021/ja060711i
WEZENDONK, T. A. et al. Controlled formation of iron carbides and their performance in Fischer-Tropsch synthesis. Journal of Catalysis, [s. l.], v. 362, p. 106–117, 2018. Available at: https://doi.org/10.1016/j.jcat.2018.03.034
YANG, C. et al. Fe 5 C 2 Nanoparticles: A Facile Bromide-Induced Synthesis and as an Active Phase for Fischer–Tropsch Synthesis. Journal of the American Chemical Society, [s. l.], v. 134, n. 38, p. 15814–15821, 2012. Available at: https://doi.org/10.1021/ja305048p
YANG, Z. et al. Modulating the phases of iron carbide nanoparticles: from a perspective of interfering with the carbon penetration of Fe@Fe 3 O 4 by selectively adsorbed halide ions. Chemical Science, [s. l.], v. 8, n. 1, p. 473–481, 2017. Available at: https://doi.org/10.1039/C6SC01819J
YU, J. et al. Iron carbide nanoparticles: an innovative nanoplatform for biomedical applications. Nanoscale Horizons, [s. l.], v. 2, n. 2, p. 81–88, 2017. Available at: https://doi.org/10.1039/C6NH00173D


