CATALISADOR A BASE DE ÓXIDO DE MANGANÊS (MnO2) PARA OXIDAÇÃO ELETROQUÍMICA DE BENZENO
- Home
- Trabalhos
ÁREA
Físico-Química
Autores
Alves, I.C.B. (UFMA) ; dos Santos, J.R.N. (UFMA) ; Marques, A.L.B. (UFMA) ; Marques, E.P. (UFMA)
RESUMO
A oxidação eletroquímica é considerada como uma das mais importantes alternativas, para degradação de BTX, por ser um método ambientalmente correto. Este trabalho mostra o estudo do comportamento eletroquímico do benzeno usando eletrodo de ECV/MnO2. Os estudos de voltametria cíclica indicam que o benzeno é oxidado em meio ácido (H2SO4 0,5 M) em +1,8 V (E vs Ag/AgCl|KClsat) em um processo de difusão controlada. O processo de eletrólise foi realizado utilizando a Cronoamperometria aplicando potencial de +2 V durante 1 h. O acompanhamento da degradação do benzeno foi realizando por meio de Uv-Vis, na qual foi possível determinar que o eletrodo de carbono vítreo modificado com MnO2 mostrou-se eficiente com 99,2% do benzeno degradado após 1h.
Palavras Chaves
Benzeno; Degradação eletroquímica; Óxido de manganês
Introdução
A preservação do meio ambiente é uma das grandes questões que o mundo enfrenta, ao lado do progresso tecnológico, porque as atividades humanas contribuem para o aumento dos níveis de poluição causados por compostos orgânicos. A proteção do meio ambiente e da saúde humana impõe desenvolvimento de estratégias eficazes para redução da emissão global de VOCs. A contaminação de solos e águas subterrâneas por compostos orgânicos voláteis é, em grande parte, oriunda dos derivados de petróleo em postos de combustíveis. Se destacam como contaminantes de origem orgânica os BTX (benzeno, tolueno, etilbenzeno e xileno). E, apesar dos grandes vazamentos acidentais de petróleo serem potencialmente preocupante, segundo Tiburtius et al (2005) a principal fonte de contaminação está relacionada aos pequenos e contínuos vazamentos de combustível em postos de distribuição favorecidos pelo envelhecimento dos taques de estocagem. No Maranhão, região úmida, este fato é, particularmente preocupante. Em termos de BTX o benzendo é o mais tóxico (MA, et al., 2021). De acordo com a portaria 518/04 do Ministério da Saúde, os valores máximos permitidos para os BTX em água para consumo humano são: 5 µg L-1 para o benzeno, 170 µg L-1 para tolueno, 200 µg L-1 para o etilbenzeno e 300 µg L-1 para os xilenos, o menor valor para benzeno se deve ao fato de que o mesmo é o mais nocivo à saúde humana (MINISTÉRIO DA SAÚDE, 2004). Com base nesses achados, o presente trabalho visa contribuir com os estudos sobre a necessária degradação do benzeno, quando presente no meio ambiente, através de sua oxidação em eletrodo de ECV/MnO2.
Material e métodos
O óxido de manganês foi sintetizado por meio do método sol-gel. 3 g de MnCl2 foram dissolvidos em etilenoglicol (50 mL) sob agitação a 40 °C. A solução foi aquecida até 80°C para formação do gel, após o que o gel foi agitado a temperatura ambiente por 2h e seco a 150°C. Em seguida o pó é moído e aquecido a 600 °C por 3 h, a uma taxa de aquecimento de 5°C/min. Antes da modificação, a superfície do eletrodo de carbono vítreo (ECV) foi polida com suspensão de alumina 0,05 µm. 5,0 mg de MnO2 foram suspensos em 1 mL água contendo 0,5% de Nafion. A suspensão foi dispersa usando agitação ultrassônica por 30 min. Uma alíquota de 10 µL desta dispersão foi depositado na superfície do eletrodo GC. em seguida, o eletrodo modificado foi levado ao dessecador para secagem a vácuo. Os experimentos eletroquímicos (Voltametria Cíclica (VC) e Cronoamperometria) foram realizados em uma célula convencional de três eletrodos utilizando um potenciostato modelo PGSTAT 302 da Metrohm. Um eletrodo de carbono vítreo (Ageom = 0,07 cm2) modificado com óxido de manganês, AgǀAgClǀKClsat e um fio de platina, foram utilizados como eletrodos de trabalho, referência e auxiliar, respectivamente. Todos os experimentos foram realizados em um ambiente com temperatura controlada (25 °C). A VC foi realizada em uma solução 0,5 mol L-1 H2SO4, com uma taxa de varredura de 50 mV s-1. Os experimentos de eletrólise do benzeno foram realizados utilizando a cronoamperometria com potencial fixo em +2,0 V por 1 h. O acompanhamento da decomposição do benzeno foi realizado por meio do Espectrofotômetro UV-Vis Thermo Fisher Scientific.
Resultado e discussão
Para otimizar as melhores condições de trabalho, realizou-se vários ensaios
eletroquímicos, em diferentes eletrólitos suportes (tampão BR, tampão acetato,
Na2SO4 e H2SO4 em diferentes concentrações 0,1, 0,5 e 1 mol L-1). Sendo a
melhor resposta para oxidação do benzeno em termos (Ip) e (Ep¬), foi
encontrada utilizando H2SO4 0,5 mol L-1. De acordo com o voltamograma na Fig.
1, o potencial de oxidação do benzeno ocorre aproximadamente em 1,8 V,
mostrando assim uma excelente resposta em termos energéticos utilizando o
eletrodo ECV/MnO2. Na literatura, os autores conseguiram potencial de oxidação
de +1,8 V utilizando Ag/CNT (CESARINO, et al., 2013).
O potencial adequado para eletrólise foi determinado por meio do estudo
cronoamperométrico aplicando diferentes Ep (1,6, 1,7, 1,8, 1,9 e 2 V) durante
120 s. Verificou-se por meio desse estudo que o Ep adequado para realizar a
eletrólise é +2V, pois, dentre os potenciais estudados apresentou maior
corrente, além disso tendo em vista que o potencial de oxidação do benzeno
estudado na Fig. 1 foi 1,8 V, aplicando +2V nos garante a completa oxidação do
benzeno. Após a realização deste estudo realizou o processo de oxidação do
benzeno, durante 1 hora, sendo que a cada 15 minutos foi realizado o
acompanhamento por UV-vis, onde nos permitiu determinar a porcentagem de
degradação do benzeno no meio estudado tal como mostra a Fig. 2 levando em
consideração a absorbância em 253,62 λ(nm). Por meio deste acompanhamento
constatou que o eletrodo conseguiu degradar o benzeno com eficiência de 99,82
%.
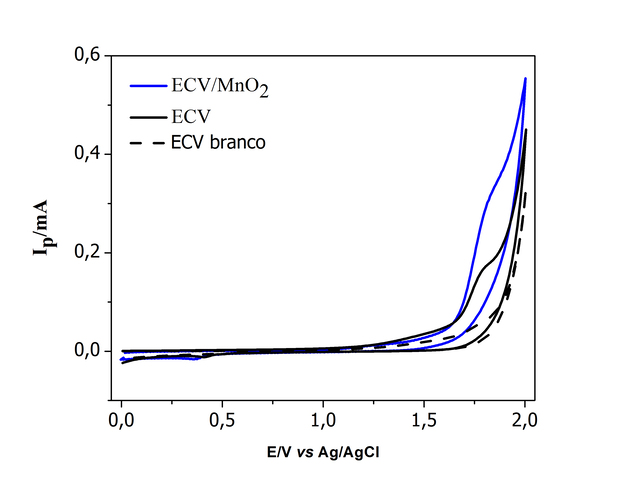
VC em diferentes eletrodos ECV, ECV/MnO2 na presença de benzeno (3 x 10-3 mol L-1) em H2SO4 0,5 mol L-1 com v = 50 mV s-1.
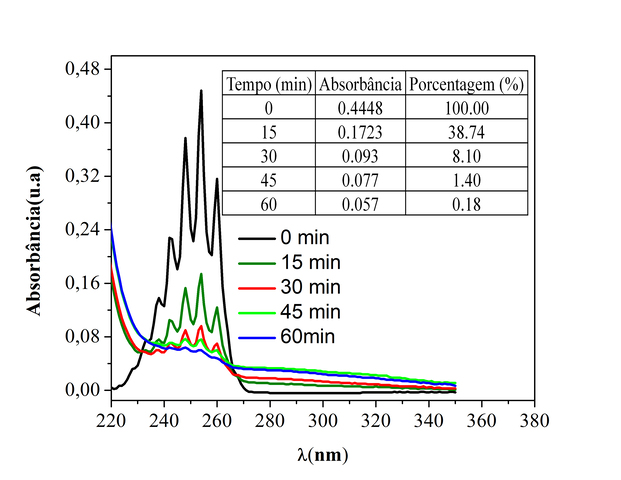
UV-vis do benzeno em diferentes tempos, iniciando 3 x10-3 mol L-1 Ep = +2 V por 1 hora.
Conclusões
Uma metodologia alternativa para a degradação eletroquímica do benzeno foi proposta por meio deste estudo. Sendo possível determinar que o eletrodo de carbono vítreo modificado com MnO2 é uma alternativa viável e eficiente para degradação do benzeno nas condições propostas. A alta atividade catalítica do MnO2, comprovado por meio dos ensaios eletroquímicos garantem maior eficiência na degradação do benzeno quando comparado com ECV. Em essência o eletrodo ECV/MnO2, apresenta-se como material alternativo a ser utilizado na área de análise ambienta.
Agradecimentos
CAPES (PROCAD-AM / SCBA 450 88887.200615 / 2018-00], CNPq [PQ 2017, Proc. 310664 / 2017-9], e ANP [1.029 / 2016-ANP-007.639].
Referências
BRASIL. Ministério da Saúde. Portaria MS n 518/2004, Brasília, 26 de março de 2004. p. 266-270.
CESARINO, Ivana et al. Electrochemical degradation of benzene in natural water using silver nanoparticle-decorated carbon nanotubes. Materials Chemistry and Physics, v. 141, n. 1, p. 304-309, 2013.
MA, Dingren et al. Photocatalytic degradation mechanism of benzene over ZnWO4: Revealing the synergistic effects of Na-doping and oxygen vacancies. Chemical Engineering Journal, v. 405, p. 126538, 2021.
TIBURTIUS, Elaine Regina Lopes et al. Degradação de BTXs via processos oxidativos avançados. Química Nova, v. 28, n. 1, p. 61-64, 2005.


