Emprego de bentonita como suporte sólido para a síntese de chalconas em microondas
- Home
- Trabalhos
ÁREA
Química Ambiental
Autores
Rosa, M. (UNIOESTE) ; Costa, L.H.F.M. (UNIOESTE) ; Lobo, V.S. (UTFPR)
RESUMO
Este projeto teve como objetivo a síntese de vários derivados chalcônicos pelo método de Claisen-Schmidt, empregando radiação de microondas e bentonita como suporte sólido. Foram empregados como suporte a bentonita nativa (BENT), a submetida a tratamento térmico (BENTT) e a modificada com íons K+ (BENTK). Os melhores rendimentos foram obtidos quando foram empregadas BENTT e BENTK. Análises por técnicas espectroscópicas (FTIR), difratométricas (DRX) e termogravimétricas (TGA e DSC) mostram que houve diminuição do espaçamento basal para a BENTT e BENTK. Os resultados mostram a potencialidade do emprego de bentonita como suporte para síntese orgânica em microondas.
Palavras Chaves
química verde; Claisen-Schmidt; argilas
Introdução
A partir dos trabalhos pioneiros de Gedye et al. (1986) e Giguere et al. (1986), que reportaram a utilização da radiação de micro-ondas como fonte de aquecimento em reações orgânicas, o número de trabalhos relatados na literatura cresceu quase exponencialmente na segunda metade da década de 80 e na década de 90, e ainda hoje continua sendo uma área de interesse. Os benefícios mais comuns da utilização da radiação de micro-ondas são: - reações muito mais rápidas, freqüentemente na escala de poucos minutos; - alto grau de pureza dos produtos, devido principalmente ao curto tempo de residência em altas temperaturas; - rendimentos geralmente melhores, obtidos em tempos menores e com produtos mais puros. O equipamento mais popular e barato para síntese orgânica é o forno de micro-ondas doméstico, porém este equipamento, por ser um equipamento multi- modo, apresenta a desvantagem da distribuição não homogênea da energia dentro da cavidade, gerando pontos de hot e cold spots, ou seja, o aquecimento não é uniforme. Atualmente no mercado já são encontrados equipamentos monomodos (single mode) especialmente desenhados para fins sintéticos. Nestes equipamentos obtém-se forças de campo muito mais intensas o que resulta em aquecimentos mais rápidos. Por outro lado, este rápido aquecimento torna as reações realizadas na presença de solventes menos seguras. Assim o desenvolvimento de metodologias reacionais isentas de solventes (solvent-free methodologies) tem efeito positivo, pois tornam as reações mais limpas, seguras e fáceis de fazer (Loupy, 2004). Essas reações podem ser realizadas utilizando suportes minerais sólidos, tais como montmorilonita, bentonita, alumina, sílica e etc, que absorvem radiação de micro-ondas e transferem para o meio reacional e ainda podem ser reciclados para outras reações. Nestas situações o isolamento do produto pode ser conseguido simplesmente pela eluição deste com um solvente apropriado. Bentonita (ou bentonite) é uma designação genérica para uma mistura de argilas muito utilizada na produção de porcelanas e também em tratamentos estéticos. Ela pode ser definida como uma rocha constituída essencialmente por um argilomineral montmorilonítico cuja fórmula química geral é Mx(Al4- xMgx)Si8O20(OH)4. Possui partículas de tamanho médio de 0,5 m e formato de placas ou lâminas (Silva & Ferreira, 2008). A bentonita mais comum é a bentonita cálcica, porém outros tipos, contendo sódio, potássio, ferro e alumínio, também podem ser encontradas. A sua estrutura lamelar permite a inclusão de outras moléculas ou íons em seus interstícios, habilitando as bentonitas atuarem como catalisadores para as mais variadas reações. As benzilidenoacetofenonas (1,3-difenil-prop-2-enonas), mais conhecidas como chalconas, são compostos comumente encontrados na natureza e facilmente obtidos pela clássica reação de condensação aldólica de Claisen-Schmidt, que requer, além da cetona e do aldeído, um meio fortemente básico. Estruturalmente as chalconas são cetonas α,β-insaturadas, que apresentam dois anéis aromáticos interligados por três carbonos com diversas ramificações em seus anéis arométicos. As ramificações dos anéis podem produzir uma diversificação tanto na funcionalidade quanto na intensidade de ação das atividades biológicas do composto.Por exemplo, um medicamento comercial da classe das chalconas utilizado para problemas de ordem digestiva é a metochalcona, quimicamente denominada 4-metoxifenil-3-(2,4- dimetoxifenil)-2-propenona. Este fármaco é distribuído na Itália e na Espanha pelos nomes comerciais de Megalip® e Neocolan® como colerético, cuja função é estimular a secreção de bile pelos hepatócitos (Buzzi, 2007). O trabalho da Navarini et al. (2009), estudou a sensibilidade de células de melanoma (B16F10) frente às diversas chalconas, avaliando-se o efeito citotóxico. Os resultados mostraram que algumas chalconas sintetizadas, derivadas do 3,4-metilenodioxibenzaldeído ou do composto, apresentaram efeito citotóxico, induzindo à morte da célula de melanoma. Este efeito identifica estes compostos como potenciais antitumorais. Por estas razões a síntese e o estudos de novos derivados chalcônicos é de grande interesse científico e comercial. Entretanto as condições empregadas para a sua síntese demandam a manipulação de reagentes que, além de perigosos, são potenciais poluidores do meio ambiente. Logo o desenvolvimento de novas metodologias sintéticas que sejam mais ambientalmente amigáveis ao meio ambiente são de vital interesse.
Material e métodos
OBTENÇÃO DOS SUPORTES SÓLIDOS A modificação da bentonita com íons K+ (BENTK) foi baseada no artigo Bautista et al.(2002). Resumidamente consistiu na suspensão de 1g de bentonita nativa (BENT) em 20 mL de 2-propanol, sendo em seguida a esta adicionada, lentamente e sob agitação constante, uma solução de 0,003 mol de KF em 10 mL de 2-propanol. A agitação foi mantida por mais 4 horas à temperatura ambiente após a adição da solução de KF. O pó obtido foi seco a 110 oC por 5 horas em forno mufla. O sólido obtido foi moído em gral para se obter um pó fino. A bentonita com tratamento térmico (BENTT) foi preparada aquecendo-se cerca de 5g de BENT em forno mufla a 110ºC por 5 horas, depois moída em gral para se obter um pó fino. SÍNTESE DA CHALCONA Em um béquer, pesou-se 3,429 mmol acetona aromática (acetofenona ou derivados), 3,6008 mmol aldeído aromático e 0,5 g de BENT ou modificada. Adicionou-se o etanol como solvente, sendo somente a quantidade necessária para homogeneizar a mistura. Em seguida, a reação foi aquecida em forno de microondas de 700W de potência máxima, por 4 minutos. Após o resfriamento do sólido submetido ao aquecimento por microondas, foi adicionado um pequeno volume de um solvente orgânico (diclorometano ou clorofórmio) e foi submetido ao ultrassom por 5 minutos para a total solubilização dos produtos e material não reagido do suporte sólido, em seguida foi filtrado para remover a argila. O extrato orgânico foi submetido a uma cromatografia em camada delgada (CCD) para se verificar a pureza do produto. Como eluente (fase móvel) foi empregada uma mistura de hexano e acetato de etila na proporção 1:1. Quando necessário uma etapa de isolamento do produto, evidenciado pelo aparecimento de mais de uma mancha na CCD, foi efetuada uma cromatografia em coluna (CC) empregando-se os mesmos solventes da análise por CCD, porém em proporções variadas. O rendimento da reação foi calculado a partir do produto não purificado. CARACTERIZAÇÃO DO CATALISADOR Fez-se a caracterização dos catalisadores, BENT, BENTK e BENTT, por técnicas espectroscópicas, difratométricas e térmicas. ESPECTROSCOPIA DE INFRAVERMELHO COM TRANSFORMADA DE FOURIER (FTIR): As analise de FTIR foram realizadas utilizando um espectrofotômetro (Perkin- Elmer 1600), com técnica de pastilha de KBr, com faixa de varredura de 4000 cm-1 a 400 cm-1. DIFRAÇÃO DE RAIO X (DRX):As medidas de DRX foram obtidas utilizando um difratômetro (DRX-D2 Phaser, Bruker), com 2θ variando de 5º a 80º, com velocidade de varredura de 2º/min e passo de leitura de 0,02º. ANÁLISE TERMOGRAVIMÉTRICA (TGA) e CALORIMETRIA EXPLORATÓRIA DIFERENCIAL (DSC OU dTGA): As analises termogravimétricas foram realizadas usando um analisador térmico (TGA- STA 6000, Perkin Elmer), com tipo de atmosfera de gás N2, com vazão de 20 mL/min, razão de aquecimento de 10 ºC/min e faixa de temperatura de 30 a 900 ºC. O DSC foi obtido a partir da derivada da curva de TGA, registrando-se a dTGA da massa em relação a temperatura (dm/dT)
Resultado e discussão
Comparando-se os espectros de FTIR das bentonitas (Figura 1A) observa-se que
a intensidade das bandas de OH livre e OH associado da água, entre 3000 e
3700 cm-1, e 1632 cm-1, respectivamente, diminuem com a modificação com íons
K+ e ainda é menos intensa na argila com tratamento térmico. Essa diminuição
na intensidade das respectivas bandas indica que a bentonita está menos
hidratada.
Uma vez que a modificação da bentonita resultou na redução de moléculas de
água nas galerias da mesma, pode-se dizer que a presença dos íons K+
resultou em uma maior atração das camadas, reduzindo o número de moléculas
nas lamelas, havendo maior possibilidades de acomodação das moléculas nos
interstícios da bentonita, na síntese das chalconas, aumentando o seu
desempenho, como pode-se visualizar nos rendimentos obtidos. Entretanto,
como a intensidade das bandas de OH na argila tratada termicamente são ainda
menores, o melhor desempenho do catalisador pode ser graças ao processo de
desidratação da argila, e assim, também dando maior espaço nas galerias para
o englobamento de moléculas na síntese.
A análise que pode ser feita dos difratogramas (Figura 1B) é o espaçamento
basal característico da montmorilonita. Quando ambas são comparadas
observam-se diferenças no espaçamento basal de 5 a 10º, correspondente pico
da montmorilonita. Dito isso, observa-se que o espaçamento basal da BENT é
bem maior do que as das argilas modificada e tratada termicamente. Também se
observa que o difratograma da argila modificada e com tratamento térmico se
sobrepõem, não havendo, aparentemente, diferenças nos espaçamentos basais no
pico referente a montmorilonita. Tais diferenças indicam que houve
modificação na estrutura da BENT. Pode-se associar esta alteração no
difratograma à incorporação dos íons K+ nos interstícios das lamelas da
bentonita. Porém como também houve mudanças na estrutura da argila com
tratamento térmico, pode-se atribuir o melhor desempenho do catalisador a
desidratação, já que tanto a BENTK e a BENTT passaram por tratamentos
térmicos.
Foram sintetizadas oito chalconas utilizando-se três derivados de
acetofenona e três derivados de benzaldeído, empregando-se como catalisador
a BENT, BENTK ou a BENTT e tempo de radiação de 4 minutos. Após o work up da
reação os rendimentos foram calculados e estão apresentados na Tabela 1
abaixo. Comparando-se os rendimentos obtidos neste trabalho com os
rendimentos verificados na literatura observa-se de maneira geral que eles
foram inferiores aos relatados, com somente uma exceção (entrada 3). Todos
os procedimentos consultados empregavam o método clássico de síntese, ou
seja, em fase líquida na presença de base e aquecimento prolongado, ao
contrário do nosso que ocorreu em fase sólida, com o mínimo de solvente e
aquecimento por período de tempo reduzido, o que pode ser uma explicação
para os menores rendimentos relatados.
Comparando-se os rendimentos obtidos com os suportes preparados, BENT e
BENTK, observa-se que, com poucas exceções (entradas 3, 5, 7 e 8), estes
foram comparáveis. Desta forma não se pode afirmar que a modificação com
íons K+ leva a obtenção de um catalisador mais eficiente do que a argila
nativa em todas as situações.
No processo de modificação da bentonita com íons K+ é realizada uma etapa de
tratamento térmico para a secagem do catalisador, procedimento este que não
foi realizado para a BENT. Esta etapa é responsável pela perda de
água, não só de hidratação como de adsorção, e consequentemente causa a
diminuição do espaçamento basal da argila, como demonstrado pelos
difratogramas.
Com objetivo de se verificar se esta modificação foi a responsável pelo
melhor desempenho do catalisador BENTK nas reações 3, 5, 7 e 8, foi
realizado um tratamento térmico da BENT para se obter uma bentonita
com as mesmas características difratométricas da BENTK, obtendo-se então a
BENTT, e esta foi testada como catalisador numa reação de síntese da
chalcona.
Assim, fez-se um teste comparativo da BENTT com a BENT e a BENTK, efetuando-
se a síntese com das chalconas que geraram o melhor resultado de rendimento.
Ao realizar a síntese da chalcona 3, 5, 7 e 8 com BENTT obteve-se um
rendimento de 74%, 66%, 61% e 40% os quais são inferiorres ao rendimento
obtido com a BENT e BENTK, com exceção da chalcona 5, onde o rendimento com
a BENTT é 10% a mais com que a BENT. Estes resultados são um indicativo de
que a incorporação de íons K+ nos interstícios da bentonita pode levar à
obtenção de catalisadores a base de bentonita mais eficientes.
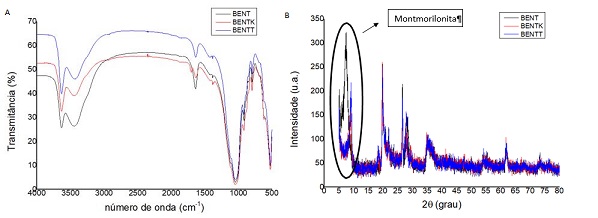
A-Espectro de FTIR da BENT, BENTK e BENTT obtidos na forma de discos de KBR, empregando- se a faixa de 400cm-1 a 4000 cm-1;B-DRX da BENT (linha preta),
Tabela 1-Derivados sintetizados, rendimentos obtidos e rendimentos relatados na literatura para a síntese das chalconas empregando-se BENT e BENTK
Conclusões
Apesar dos rendimentos obtidos pelo método empregando bentonita e microondas terem sido, em sua maioria, inferiores daqueles relatados na literatura obtidos pelo método clássico (presença de solvente e aquecimento convencional), o método relatado apresenta potencialidade, pois o tempo empregado nas reações (4 min) foi consideravelmente inferior ao método usual. Portanto empregando-se tempos maiores pode-se chegar a rendimentos comparáveis. Em relação ao uso da bentonita como suporte verificou-se que a bentonita submetida ao tratamento térmico (BENTT) e a com inclusão de íons K+ (BENTK) apresentaram rendimentos superiores aqueles obtidos com a bentonita nativa (BENT). Comparando-se o rendimento obtido quando empregou-se BENTK com aqueles obtidos quando empregou-se BENTT, observou-se que os primeiros sempre foram superiores ao segundo, evidenciando que a substituição dos íons Na+ e Ca2+ ne bentonita nativa por íons K+ aumentou o poder catalítico desta argila para a reação em tela.
Agradecimentos
Os autores agradecem ao CNPq, pela bolsa de IC de LHFMC, à Fundação Araucária pela bolsa de IC de FM e à CAPES pelo auxilio financeiro pelo PROAP
Referências
1) AWAD, R. et al. Síntese de chalconas com potencial atividade biológica para a doença de alzheimer. In: 57º CONGRESSO BRASILEIRO DE QUÍMICA, 2017, Gramado, Rio Grande do Sul, Brasil; 2) BAUTISTA, F. M. et al. Study on dry-media microwave azalactone synthesis on different supported KF catalysts: influence of textural and acid–base properties of supports. JCS Perkin Trans., v. 12, p. 1961-2164, 2002; 3) BUZZI, F.C., Síntese de novas moléculas com potencial terapêutico: imidas cíclicas,chalconas e compostos relacionados. 2007. Tese (Doutorado em Química) - Programa de Pós-graduaçâo em Química, Universidade Federal de Santa Catarina, Florianópolis, 2007; 4) DIAZ, G. & BURKE, V. Synthesis of Tyrosinase Inhibitors: Designing Chalcones. 2009. Saint Mary’s College of California Summer Research / Department of Chemistry. Disponível em: <https://www.stmarys-ca.edu/sites/default/files/attachments/files/DiazGabrielleFinalReport.pdf>. Acesso em: 24 ago. 2018; 5) GEDYE, R. et al. The use of microwave ovens for rapid organic synthesis. Tetrahedron Lett. (1986), 27, 279; 6)
GIGUERE, R. J. et al. Application of commercial microwave ovens to organic synthesis. Tetrahedron Lett. (1986) 27, 4945; 7) LOUPY, A. Solvent-free microwave organic synthesis as an efficient procedure for green chemistry. C. R. Chimie (2004), 7, 103; 8) Navarini, A. L. F. et al. Hydroxychalcones induce apoptosis in B16-F10 melanoma cells via GSH and ATP depletion. Eur. J. Med. Chem. (2009), 44, 1630; 9) SILVA, A. R. V. & FERREIRA, H. C. Argilas bentoníticas: conceitos, estruturas, propriedades, usos industriais, reservas, produção e produtores/fornecedores nacionais e internacionais. Rev. Elet. Mater. Proc. (2008), 3, 26.


