Autores
Vargas-gutierrez, A. (UNIVERSIDAD NACIONAL DE INGENIERÍA) ; Vega-chacón, J. (UNIVERSIDAD NACIONAL DE INGENIERÍA) ; Horn, M. (UNIVERSITY OF KASSEL) ; Carlos-salazar, M. (UNIVERSIDAD NACIONAL DE INGENIERÍA)
Resumo
La realización de este trabajo busca desarrollar y evaluar la síntesis de
poliácido aspártico (PAA) y aminodextrano (AMD) así como su evaluación en la
preparación de películas para su posterior uso en la liberación de fármacos. Se
sintetizó poliácido PAA mediante el proceso de hidrólisis alcalina, así como
también AMD a partir de la modificación química del dextrano con 1,6-
hexametilendiamina. Posteriormente se realizó la caracterización mediante las
técnicas de espectroscopía de infrarrojo (FTIR), cromatografía de exclusión por
tamaño (SEC) y determinación del porcentaje de grupos amino de AMD. Finalmente se
prepararon películas de PAA/AMD usando el método de moldeo por evaporación de
solvente.
Palavras chaves
Poli Ácido Aspártico; Aminodextrano; películas poliméricas
Introdução
La administración de fármacos es un amplio campo de investigación en el cual se
ha desarrollado nuevos sistemas con la finalidad de aumentar la eficiencia
terapéutica y reducir los efectos secundarios. Entre los sistemas de
administración de fármacos, aquellos basados en películas poliméricas son
prometedores y vienen siendo utilizados en distintos tratamientos dado que
permiten una incorporación eficaz del fármaco y pueden superar algunas de las
limitaciones de la liberación controlada.
Uno de los polímeros más utilizados para elaborar estos sistemas es el PAA por
ser biodegradable, biocompatible y soluble en agua. La presencia de grupos
débilmente ácidos en su estructura le otorga un carácter responsivo, haciendo
que se liberen protones en respuesta a una variación en el pH, provocando un
cambio conformacional macromolecular. Por su parte, el dextrano también viene
siendo muy utilizado, ya que su alto contenido de grupos hidroxilo reactivos le
otorga la facilidad de modificarse para formar conjugaciones de diferentes
moléculas y películas funcionales mediante reticulación con agentes funcionales
adicionales, teniendo al AMD entre sus principales polímeros modificados porque
disminuye la toxicidad de los fármacos y posee una alta estabilidad en pH
ácido o básico beneficiando la conjugación fármaco polímeros.
Este estudio busca contribuir con el desarrollo de la administración de
fármacos, usando películas de PAA/AMD con una matriz responsiva al pH dado que
estos polímeros mejoran la farmacocinética y la biodistribución del agente
activo.
Material e métodos
Síntesis de poliácido aspártico.
Una mezcla de ácido L-aspártico y ácido fosfórico 10:1 (p/p) a 200 °C en
atmósfera de nitrógeno durante 4 horas. El polímero obtenido fue lavado con
metanol y agua desionizada, posteriormente fue secado a temperatura ambiente en
un desecador por 24 horas. La PSI obtenida fue disuelta en una solución de NaOH
1 mol L-1 y agitada durante 3 horas a temperatura ambiente. Finalmente, la
solución fue dializada en agua desionizada por 24 horas y secada por
liofilización.
Síntesis de aminodextrano.
El dextrano (Dex) fue disuelto en una solución buffer de sodio (pH 6,5) y
oxidado con NaIO4 durante 10 minutos, en oscuridad, agitada 2,5 horas a
temperatura ambiente y se dializó por 20 horas con agua desionizada. La solución
obtenida fue enfriada hasta 8 °C, se adicionó 1,6-hexametilenodiamina y se agitó
por 1,5 horas en baño hielo. Posteriormente se agregó NaBH4 en solución de NaOH
y agitada por 10 minutos. Por último, se mantuvo en agitación durante 3 horas,
se dializó por 24 horas y liofilizó.
Caracterización de polímeros.
La espectroscopía infrarroja (FTIR) de los polímeros fue obtenida por el método
ATR en el rango de 4000 - 400 cm-1. La masa molecular fue evaluada por la
cromatografía de exclusión por tamaño (SEC). La determinación del porcentaje de
grupos amino se calculó utilizando una adaptación del método conductimétrico, el
AMD fue disuelto en HCl, se adicionó NaCl y se homogenizó. La solución fue
titulada conductimétricamente con NaOH.
Obtención de películas de PAA/AMD.
Una solución acuosa de AMD 5% (p/v) fue mezclada con una de PAA 5% (p/v). La
solución polimérica obtenida fue transferida a un molde de teflón y fue secada
en la estufa por el tiempo necesario a 50 °C.
Resultado e discussão
El resultado del análisis por SEC mostró que la masa molecular promedio en
número (Mn) del PAA fue 4,579 kDa y la masa molecular promedio en peso (Mw) fue
6,511 kDa. La polidisperidad para este sistema fue de 1,422. Los espectros FTIR
correspondiente al PAA muestran picos principales en la banda en 3258 cm-1, que
corresponde a los estiramientos N-H del grupo amida y
O-H del grupo COOH. La banda 1569 - 1516 cm-1 corresponde al estiramiento C=O de
los grupos amida. Con la información reportada, se pudo corroborar que
efectivamente se ha obtenido polisuccinimida y, consecuentemente, poliácido
aspártico
Los resultados del análisis por SEC mostraron que la masa molecular promedio en
número (Mn) del AMD fue 4,260 kDa y la masa molecular promedio en peso (Mw) fue
8,608 kDa. La polidisperidad del AMD fue de 2.021. En la obtención del AMD, los
intermediarios fueron aislados y caracterizados por FTIR (Figura 1). La señal
1642 cm−1 en el espectro de Dex oxidado es característica del estiramiento del
C=O de las unidades de Dex, en la modificación con 1,6-hexametilendiamina, se
observa el ensanchamiento de esa banda y la formación de una banda de menor
intensidad en 1599 cm−1. La gráfica de conductividad vs volumen de titulante
añadido, obtenida de la determinación del porcentaje de grupos amino del AMD,
los resultados de los ensayos se muestran que el porcentaje promedio obtenido es
igual a 6,02%.
En el espectro FTIR (Figura 2) de la película de PAA/AMD. La banda que se
encuentra en 3255 cm-1, que corresponde a los estiramientos N-H del grupo amida
y O-H del grupo COOH. La señal 1576 cm-1 corresponde al estiramiento C=O de los
grupos amida. Estos picos señalados corroboran que la película está conformada
por ambos polímeros en su estructura.
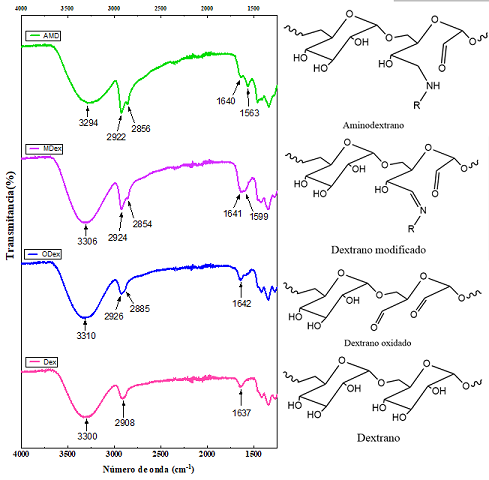
Espectro FTIR de (Dex) dextran0, (ODex) dextran0 oxidada, (MDex) dextrano modificado con 1,6- hexametilenodiamina y (AMD) aminodextrano
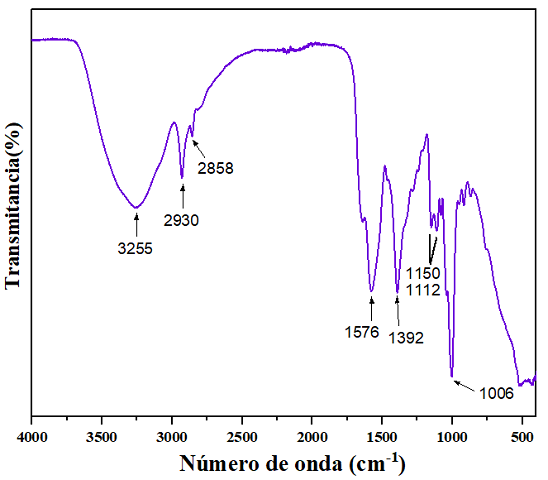
Espectro FTIR de la película de PAA/AMD
Conclusões
Se sintetizaron PAA y AMD, cuyas masas moleculares promedio en número obtenidas
mediante SEC fueron de 4,579 kDa para PAA y 4,260 kDa para AMD respectivamente.
Los espectros FTIR confirmaron la modificación de los polímeros precursores y la
obtención de los polímeros finales. Se resalta la presencia del grupo amino en el
espectro de AMD, donde se obtuvo un valor promedio de 6,02%, lo que indica que
hubo poca cantidad de grupos carbonilos disponibles. Se obtuvieron películas de
PAA/AMD, cuyo espectro infrarrojo corroboró la presencia de los principales grupos
funcionales de cada polímero.
Agradecimentos
Agradecimiento a la Unidad de Investigación de la Facultad de Ciencias de la UNI
por el financiamiento en la realización de este trabajo y a la Universidade
Estadual Paulista por los análisis SEC.
Referências
AHMED, A.; SARWAR, S.; HU, Y.; MUNIR, M. U.; NISAR, M. F.; IKRAM, F.; ASIF, A.; RAHMAN, S. U.; CHAUDHRY, A. A.; & REHMAN, I. U. Surface-modified polymeric nanoparticles for drug delivery to cancer cells. Expert Opinion on Drug Delivery, no 18, 1–24, 2021.
ARIGA, K.; MINAMI, K.; EBARA, M.; & NAKANISHI, J. (2016). What are the emerging concepts and challenges in NANO? Nanoarchitectonics, hand-operating nanotechnology and mechanobiology. Polymer Journal, no 48, 371–389, 2016.
CARLOS-SALAZAR, M. Estudio de liberación controlada de antiocianinas a partir de películas de quitosano despolimerizado y reticulado con tripolifosfato de sodio. Universidad Nacional de Ingeniería, 2013.
FARHOOD, B.; GERAILY, G.; & ABTAHI, S. M. M. A systematic review of clinical applications of polymer gel dosimeters in radiotherapy. Applied Radiation and Isotopes, no 143, 47–59, 2019.
FARRIS, S.; MORA, L.; CAPRETTI, G.; & PIERGIOVANNI, L. Charge density quantification of polyelectrolyte polysaccharides by conductometric titration: An analytical chemistry experiment. Journal of Chemical Education, no 89, 121–124, 2012.
GUNDLOORI, R. V.; SINGAM, A.; & KILLI, N. Nanobased Intravenous and Transdermal Drug Delivery Systems. Applications of Targeted Nano Drugs and Delivery Systems, 551–594, 2019.
KHIZAR, S.; AHMAD, N. M.; AHMED, N.; MANZOOR, S.; HAMAYUN, M. A.; NASEER, N.; TENÓRIO, M. K. L.; LEBAZ, N.; & ELAISSARI, A. Aminodextran Coated CoFe2O4 Nanoparticles for Combined Magnetic Resonance Imaging and Hyperthermia. Nanomaterials, no 10, 2182, 2020.
LI, J.; & MOONEY, D. J. Designing hydrogels for controlled drug delivery, 2016.
LIMA-TENÓRIO, M. K.; PINEDA, E. A. G.; AHMAD, N. M.; AGUSTI, G.; MANZOOR, S.; KABBAJ, D.; FESSI, H.; & ELAISSARI, A. Aminodextran polymer-functionalized reactive magnetic emulsions for potential theranostic applications. Colloids and Surfaces B: Biointerfaces, no 145, 373–381, 2016.
MASOOD, F. Polymeric nanoparticles for targeted drug delivery system for cancer therapy. Materials Science and Engineering: C, no 60, 569–578, 2016.
MOUAZIZ, H.; VEYRET, R.; THERETZ, A.; GINOT, F.; & ELAISSARI, A. Aminodextran containing magnetite nanoparticles for molecular biology applications: Preparation and evaluation. Journal of Biomedical Nanotechnology, no 5, 172–181, 2009.
NARMANI, A.; REZVANI, M.; FARHOOD, B.; DARKHOR, P.; MOHAMMADNEJAD, J.; AMINI, B.; REFAHI, S.; & GOUSHBOLAGH, N. A. Folic acid functionalized nanoparticles as pharmaceutical carriers in drug delivery systems. Drug Development Research, no 80, 404–424, 2019.
PADILLA MONTERO, S. F. (2018). Fabricación de películas poliméricas con adición de pululan para la impresión 2D de tinta modelo como potencial forma farmacéutica de administración bucal, Universidad de Chile, 2018.
PAL, D.; & NAYAK, A. K. Alginates, Blends and Microspheres: Controlled Drug Delivery. Encyclopedia of Biomedical Polymers and Polymeric Biomaterials, 89–98, 2015
PARHIZKAR, E.; DANESHAMOUZ, S.; MOHAMMADI-SAMANI, S.; SAKHTEMAN, A.; PARHIZKAR, G.; OMIDI, M.; & AHMADI, F. Synthesis and in vitro assessment of novel water-soluble dextran-docetaxel conjugates as potential pH sensitive system for tumor-targeted delivery. Journal of Applied Polymer Science, no 134, 45457, 2017.
RONG, F.; TANG, Y.; WANG, T.; FENG, T.; SONG, J.; LI, P.; & HUANG, W. Nitric Oxide-Releasing Polymeric Materials for Antimicrobial Applications: A Review. Antioxidants 2019, no 8, 556, 2019.
UPPUTURI, R. T. P.; KULANDAIVELU, K.; & MANDAL, A. K. A. Nanotechnology-Based Approach for Enhanced Bioavailability and Stability of Tea Polyphenols—A Review. Studies in Natural Products Chemistry, no 50, 399–410, 2016.
VEGA-CHACÓN, J; ARBELÁEZ, M. I. A.; JORGE, J. H.; MARQUES, R. F. C.; & JAFELICCI, M. pH-responsive poly(aspartic acid) hydrogel-coated magnetite nanoparticles for biomedical applications. Materials Science and Engineering C, no 77, 366–373, 2017.
VEGA-CHACÓN, J.; DEBONE PIAZZA, R.; COSTA MARQUES, R. F.; ELAISSARI, A.; & JAFELICCI, M. The influence of pH, hydrolysis and degree of substitution on the temperature-sensitive properties of polyaspartamides. Polymer International, no 68, 88–93, 2019.
YEH, J. C.; YANG, H. H.; HSU, Y. T.; SU, C. M.; LEE, T. H.; & LOU, S. L. Synthesis and characteristics of biodegradable and temperature responsive polymeric micelles based on poly(aspartic acid)-g-poly(N-isopropylacrylamide-co-N,N-dimethylacrylamide). Colloids and Surfaces A: Physicochemical and Engineering Aspects, no 421, 1–8, 2013.
ZEGARRA URQUIA, C. L. Síntesis de un nuevo vehículo polimérico α,β-poli(dl-ácido aspártico) del agente antidiabético oxovanadio(iv), 2012.
ZELIKIN, A. N. Drug releasing polymer thin films: New era of surface-mediated drug delivery. ACS Nano, no 4, 2494–2509, 2010.
ZHANG, G.; YI, H.; & BAO, C. (2021). Stimuli-Responsive Poly(aspartamide) Derivatives and Their Applications as Drug Carriers. International Journal of Molecular Sciences, no 22, 8817, 2021.
















