Autores
Toledo Neira, C. (UNIVERSIDAD DE SANTIAGO DE CHILE) ; Rebolledo, K. (UNIVERSIDAD DE SANTIAGO DE CHILE) ; Mesias, A. (UNIVERSIDAD DE SANTIAGO DE CHILE) ; Lucena, R. (UNIVERSIDAD DE CORDOBA)
Resumo
Los Hidrocarburos Aromáticos Policíclicos (PAHs) son uno de los contaminantes
más comunes y extendidos en el mundo, presentan genotoxicidad y causan daño
ambiental debido a su bioacumulación. En este sentido el solvente eutéctico
profundo (DES) de carácter hidrofóbico [Timol-Lidocaina] ha resultado ser un
buen candidato para la extracción de estos compuestos en matrices tan complejas
y diversas como alimentos de té-café y muestras de orina. La ayuda de la técnica
de microextracción líquido líquido dispersiva es crucial para obtener
metodologías mas rápidas, eficientes y ecoamigables debido a las características
de baja volatilidad y biodegradabilidad de este DES y el bajo consumo de muestra
y solvente orgánico usado. Los resultados resultan ser promisorios con LOD bajo
los 2 µg/L
Palavras chaves
Solventes verdes DES; PAHs; alimentos y orina
Introdução
Los hidrocarburos aromáticos policíclicos (PAHs), son un grupo de moléculas de
alto interés debido a que muestran una naturaleza ambiental altamente lipofílica
[1,2]. Estas moléculas son altamente cancerígenas y genotóxicas, y tienen la
capacidad de migrar largas distancias [3-5]. Actualmente, se sabe que las
principales vías de exposición directa de los humanos son a través del consumo
de cigarrillos [6,7] y alimentos contaminados, lo que en los últimos años ha
sido foco de estudios en que se ha comprobado que los PAHs son absorbidos por
los alimentos principalmente por aire y deposición [6,8], mostrando así estar
presentes en alimentos que han sido expuestos al proceso de secado μg/L que
permiten el contacto directo entre alimentos y productos de combustión. La
presencia de PAHs en los alimentos requiere un seguimiento continuo, rápido y
eficaz. Debido a esto, se están buscando y desarrollando nuevos procesos para la
determinación de HAP que sean amigables con el medio ambiente. Los solventes
eutécticos profundos por su parte, se consideran una clase de líquidos iónicos,
ya que comparten con ellos algunas propiedades como baja volatilidad, alta
capacidad de extracción, alta viscosidad y propiedades ajustables según su
composición química.
En este trabajo se desarrolló una metodología analítica para la determinación de
6 hidrocarburos aromáticos policíclicos cancerígenos en muestras de infusiones
de té y café. La metodología propuesta involucra un procedimiento de
microextracción líquido-líquido dispersivo que utiliza un solvente eutéctico
profundo de baja densidad (DES-DLLME). Después de la extracción, los analitos
finalmente se determinan por HPLC-FLD. Actualmente está en estudio la
determinación de los 6 PAHs y algunos metabolitos en orina.
Material e métodos
Reactivos: Los PAHs estudiados Benzo[a]Antraceno, Criseno, BenzoFluoranteno,
Benzo[k]Fluoranteno, Benzo[a]Pireno y Dibenzo[a,h]Antraceno, se obtuvieron del
Dr.Ehrenstorfer (LGC Standards, Alemania). Para preparar el DES se utilizó
glicerina, fenol, cloruro de colina, timol y lidocaína, todos Sigma-Aldrich
(Merck KGaA, Alemania).
Muestras y DES-DLLME: Diez muestras, de té y café, fueron adquiridas en
supermercados en Santiago de Chile durante el 2021. Las bolsas de té se
prepararon en 200 mL de agua milli-Q a 95 °C, y reposo de 5 min según el
fabricante.El café se preparó con 1 g en 200 mL de agua milli-Q a 95 °C. La
solución de café fría se filtra con Filtro Jeringa 13mm PVDF. Luego se tomaron 8
mL de muestra de café, realizando adición estándar de 1 a 4 mL con PAHs estándar
de 50 μg/L.Para la extracción. Se usaron 8 mL de muestra de té y café, solo las
muestras de café, fueron filtradas con filtro Jeringa 13 mm PVDF Hidrofílico
0,22 m, para separar el particulado. Las muestras fueron llevadas a un tubo de
centrífuga con 300 µL de la solución extractante (DESs:MeCN; 1:1) para el té y
600 para el café. El tubo se agita por 1 min con agitador vortex (DRAGONLAB
Scientific) y se centrifuga a 5500 rpm (Hettich EBA 20) por 10 min para el té y
de 20 min para el café. Finalmente, se aísla los 150 µL de DES, inyectando 20 µL
en HPLC-FLD.
HPLC-FLD: Los análisis se realizaron en un sistema Jasco LC Net II con detector
de fluorescencia (FP-4025) y horno para columna (CO-4061).La columna utilizada
fue de fase inversa ZORBAX Eclipse Plus PAH (4,6x150x3,5) a 40 ºC modo
isocrático MeCN:H2O (84:16) a 1 mL/min y volumen de inyección de 20 μL. Las
longitudes de onda de excitación y emisión fueron 270 y 390 nm para BaA, CHR y
DBahA y 255 y 420 nm para CHR, BbFA y BkFA respectivamente.
Resultado e discussão
Primeramente, se evaluaron tres DES:ChCl-Glicerol, ChCl-fenol y timol-lidocaína,
para la extraccion mediante DLLME. Los DES basados en ChCl fueron descartados
como extractantes ya que no mostraron separación de fases al tiempo del
procedimiento experimental. Se optimizaron los parámetros de: tiempo de
agitación de vórtex, volumen de DES, tiempo de centrifugación y volumen de
muestra. Se probaron 4 proporciones de DES:ACN para evaluar su capacidad de
extracción y se demostró que la extracción óptima se da con la mezcla en partes
iguales de DES:ACN, este fenómeno responde a un proceso físico, donde el agente
dispersante ayuda al DES a interactuar con la matriz acuosa. Para el caso de
muestras de alimentos, se definió un volumen óptimo de mezcla de 300 mL para las
muestras de té y 600 mL para café. La máxima recuperación se obtuvo con un
tiempo de agitación de vórtex de 60 s. El tiempo de centrifugado se definió en
10 min para las muestras de té y 40 min para café, ya que estas últimas
mostraron una mayor emulsión. Para el volumen de muestra se probaron volúmenes
entre 4 y 10 mL, siendo 8 mL el volumen apropiado. La cuantificación se realizó
mediante el calibrado de los 6 analitos de una solución acuosa de trabajo, en un
rango de concentraciones de 2,5 a 500 mg/L-1. Los LOD obtenidos fueron entre
2.02 y 30.8 ng/L-1, llegando a factores de enriquecimiento hasta 90 veces, y los
porcentajes de recuperación varían entre 57 y 94%. Se analizaron 10 muestras
reales de té y café encontrando niveles por sobre los 1.84 y 9.10 mg/L-1, para
las muestras de café se obtuvieron valores entre 0,06 y 2,16 mg/L-1. Finalmente
el método también fue aplicado a determinación de PAHs y sus metabolitos en
orina sintética, obteniendo resultados similiares en cuanto a parámetros
analíticos.
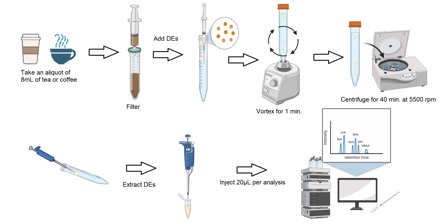
Diagrama esquemático de la microextracción propuesta con DES-DLLME y HPLC-FLD para la determinación de PAHs en té y café
Conclusões
Se desarrolló un método analítico de microextracción líquido-líquido dispersiva
utilizando solventes eutécticos profundos hidrofóbicos como extractante y el uso
de HPLD-FLD, para la detección rápida y eficiente de 6 PAHs cancerígenos.
Se obtuvo un método simple, rápido y ecoamigable. El método fue aplicado a 10
muestras favoreciendo una detección rápida y eficiente de PAHs presentes en té y
café.
Las muestras analizadas se encuentran por encima de los límites recomendados para
este tipo de sustancias químicas cancerígenas establecidos por entes reguladores
como la UE o USEPA.
Agradecimentos
Los autores agradecen PROYECTO FONDECYT nº 1201978 por financiamiento. A.M
agradece a beca POSTDOC-DICYT,022142TN-POSTDOC, Vicerrectoría de Investigación,
Desarrollo e Innovación, Usach. K.R agradece a la beca VIPO USACH.
Referências
1-Plaza-Bolaños P, Frenich AG, Vidal JL. J Chromatogr A. 2010 Oct 8;1217(41):6303-26. doi: 10.1016/j.chroma.2010.07.079. Epub 2010 Aug 12. PMID: 20828703.
2-F. Fazaieli, M.R. Afshar Mogaddam, M.A. Farajzadeh, B. Feriduni, A. Mohebbi, J. Sep. Sci. 43 (2020) 2393–2400.
3-Jalili, Vahid, Barkhordari, Abdullah and Ghiasvand, Alireza. "Liquid-phase microextraction of polycyclic aromatic hydrocarbons: A review" Reviews in Analytical Chemistry, vol. 39, no. 1, 2020, pp. 1-19.
4-Hendryx M, Wang S, Romanak KA, Salamova A, Venier M. Environ Pollut. 2020;257:113501.10.1016/j.envpol.2019.113501 cancerigeno
5-He Y, Yang C, He W, Xu F. Sci Total Environ 2020, 723:138099. https://doi.org/10.1016/j.scitotenv.2020.138099 cancerigeno
6-M. Behzadi, Ecotoxicol. Environ. Saf. 208 (2021), 111568.
7-Shi Y, Wu H, Wang C, Guo X, Du J, Du L. Food Chem. 2016;199:75–80.10.1016/j.foodchem.2015.11.137
8-Thomas Wenzl, Rupert Simon, Elke Anklam, Juliane Kleiner, TrAC Trends in Analytical Chemistry, Volume 25, Issue 7, 2006, Pages 716-725, ISSN 0165-9936, https://doi.org/10.1016/j.trac.2006.05.010.
















