Autores
Silva Junior, J.H. (UFRN) ; Medeiros, L.G. (UFRN) ; Silava, K.A. (UFRN) ; Castro, P.S. (UFRN)
Resumo
Este trabalho descreve uma metodologia alternativa para fabricação de eletrodos
utilizando hastes de grafite retiradas de pilhas comuns (tipo AAA) e sua
sistematização através da impressão 3D. Essa nova tecnologia apresenta-se como
uma alternativa bastante atrativa devido à sua simplicidade, robustez,
versatilidade, baixo custo e diversidade de materiais para impressão. Os
espelhos foram projetados e impressos para formação de um molde de silicone. As
hastes foram conectadas a um fio de cobre e encapsuladas utilizando resina
epóxi. Os eletrodos foram caracterizados utilizando voltametria cíclica com
resposta equiparável aos eletrodos comerciais. Além disso, o fator
reprodutibilidade também foi avaliado evidenciando possibilidade de utilização
em aulas didáticas e em pesquisas científicas.
Palavras chaves
impressão 3D; eletrodo de grafite; fabricação de eletrodos
Introdução
A busca por novos materiais e inovação nas metodologias de fabricação são
atualmente um dos principais desafios encontrados no desenvolvimento de sensores
eletroquímicos. A impressão 3D é uma tecnologia de manufatura aditiva baseada no
princípio da construção por deposição em camadas, que se destaca dos demais
processos de construção pela maior economia de matéria-prima, maior velocidade
de produção, grande capacidade de personalização e de confecção de estruturas
complexas e bem definidas - especialmente, internas (SILVA JUNIOR, 2021). Desta
forma, nos últimos anos, essa nova tecnologia vem se destacando como ferramenta
essencial para diversas aplicações interessantes na área de eletroanalítica.
Assim, diferentes configurações de eletrodos vêm sendo introduzidos com
aplicações em análises clínicas, ambientais, farmacêuticas e forenses (OLIVEIRA
et. al., 2020; CAMPOS JANEGITZ et al., 2022; MUNIZ et al. 2022).
Os dispositivos eletroquímicos, tais como pilhas e baterias estão amplamente
presentes no cotidiano da vida moderna. Ainda que úteis, estes aparelhos
apresentam grande risco ambiental devido sua composição composta de elementos
potencialmente poluentes, tais como zinco, manganês, níquel, cádmio, chumbo e
mercúrio. Apesar de diversos incentivos e campanhas de descarte de forma segura,
uma grande quantidade de pilhas ainda são descartadas diariamente em aterros
sanitários e terrenos baldios (AFONSO et al., 2003). Segundo dados da Associação
Brasileira da Indústria Elétrica e Eletrônica (ABINEE) são produzidos
anualmente, apenas no Brasil, cerca de 800 milhões de pilhas, sendo 80% destas
pilhas secas do tipo zinco e carbono e 20% de pilhas alcalinas. Embora haja
conhecimento da quantidade produzida de pilhas e baterias no país, não há
estimativas da porção destes dispositivos que são recolhidos e reciclados, ou
descartados de forma correta (CONTE, 2016).
Atualmente existem alguns processos químicos nos quais os metais de
pilhas e baterias conseguem ser reciclados, como por exemplo na recuperação de
zinco e manganês de pilhas através de eletrólise (FERELLA; DE MICHELIS; VEGLIÒ,
2008). No entanto, a reutilização do cátodo de grafite presente nestes
dispositivos também apresenta relevância, uma vez que este material de carbono
tem potencial para ser empregado como sensor eletroquímico (SIQUEIRA SANTOS et
al., 2018).
O carbono pode apresentar-se de diferentes formas, tais como: fibras, pó,
folhas, espumas e compósitos. Estas formas possuem propriedades atrativas em
diferentes aplicações eletroquímicas, uma vez que o material citado apresenta
boa condutividade elétrica. Umas das formas elementares mais comuns do carbono é
o grafite. O grafite possui estrutura de carbono em planos de camadas, e pode
ser encontrado de forma natural ou ser sintetizado a partir de precursores
industriais como coque de petróleo, pixe e negro de fumo. (BAIO; RAMOS;
CAVALHEIRO, 2014). Assim, os cátodos das pilhas comuns possuem como fonte de
carbono o grafite natural de alta pureza que podem ser empregados como material
condutor para fabricação de sensores eletroquímicos utilizando a impressão 3D
como alternativa para confecção de moldes de silicone para encapsulamento em
resina epóxi.
Material e métodos
Reagentes
Os reagentes utilizados na caracterização e análise dos eletrodos foram
reagentes do tipo PA (para análise) da marca Sigma-Aldrich. As soluções foram
preparadas com água destilada purificada através de sistema de osmose reversa
(Permution–E. J. Krieger & Cia LTDA, 18 MΩ cm-1). Os reagentes
utilizados foram: hidróxido de potássio, hexacianoferrato (III) de potássio,
cloreto de potássio, ácido fosfórico, dihidrogenofosfato de sódio e padrão de
cafeína (C8H10N4O2- Dinâmica). A
solução estoque de cafeína foi preparada no dia de sua utilização, a fim de se
evitar possíveis oxidações químicas.
Equipamentos e medidas eletroquímicas
Para limpeza dos eletrodos de grafite foi utilizado o ultrassom Unique
UltraCleaner 1450. As medidas eletroquímicas foram realizadas em um
potenciostato Metrohm Autolab PGSTAT302N utilizando uma célula eletroquímica de
três eletrodos: eletrodo de trabalho – eletrodo de grafite confeccionado,
eletrodo de referência – Ag/AgCl/KCl(3M) de fabricação própria e eletrodo
auxiliar – fio de platina.
Fabricação do eletrodo de carbono grafite utilizando impressão 3D
Os eletrodos foram confeccionados utilizando hastes de grafite retiradas de
pilhas comuns exauridas (zinco-carbono, tipo AAA). Em seguida, as hastes foram
lixadas (lixa d’água #600) e lavadas com água destilada. O método de fabricação
utilizado foi o de encapsulamento em resina epóxi (Redelease 2004) a partir de
moldes de silicone que foram confeccionados via impressão 3D seguindo os
parâmetros para impressão da peça espelho para confecção dos moldes em
silicone: Material = PLA (⌀ 1,75 mm); Temperatura do extrusor = 245 °C; Altura
de camada = 0,2 mm; Densidade de preenchimento = 60 %; Padrão de preenchimento =
Cúbico; Velocidade de impressão = 40 mm/s.
Verificação do funcionamento dos eletrodos de carbono grafite
Os testes para verificação do funcionamento dos dispositivos fabricados foram
realizados utilizando uma solução contendo uma espécie mediadora conhecida,
ferricianeto de potássio (K3[Fe(CN)6]), de concentração 10 mmol/L em KCl 100
mmol/L como eletrólito suporte. Logo, foram executadas análises voltamétricas
utilizando voltametria cíclica para verificação dos resultados e sua comparação
com os dados descritos na literatura.
Resultado e discussão
Fabricação de eletrodos de grafite utilização impressão 3D
A Figura 1 descreve as etapas para construção do eletrodo. Para a construção dos
moldes, uma peça espelho com a forma dos eletrodos (Etapa 1) foi desenhada
digitalmente utilizando a plataforma Tinkercad, e impressa em PLA (Ácido
polilático, 3DFila) utilizando uma impressora 3D modelo Ender 3, fabricada pela
Creality. O molde de silicone foi preparado vertendo na peça impressa uma
mistura homogênea de borracha e catalisador (Redelease) na proporção mássica de
100:3, respeitando o tempo de cura de 24 horas até o desmolde (Etapa 2 e 3).
Para compor o condutor dos eletrodos, a haste de grafite foi cortada em
fragmentos de 5 mm, e com o auxílio de uma mini retifica, um pequeno orifício
foi feito em uma das faces de cada fragmento, onde foi conectado (por pressão)
um pedaço de fio rígido de cobre (⌀ 1mm) (Etapa 4). Os conjuntos haste-fio foram
inseridos no molde de silicone, onde foi vertido uma mistura homogênea de resina
epóxi e catalisador (2:1) (Etapa 5). O tempo de cura respeitado foi de 24 horas,
quando então os eletrodos foram retirados e lixados (lixa d’água #600) até a
obtenção de uma superfície plana e rente ao corpo de epóxi, com o condutor de
disco de grafite exposto (Etapa 6).
Caracterização dos eletrodos de grafite
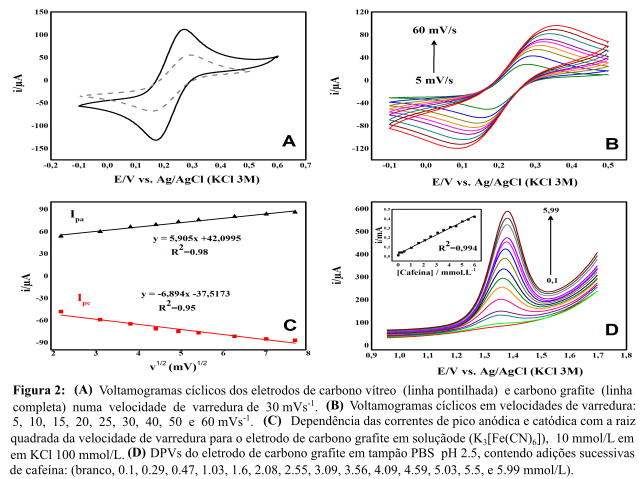
A resposta voltamétrica do eletrodo de carbono grafite fabricado foi comparada à
de um eletrodo de carbono vítreo comercial como mostra a Fig. 2A. Para isso, a
técnica de voltametria cíclica foi utilizada empregado uma solução de
K3[Fe(CN)6] 10 mmol/L em KCl 100 mmol/L com velocidade de varredura de 30 mV/s.
Pode-se observar que há diferenças nos valores de corrente e potencial de picos
anódico e catódico. Desta forma, a maior corrente observada para o eletrodo de
carbono grafite evidencia uma maior área eletroativa de sua superfície. A
aproximação entre os picos no voltamograma associado ao eletrodo de carbono
grafite reflete uma maior transferência de elétrons nas reações de oxidação e
redução que ocorrem na interface entre a superfície do eletrodo de trabalho e a
solução eletrolítica. A diferença entre os picos no eletrodo de carbono vítreo
foi de aproximadamente 0,137 V, enquanto que no eletrodo de carbono grafite foi
de 0,098 V.
Cálculo da área eletroativa do eletrodo de grafite
A técnica de voltametria cíclica foi utilizada para determinar a área
eletroativa do eletrodo de grafite fabricado neste trabalho. Para tal, uma série
de medidas foram realizadas modificando as velocidades de varredura a fim de
correlacionar os picos anódicos e catódicos e determinar através da Equação de
Randles-Sevick (Equação 1) a área efetiva do eletrodo de carbono grafite.
ip = 2,69×105n(3/2)AD(1/2)Cv
(1/2) Equação 1
onde, ip é a corrente de pico anódico (μA), n é o número de elétrons
transferidos (n = 1 for K3[Fe(CN)6], A é a área do eletrodo (cm2), C
é a concentração das espécies oxidadas (mol/cm3), D é o coeficiente
de difusão das espécies oxidadas (D = 7,6 × 10-6 cm2/s
para K3[Fe(CN)6] e v é a velocidade de varredura (V/s).
As Fig. 2B e 2C mostram respectivamente as respostas eletroquímicas obtidas
através das medidas voltamétricas em diferentes velocidades de varredura (5 - 60
mV/s) e as equações da reta obtidas para o processo anódico e catódico.
Utilizando a equação 1 foi possível determinar que a área eletroativa do
eletrodo de grafite fabricado corresponde à 0,796 cm2. Observando as
equações das retas obtidas podemos afirmar que o transporte de massa foi
controlado por difusão. Além disso, podemos observar que à medida em que a
velocidade de varredura foi aumentando, houve um pequeno deslocamento nos
potenciais de pico anódico e catódico das correntes. Essa mudança na região dos
picos pode ser explicada pela adsorção ou formação da dupla camada na superfície
do eletrodo de grafite, uma vez que devido sua porosidade, a superfície do
eletrodo revela uma reação redox quase reversível.
Reprodutibilidade de fabricação dos eletrodos
No tocante à reprodutibilidade, foram analisados 5 eletrodos de grafite
confeccionados de forma similar. Utilizando voltametria cíclica e uma solução de
K3[Fe(CN)6] 10 mmol/L em KCl 100 mmol/L a uma velocidade de varredura de 30 mV/s
obtivemos os dados: Corrente de Pico Anódico(μA) = 94,55; 99,24; 110,57; 99,89;
103,94 com Valor Médio = 101,64 e Desvio Padrão(σ) = 6,00 e Corrente de Pico
Catódico(μA) = -113,54; -115,68; -131,87; -116,33; -123,13 com Valor Médio =
-120,11 e Desvio Padrão(σ) = 7,49.
Levando em consideração a metodologia proposta de fabricação utilizando a
impressão 3D, a reutilização das hastes de pilhas, o contato elétrico entre a
haste e o fio de cobre, e o encapsulamento utilizando resina podemos considerar
podemos considerar que a metodologia artesanal proposta neste trabalho é
bastante reprodutível e pode ser considerada uma alternativa bastante favorável
para laboratórios didáticos e grupos de pesquisa em eletroanalítica. Desta
forma, existe ainda um grande potencial de produção destes eletrodos em larga
escala.
Aplicação do eletrodo de grafite na identificação de cafeína
Dentre as técnicas eletroquímicas disponíveis, a técnica da voltametria de pulso
diferencial - DPV (Differential Pulse Voltammetry) foi a selecionada para
determinar cafeína em amostras produzidas em laboratório. Dessa forma, foram
analisadas soluções contendo concentrações distintas de cafeína em tampão PBS pH
2,5 numa faixa de concentração entre 0,1 e 5,99 mmol/L. Para medição do
analito proposto foram feitas adições consecutivas de volumes pré-fixados da
solução padrão de cafeína 500 ppm. Após a adição da alíquota no sistema e sua
respectiva homogeneização a leitura de sinal em triplicata foi feita utilizando
DPV.
A partir dos picos apresentados pela técnica de DPV, Figura 2D, foi possível
construir uma curva de calibração. Os sinais obtidos na voltametria de pulso
diferencial apresentaram-se na faixa esperada da cafeína, entre 1,3 e 1,4 V
(MARTÍNEZ - HUITLE et al., 2010). A correlação entre as concentrações de cafeína
(mmol/L) e o sinal associado de corrente (mA) produziu um coeficiente de
determinação ótimo (R2=0,994), ou seja, foi possível observar um
comportamento linear do pico de oxidação da cafeína com o aumento da sua
concentração.

Conclusões
O desenvolvimento de novas tecnologias para fabricação de sensores
eletroquímicos busca fomentar a inovação na criação de novos materiais e métodos
alternativos às técnicas tradicionais. Neste cenário, o trabalho desenvolvido
buscou através da utilização do grafite oriundo da reciclagem de pilhas comuns e
por meio da impressão 3D confeccionar eletrodos de carbono grafite apresentando
qualidade analítica e potencial de produção em larga escala.
A impressão 3D para confecção de sensores eletroquímicos dispõe de diversas
vantagens, como por exemplo, sua simplicidade, robustez, versatilidade, além de
apresentar baixo custo e facilidade na aplicação da técnica.
Apesar da matéria prima utilizada ser fruto de reciclagem, quando comparado com
eletrodo de carbono vítreo comercial, o eletrodo de grafite possui correntes de
pico anódica e catódica maiores, além de aproximação dos picos. Fato este
associado à maior área eletroativa do eletrodo, a qual foi calculada e
corresponde à 0,796 cm2.
Através das medidas de reprodutibilidade, o eletrodo de carbono grafite
apresentou uma resposta estável para os diferentes dispositivos testados, com
desvios padrões de 6,0 e 7,49 para os picos anódico e catódico, respectivamente.
Finalmente, o eletrodo de carbono grafite foi aplicado na determinação de
cafeína em diferentes concentrações. Através da técnica de voltametria de pulso
diferencial (DPV) foi possível observar um comportamento linear da oxidação da
cafeína, com o sinal de corrente associado aos picos. A correlação entre os
parâmetros apresentou valor ótimo, R2=0,994.
Agradecimentos
Os autores agradecem à UFRN, ao Laboratório de Eletroquímica Ambiental e Aplicada
(LEAA), a Central Analítica do Instituto de Química-UFRN e ao PIBIC pelo apoio
financeiro.
Referências
AFONSO, J. C. et al. Processamento das pastas eletrolítico de pilhas usadas, Química Nova vol.26 n. 4, agosto, 2003.
BAIO, J.; RAMOS, L.; CAVALHEIRO, É. Construction of a graphite electrode removed from common batteries: DIDACTIC APPLICATIONS. Química Nova, 2014.
CAMPOS JANEGITZ, BRUNO, at al. Different approaches for fabrication of low-cost electrochemical sensors. Current Opinion in Electrochemistry, v. 32, p. 100893, 2022.
CONTE, A. Ecoeficiência, logística reversa e a reciclagem de pilhas e baterias: revisão. Revista Brasileira de Ciências Ambientais (Online), n. 39, p. 124-139, 2016.
FERELLA, F.; DE MICHELIS, I.; VEGLIÒ, F. Process for the recycling of alkaline and zinc–carbon spent batteries. Journal of Power Sources, v. 183, n. 2, p. 805-811, 2008.
MARTÍNEZ-HUITLE, N. SUELY FERNANDES, S. FERRO, A. DE BATTISTI, M.A. QUIROZ. Fabrication and application of Nafion®-modified boron-doped diamond electrode as sensor for detecting caffeine. Diamond & Related Materials. v. 19, 10 th p. 1188–1193, 2010.
MUNOZ, RODRIGO et al. Promising Applications of Additive-Manufactured (3D-printed) Electrochemical Sensors for Forensic Chemistry. Brazilian Journal of Analytical Chemistry - BrJAC (Online), v. 9, p. 79-105, 2022.
MUNOZ, RODRIGO et al. Electrochemical (Bio)Sensors Enabled by Fused Deposition Modeling-Based 3D Printing: A Guide to Selecting Designs, Printing Parameters, and Post-Treatment Protocols, Analytical Chemistry, 94, 17, 6417–6429, 2022
OLIVEIRA, F. M.; MELO, E. I.; SILVA, R. A. B. 3D Pen: A low-cost and portable tool for manufacture of 3D-printed sensors. Sensors and Actuators B: Chemical, v. 321, 128528, 2020.
SILVA JUNIOR, J. Fabricação e validação de acessórios para espectroscopia e espectroeletroquímica usando impressão 3D para investigações de processos dinâmicos interfaciais e de superfícies. Mestrado—[s.l.] Universidade Federal do Rio Grande do Norte, 2021.
SIQUEIRA SANTOS, C. et al. Carbon Graphite Obtained of Zinc-Carbon Exhausted Batteries Applied as Electrode in Electrochemical Sensors. Revista Virtual de Química, v. 11, n. 1, p. 275-296, 2019.
















