Autores
Junior, P.S.B. (UFS) ; Sobrinho, A.A.S. (UFS) ; Dorea, H.S. (UFS)
Resumo
Através da técnica UA-MSPD (dispersão da matriz em fase sólida assistida por
ultrassom) com GC-MS e GC-FID, fez-se um planejamento fatorial 2³ para
desenvolver o método e achar os melhores valores para os parâmetros massa do
adsorvente, volume do eluente e tempo do ultrassom, assim obtidos: 0,5 g de
sílica, 4 mL de Acetona/Hexano e 480s de ultrassom, a recuperação variou de 59,79
a 89,7% com média de 75,23% e um RSD de 12,45%, exceto o naftaleno que teve uma
recuperação de 15,89%, utilizando o GC-MS foi feito uma curva analítica onde
obteve-se bons resultados como LOQ (Limite de Quantificação) e de exatidão. o
limite de quantificação para o GC-MS foi de 50ug/Kg, no GC-FID teve uma
sensibilidade boa para os 16 compostos
Palavras chaves
UA-MSPD; HPA; sedimento
Introdução
O estuário do Rio Sergipe é de grande importância para a população sergipana
onde cerca de 57,4% habitam em áreas de influência da bacia, além disso, o rio
percorre 3,673 km² nascendo na Serra Negra divisa de Sergipe com a Bahia
atravessando o Estado, as águas são utilizadas na zona rural para agricultura
estendendo-se até a zona urbana, entretanto. A existência de lixões e centros
industriais próximo ao rio influência a qualidade da água. (BARBOSA et al.,
2019).
A zona estuaria é a transição entre a água do mar e do rio. Segundo DE SOUSA
MOURA (2016) Os estuários são importantes regiões de interação entre o
continente e o oceano, com a mistura da água salgada com a doce gera uma
variação da qualidade da água: variação na salinidade e instabilidade dos
fatores ambientais do estuário.
Os sedimentos provenientes dos rios e oceanos são utilizados para análise
geoquímica, segundo CARVALHO et al., 2020, a matéria orgânica (MO) e poluentes
orgânicos tendem a associar-se às partículas finas. Portanto, o conhecimento da
composição química do sedimento é de grande importância para determinar a
contaminação dele.
Os Hidrocarbonetos Policíclico Aromáticos (HPA) são compostos orgânicos tóxicos
e cancerígenos provindos da pirólise ou combustão incompleta de compostos
orgânicos (LEE, kwan., 2014), existem diversos compostos caracterizados como
HPA. Entretanto, a USEPA (Agência de proteção Ambiental dos Estados Unidos)
classificou 16 desses compostos como. (USEPA, 2017)
Na química analítica verde existe inúmeros métodos de análise para compostos
como os HPA, dentre esses métodos é válido destacar o MSPD (Matriz solid phase
dispersion), sua capacidade de acoplar outras técnicas para aumentar a
eficiência, como também a possibilidade de reduzir etapas são pontos positivos
desta técnica. Ela funciona com aplicação de uma força mecânica sobre a matriz e
o adsorvente fazendo uma mistura homogênea, após a homogeneização, a mistura é
levada para uma coluna e eluida para retirar o analito do adsorvente.
(WIANOWSKA, Dorota., 2019)
A técnica UA-MSPD (Ultrassom assisted – Matriz solid phase dispersion) utiliza-
se de banho ultrassônico ou de uma sonda para aumentar a eficiência da extração
na fase solido liquido. (CAPRIOTTI, Anna Laura., 2015)
Material e métodos
Materiais utilizados: Mix de HPA com concentração de , Acetona HPLC, Hexano
HPLC, Diclorometano HPLC, Florisil®, Sílica em gel e sulfato de sódio anidro.
Para utilização dos adsorventes houve um tratamento utilizando-se da mufla, o
sulfato de sódio anidro foi calcinado a 400°C por 4horas.E, a Sílica e Florisil®
foram ativados em uma temperatura de aproximadamente 130°C por 12horas.
Equipamento.
Equipamentos utilizados: Balança analítica, ultrassom, rota-evaporador, mufla,
GC-MS (Cromatografia gasosa acoplada a espectrometria de massas) e GC-FID
(Cromatografia gasosa com detector de ionização por chamas).
Planejamento Fatorial.
Foi realizado um planejamento fatorial de 3 elevado a 2, ou seja, 3 fatores e 2
níveis, os fatores foram: Tempo de ultrassom, quantidade de adsorvente e
quantidade de eluente. E, os níveis foram definidos como inferior e superior
Amostragem.
Em fevereiro de 2021 foi realizado a etapa de amostragem, onde foram coletados
16 amostras em pontos diferentes como pode ser vista na figura 1.
Figura 1. Pontos da coleta dos sedimentos, A) Ponto 4 B)Ponto 16 C)Ponto 6 D)
Ponto 5.
Preparo da amostra.
Inicialmente, foi preparado uma solução padrão de HPA intermediaria com
concentração de . A preparação das amostras seguirão os seguintes passos: em um
almofariz colocou-se 0,5 de sedimento seco (liofilizado) e da solução padrão
intermediaria, após alguns minutos, adicionou-se 0,5 ou 1g de sílica em gel, em
seguida, a mistura foi homogeneizada por 2 minutos. Em um frasco com tampa foi
adicionado a amostra-dispersante e 4 ou 8 mL do solvente Acetona/Hexano (1:1),e
o frasco levado ao ultrassom por 90 ou 480s. Posteriomente, uma coluna MSPD foi
preparada com lã de vidro, 0,5 g de sulfato de sódio anidro e 0,5g de Florisil®,
após a preparação da coluna, coletou o sobrenadante da amostra passando na
coluna e eluindo com 3mL de Hexano, por fim, a amostra foi completamente seca no
rota evaporador para proceder a troca de solvente para Diclorometano.
Curva de Calibração.
Utilizando-se da solução padrão intermediaria foram preparados viais com
concentrações diferentes, sendo elas: 25 ppb, 50 ppb, 100pbb, 250pbb, 500ppb e
1000 ppb.
Resultado e discussão
Para a realização da análise foi utilizado um cromatógrafo GCMS-TQ8040 da
Shimadzu, que possui a coluna SH-RTX-5SILMS: 30m comprimento; 0,25 mm de
diâmetro interno; 0,25 µm de espessura de filme (fasé sólida), a rampa de
aquecimento do forno é iniciado a 40 ºC que permanece durante 1 min, em
seguida, o forno volta a aquecer em uma taxa de 20 ºC por minuto até chegar a
150 ºC, que volta a aquecer em uma taxa de 10 ºC por minuto até 220 ºC ,depois,
volta a aquecer a uma taxa de 5 ºC por minuto até 245 ºC, por fim, o forno
aquece a 10 ºC por mim até chegar 300 ºC que permanece durante 7 min. O Hélio
foi usado como gás arraste, grau de pureza (99,995%), volume injetado 1,0 µL,
temperatura do injetor 300 ºC, temperatura da interface 280 ºC, temperatura da
fonte de íons 280 ºC, injeção Splitless, voltagem do detector 70 eV.
GC-FID.
Para a realização da análise foi utilizado um cromatógrafo GC-FID 2010 da
Shimadzu, que possui a coluna DB-5MS: 30 m de comprimento; 0,25 mm de diâmetro
interno; 0,25 µm de espessura de filme (fase sólida), a rampa de aquecimento do
forno é iniciado a 40 ºC que permanece durante 1 min, em seguida, o forno volta
a aquecer em uma taxa de 20 ºC por minuto até chegar a 150 ºC, que volta a
aquecer em uma taxa de 10 ºC por minuto até 220 ºC ,depois, volta a aquecer a
uma taxa de 5 ºC por minuto até 245 ºC, por fim, o forno aquece a 10 ºC por mim
até chegar 300 ºC que permanece durante 7 min, o volume injetado 1,0 µL, em
modo splitless e temperatura do injetor 300 ºC.
Amostragem.
Em cada ponto onde houve a coleta do sedimento foram anotados dados como:
Salinidade, Turbidez, profudindade e localização.Ademais, a medida que a coleta
do sedimento distanciou-se do oceanoa salinidade diminiu, a variação da turbidez
foi de 50 a 115.
Planejamento Fatorial
Com a realização de todos os testes foi possível determinar o teste
com maior eficiência nas recuperações dos HPAs, foram feitas análises através de
gráficos de barras visto na figura 1.
Figura 1.Comparação dos testes.
Com esses dados foi possível perceber dois testes que destacaram-se o 3 e 6, em
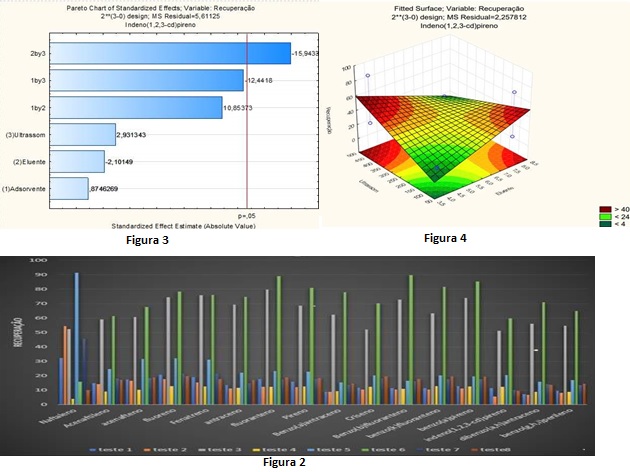
seguida, foi feito gráficos de Pareto (Vide figura 2).
Figura 2 – Gráfico de Pareto – Composto Indeno(1,2,3-cd)pireno.
O gráfico de pareto foi utilizado para analisar se algum fator
foi significativo, no gráfico acima percebe-se que o único fator significativo é
a interação do eluente com o ultrassom, para entender melhor essa interação foi
feito gráfico de superfície de resposta para os compostos e fatores
significativos como pode ser visto na figura 3.
Figura 3 – gráfico de superfície de resposta- Indeno(1,2,3-cd)pireno.
Analisando o gráfico de superfície do indeno(1,2,3-cd)pireno de ultrassom e
eluente, percebeu-se que a recuperação era maior quando possuía menos quantidade
de eluente e mais tempo de ultrassom. Ademais, todos os gráficos de Pareto e
superfície de resposta estão no Anexo 1.
Comparando os dados de recuperação e os gráficos de
superfície de resposta, percebemos a maior recuperação foi obtida quando
utilizamos quantias menores do eluente e adsorvente com um maior tempo de
ultrassom.
Curva de calibração.
Inicialmente, utilizou-se do GC-MS para validar o método, foi feito algumas
curvas de calibração e teste de recuperação com o teste 6, os dados da curva e
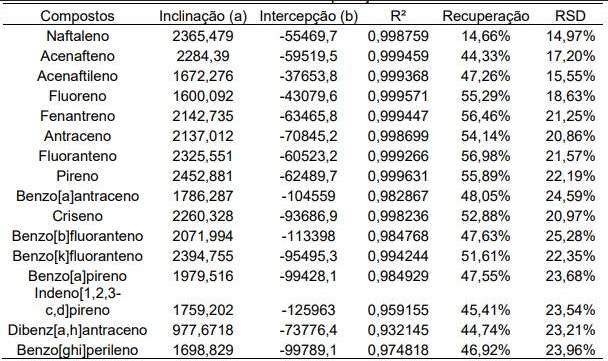
do teste de recuperação podem ser visto na Tabela 1.
Tabela 1. Dados da curva e recuperação GC-MS.
Com a realização da curva de calibração percebeu-se que o equipamento
não estava sensível no momento, foi feito algumas limpezas na coluna para a
melhoria da sensibilidade, Entretanto. Houve um problema onde o equipamento
apresentou defeito e ficou impossibilitado de realizar análises.
Para dar
andamento a pesquisa viu a possibilidade de validar o método utilizando-se do
GC-FID, Inicialmente, houve a necessidade de aprender a utilizar o cromatógrafo
e ajustar os parametros do equipamento, como curva de temperatura, tipo de
injeção e fluxo dos gases, com isso, foi realizado uma injeção com concentração
de 1 ppm para determinar o tempo de retenção de cada composto.
Com o tempo de retenção de cada composto, foi injetado 5 vials com
concentrações de: 50, 100, 150, 250, 500 e 1000 ppb para realizar a curva de
calibração.
Os gráficos utilizados para encontrar os parâmetros inclinação e
intercepção podem ser vistos em anexo.
O equipamento demonstrou sensibilidade com concentrações acima de 50
ppb, Entretanto. Houve uma contaminação na coluna que reduzindo a sensibilidade,
com isso não foi possível obter bons resultados de recuperação.
Conclusões
Com a realização do planejamento fatorial foi possível determinar o melhor teste,
sendo o 6 e, identificar a interação entre eluente, adsorvente e ultrassom,
Inicialmente. Obteve-se uma recuperação entre 59,79% a 89,70% com média de 75,23%
e um RSD <20%, a recuperação para o naftaleno foi de 15,89%. Concluida a etapa de
desenvolvimento partimos para a validação onde .Inicialmente, foi utilizado o GC-
MS conseguimos uma sensibilidade para 10 compostos, exceto para o
Benzo(a)Antraceno, Benzo(b)Fluoranteno, Benzo(a)Pireno, Indeno[1,2,3-c,d]Pireno,
Dibenzo[a,h]Antraceno e Benzo[ghi]Perileno, obtevesse uma recuperação entre
44,33% e 56,98% exceto para o naftaleno que teve 14,66% de recuperação, o limite
de quantificação para o GC-MS foi de 25ppb. Ademais, foi utilizado o GC-FID para
dar continuidade a pesquisa onde conseguimos sensibilidade para os 16 compostos e
um limite de quantificação entre 50 e 100 ppb.
Agradecimentos
Ao Condomínio de Laboratórios da Química (CLQM) pelo uso dos equipamentos GC-MS e
GC/FID.
Referências
BARBOSA, A. M. F. et al. Bacias hidrográficas e os conflitos pelos usos das águas no estado de Sergipe. Confins, n. 40, p. 1–19, 2019.
CARVALHO, Angelo CB et al. Análise espectroscópica da matéria orgânica NO SEDIMENTO superficial da baía de sepetiba, rio de janeiro, brasil. Química Nova, v. 43, p. 552-557, 2020.
CAPRIOTTI, A. L. et al. Recent advances and developments in matrix solid-phase dispersion. TrAC - Trends in Analytical Chemistry, v. 71, p. 186–193, 2015.
DE SOUSA MOURA, Hanna Tereza Garcia; NUNES, Zélia Maria Pimentel. Caracterização sazonal das águas do sistema estuarino do Caeté (Bragança-PA). Boletim do Instituto de Pesca, v. 42, n. 4, p. 844-854, 2016.
LEE, Kwan; LIM, Hyun-Sul; KIM, Heon. A study of the status of exposure to polycyclic aromatic hydrocarbons (PAHs) in relation to its metabolites among workers in a Korean chemical factory. Ciência & Saúde Coletiva, v. 19, p. 4809-4818, 2014.
USEPA. Basics of Green Chemistry. https://www.epa.gov/greenchemistry/basics-green-chemistry#definition, 2017. Acesso em: 24-04-2021.
WIANOWSKA, D.; GIL, M. New insights into the application of MSPD in various fields of analytical chemistry. TrAC - Trends in Analytical Chemistry, v. 112, p. 29–51, 2019.
















