Autores
Alves, R.C. (INSTITUTO NACIONAL DE TECNOLOGIA) ; Freitas, B.P. (INSTITUTO NACIONAL DE TECNOLOGIA) ; Lage, L.S.S. (INSTITUTO NACIONAL DE TECNOLOGIA) ; Novo, A.A. (INSTITUTO NACIONAL DE TECNOLOGIA) ; Ribeiro, L.O. (INSTITUTO NACIONAL DE TECNOLOGIA) ; Jung, E.P. (INSTITUTO NACIONAL DE TECNOLOGIA)
Resumo
O objetivo deste trabalho foi avaliar a extração dos compostos bioativos de S.
officinalis por meio da extração sólido-líquido assistida por micro-ondas
empregando glicerol como solvente. Um delineamento experimental foi usado para
avaliar a influência das variáveis independentes (concentração de glicerol,
temperatura e tempo de extração) sobre as respostas (capacidade antioxidante e
conteúdo de fenólicos totais - CFT). Os resultados indicaram que todas as
variáveis exerceram influência sobre as respostas, com destaque para a
contribuição da temperatura e da concentração de glicerol na solução extratora
(p<0,05). A maior capacidade antioxidante (378 μmol Trolox/g) foi observada no
extrato obtido a 200 °C por 30 min, empregando glicerol 40%.
Palavras chaves
Salvia officinalis; Glicerol; Micro-ondas
Introdução
Originária do mediterrâneo e pertencente à família Labitae, a S. officinalis é
popularmente conhecida por suas propriedades biológicas. Suas folhas são pilosas
e de sabor amargo, possuindo pontas agudas e de coloração cinza-esverdeada
(ALTINDAL; ALTINDAL, 2016). Seu óleo essencial e folhas são utilizados na
indústria alimentícia para dar sabor e aroma a diferentes preparações (WALCH et
al., 2011) e também em formulações farmacêuticas e cosméticas (PINTO et al.,
2007).
Os compostos fenólicos destacam-se entre os componentes não voláteis por
conferirem propriedades bioativas à S. officinalis, tais como a atividade
antioxidante, antimicrobiana, antitumoral, antifúngica, antidiabética e
antiviral (MALEŠ et al., 2022; GHORBANI; ESMAEILIZADEH, 2017). Com base na
crescente exigência de consumidores preocupados com a utilização de produtos
“verdes”, os conservantes/antioxidantes naturais estão cada vez mais sendo
empregados em formulações diversas, atendendo desde o segmento alimentício ao
farmacêutico e cosmético (MAZAUD et al., 2022). Em vista disso, diferentes
processos de extração são avaliados para a obtenção desses compostos bioativos a
partir de matrizes vegetais. Dentre eles, destaca-se a extração assistida por
micro-ondas devido a uma série de vantagens, como a possibilidade de trabalhar
com diversas amostras, baixo consumo energético, reduzido tempo de extração
quando comparado às extrações convencionais e baixo consumo de solvente (BENER
et al., 2019). Alguns solventes são extremamente tóxicos, poluentes ambientais,
inflamáveis, de fontes não renováveis e até mesmo bioacumuláveis (KASHYAP et
al., 2022). Dessa forma, a utilização de solventes verdes em processos de
extração de compostos bioativos tem sido encorajada nas últimas décadas (HASHEMI
et al., 2022).O glicerol é um solvente verde, subproduto da transesterificação
do biodiesel. O expressivo crescimento da indústria de biocombustíveis acarretou
uma produção excedente de glicerol, impulsionando pesquisas voltadas ao estudo
de novas aplicações deste composto (MONTEIRO et al., 2018).
A literatura é bastante rica em trabalhos envolvendo a caracterização química e
a avaliação do potencial antioxidante dos óleos essenciais e também dos extratos
da S. officinalis(BARATTA et al., 1998; PINTO et al., 2007; LÄNGER; MECHTLER;
JURENITSCH, 1996). A recuperação de compostos bioativos da S. officinalis
assistida por micro-ondas foi reportada em apenas dois trabalhos na literatura
(DRAGOVI´C-UZELAC et al., 2012; ZECOVI´C et al., 2017). Entretanto, o uso do
glicerol como solvente verde não foi avaliado. Além disso, não há referência na
literatura quanto à otimização destes processos de extração. Assim, o objetivo
deste trabalho foi avaliar a recuperação de compostos bioativos da S.
officinalis por meio de uma extração sólido-líquido assistida por micro-ondas
empregando o glicerol como solvente verde.
Material e métodos
Material vegetal
Para esse estudo, foi utilizada uma amostra comercial de S. officinalis L.,
adquirida no coméricio do Rio de Janeiro. Todo o conteúdo da embalagem foi
triturado em processador para obtenção de um material homogêneo.
Extração assistida por micro-ondas
A melhor condição de extração sólido-líquido assistida por micro-
ondas foi definida a partir de um planejamento experimental do tipo composto
central rotacional, variando a temperatura, a concentração de glicerol na
solução extratora e o tempo conforme apresentado na Tabela 1. A razão
sólido-líquido foi fixada em 1:20 (m/v). Os ensaios foram realizados em um
micro-ondas MILESTONE, ETHOS 1, no qual os vasos contendo 0,5 g da amostra de
S. officinalis e 10 mL de solvente foram aquecidos. Os extratos obtidos foram
filtrados e armazenados sob congelamento até a realização das análises.
Extração em acetona/água 70% (v/v)
Visando comparar a eficiência de recuperação do processo de extração dos
compostos bioativos por micro-ondas, uma extração exaustiva em acetona 70% foi
realizada, mantendo a mesma razão sólido-líquido, porém sob agitação magnética
200 rpm a 50 °C por 30 minutos. Após as macerações, os extratos foram separados,
combinados e armazenados sob congelamento até a realização das análises de CFT e
capacidade antioxidante.
Conteúdo de Fenólicos Totais (CFT)
As análises de CFT foram realizadas utilizando o reagente Folin-Ciocalteu,
seguindo o método descrito por (SINGLETON; ROSSI, 1965). Para a reação, 250 µL
do extrato filtrado e diluído foi misturado a 1250 µL do reagente Folin-
Ciocalteu a 10% e 1000 µL de uma solução de carbonato de sódio 7,5% (m/v). A
seguir, as amostras foram aquecidas a 50 ºC por 15 minutos. A absorvância foi
medida a 760 nm. Uma curva de calibração foi construída usando o padrão de ácido
gálico com concentrações variando de 11,3 mg/L a 113 mg/L. O CFT foi expresso em
mg de equivalente de ácido gálico/100 g (mg EAG/100 g).
Ensaio DPPH•
O consumo do radical 2,2-difenil-1-picrilhidrazil (DPPH•) pelos extratos foi
determinado de acordo com o método descrito por Hidalgo et al. (2010). Para esta
reação, adicionou-se a 100 µL de cada extrato, 2900 µL da solução de DPPH•
(6×10-5 M em metanol). O tempo de reação foi de 30 minutos a temperatura
ambiente. A seguir, a absorvância foi medida a 517 nm com um espectrofotômetro
usando metanol como branco. A capacidade de consumo do radical DPPH• foi
calculada usando soluções padrão de Trolox com diferentes concentrações,
variando de 80 a 694 µmol. Os resultados foram expressos em µmol Trolox/g.
Análise dos dados
Os dados foram analisados estatisticamente por meio do software Statistica
versão 13 (Dell Inc., Tulsa, OK, USA). Para avaliação da influência das
variáveis independentes sobre as respostas foram construídos os diagramas de
Pareto, considerando um intervalo de confiança de 95%. Análise de variância
(ANOVA) e teste de Tukey foram usados para verificar diferença entre os
resultados.
Resultado e discussão
Na Tabela 1 são apresentados os resultados para o CFT e capacidade antioxidante
dos extratos obtidos em cada condição operacional do delineamento proposto. É
possível notar a influência das variáveis independentes sobre as respostas. O
CFT variou de 1376 a 6120 mg EAG/100 g e a capacidade antioxidante de 97 a 378
µmol Trolox/g.
O ensaio T7 foi o que apresentou o maior valor para a capacidade antioxidante
(378 µmol Trolox/g), enquanto que o ensaio T8 foi aquele com maior CFT (6120 mg
EAG/100 g). Embora a literatura aponte para uma correlação positiva entre o CFT
e a capacidade antioxidante de extratos vegetais, no presente trabalho esse
comportamento não foi observado. Uma vez que a única variável diferente entre os
ensaios T7 e T8 foi o tempo de extração, a redução do potencial antioxidante da
amostra pode estar associada à exposição prolongada dos compostos a temperatura.
Também é importante destacar que o incremento do CFT com o aumento no tempo de
extração entre os ensaios T7 e T8 não alcançou nem 10%, portanto, a condição
operacional do ensaio T7 foi selecionada como a mais promissora para extrair
compostos bioativos dessa matriz.
Na Figura 1 é possível observar a influência das variáveis independentes sobre a
capacidade antioxidante dos extratos, mensurada pelo ensaio DPPH•. Nota-se que
todas as variáveis e as interações entre elas foram significativa (p<0,05).
Entretanto, devem ser destacados os efeitos lineares da temperatura, da
concentração de glicerol e do tempo de extração sobre essa resposta. A
temperatura e a concentração de glicerol na solução extratora exerceram um
efeito positivo sobre a capacidade antioxidante, ou seja, o incremento dessas
variáveis independentes aumentou o potencial antioxidante dos extratos.
Entretanto, como os efeitos quadráticos dessas variáveis independentes também
foram significativos, isso mostra que existe um limite máximo para esse
comportamento. Já para o tempo, o efeito foi oposto, corroborando os resultados
discutidos. O gráfico de Pareto para o CFT é mostrado na Figura 1. Nesse caso,
apenas os efeitos lineares da temperatura e da concentração de glicerol foram
significativos (p<0,05), apresentando o mesmo perfil de comportamento observado
para a capacidade antioxidante.
Comparando os resultados para o CFT e capacidade antioxidante dos extratos de S.
officinalis obtidos pela extração exaustivamente com acetona (3111 mg EAG/100 g;
177 µmol Trolox/g, respectivamente) e pela melhor condição do delineamento
experimental (T7) (5596 mg EAG/100 g; 378 µmol Trolox/g, respectivamente), o
qual foi assistido por micro-ondas, é possível observar que o método clássico
apresentou resultados inferiores quando comparados com aqueles em que se
utilizou o glicerol como solvente e o aquecimento por micro-ondas (p<0,05). A
abordagem proposta por esse trabalho resultou em um extrato duas vezes mais
antioxidante. Portanto, o método de extração assistido por micro-ondas
utilizando glicerol se mostrou mais eficiente na extração de compostos bioativos
para esta planta.
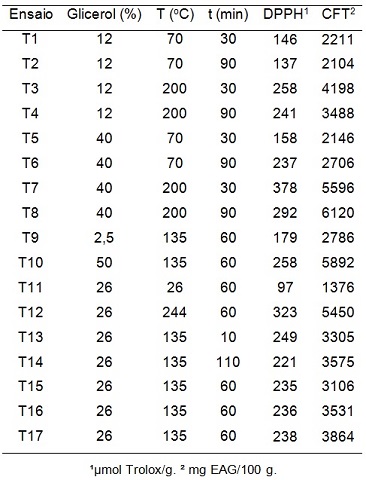
Condições operacionais para a extração sólido- líquido assistida por micro-ondas dos compostos bioativos da Salvia officinalis.

Diagrama de Pareto para a capacidade antioxidante (DPPH•) e CFT.
Conclusões
A extração assistida por micro-ondas utilizando uma solução com 40% de glicerol,
temperatura de 200 ºC por 30 minutos foi o mais eficiente na recuperação dos
compostos antioxidantes da S. officinalis, sendo destacada a influência
significativa da temperatura e da concentração de glicerol sobre as respostas
avaliadas no delineamento experimental. Os resultados obtidos por essa abordagem
foram maiores que aqueles encontrados para a extração exaustiva com acetona 70%.
Desse modo, o método proposto se mostrou promissor para a recuperação dos
compostos bioativos da S. officinalis, se destacando por usar o glicerol, que além
de ser um solvente verde e abundante, após a extração, apresenta-se como um
veículo de compostos antioxidante que pode ser empregado diretamente em
formulações cosméticas e alimentícias.
Agradecimentos
Ao CNPQ pelo auxílio financeiro;
Ao INT pela estrutura laboratorial e aos colaboradores do LAQOI pela contribuição
para este trabalho.
Referências
ALTINDAL, D., ALTINDAL, N. Sage (Salvia Officinalis) Oils. In: PREEDY, V. R. Essential Oils in Food Preservation, Flavor and Safety. Londres: Editora Elsevier, 2016. cap. 81, p.715-721.
BARATTA, M. T.; DORMAN, D.; DEANS, S. G.; BIONDI, D. M.; RUBERTO, G. Chemical Compositon, Antimicrobial and Antioxidantive Activity of Laurel, Sage, Rosemary, Oregano and Coriander Essential Oils. Journal of Essential Oil Research, nº 10, 618-627, 1998.
BENER, M.; ŞEN, F. B.; ÖNEM, A. N.; BEKDEŞER, B.; ÇELIK, S. E.; LALIKOGLU, M.; AŞÇI, Y. S.; CAPANOGLU, E.; APAK, R. Microwave-assisted extraction of antioxidant compounds from by-products of Turkish hazelnut (Corylus avellana L.) using natural deep eutectic solvents: Modeling, optimization and phenolic characterization. Food Chemistry, nº 385, 132633, 2022.
DRAGOVI´C-UZELAC, V.; GAROFULIĆ, I. E.; JUKIĆ, M.; PENIĆ, M.; DENT, M. The influence of microwave- Assisted Extraction on the Isolation of Sage (Salvia Officinalis L.) Polyphenols. Food Technology and Biotechnology. nº 50, 377-383, 2012.
GHORBANI, A.; ESMAEILIZADEH, M. Pharmacological properties of Salvia officinalis and its components. Journal of Traditional and Complementary Medicine, nº 7, 433-440, 2017.
HASHEMI, B.; SHIRI, F.; ŠEVEC, F.; NOVÁKOVÁ, L. Green solvents and approaches recently applied for extraction of natural of bioactive compounds.Trends in Analytical Chemistry, nº 157,116732,2022.
HIDALGO, M.; SÁNCHEZ-MORENO, C.; PASCUAL-TERESA, S. DE. Flavonoid-flavonoid interaction and its effect on their antioxidant activity. Food Chemistry, 121, 691-696,2010.
KASHYAP, P. K.; SINGH, SWATI.; SINGH, S.; SINGH, M. K.; GUPTA, A.; TANDON, S.; SHANKER, K.; VERMA, R. K.; VERMA, R. S. An efficient process for extraction of lutein and chemical characterization of other organic volatiles from marigold ( Tagetes erecta L.) flower. Food Chemistry, nº 396, 133647, 2022.
LÄNGER, R.; MECHTLER, CH.; JURENITSCH, J. Composition of the Essential Oils of Commercial Samples of Salvia Officinalis L. and S. fruticosa Miller: A Comparison of Oils Obtained by Extraction and Steam Distillation. Phytochemical Analysis, nº 7, 289-293, 1996.
MALEŠ, I.; DRAGOVI´C-UZELAC, V.; JERKOVI´C, I.; ZORI´C, Z.; PEDISI´C, S.; REPAJI´C, M.; GAROFULI´C, I. E.; DOBRINCI´C, A. Antioxidants. Non Volatile and Volatile Bioactives of Salvia Officinalis L., Thymus serpyllum L. and Laurus nobilis L. Extracts with Potential Use in the Development of Functional Beverages. Antioxidants, nº 11; 1140 (1-20), 2022.
MAZAUD, A .; LEBEUF, R.; LAGUERRE, M.; NARDELLO-RATAJ, V. Improved Hydrotropic Extraction of Carnosic Acid from Rosemary and Sage with Short-Chain Monoalkyl Glycerol Ethers. ACS Sustainable Chemistry & Engineering, nº 10, 3673-3681, 2022.
MONTEIRO, M. R.; KUGELMEIER, C. L.; PINHEIRO, R. S.; BATALHA, M. O.; CÉSAR, A. DA S. Glycerol from biodiesel production: Technological paths for sustainability. Renewable and Sustainable Energy Reviwes, nº 88, 109-122, 2018.
WALCH, S. G.; KUBALLA, T.; STÜHLINGER, W.; LACHENMEIER, D. W. Determination of the biologically active flavor substances thujone and camphor in foods and medicines containing sage (Salvia Offcinalis L.). Chemistry Central Journal, nº 5, 2-10,2011.
PINTO, E.; SALGUEIRO, L. R.; CAVALEIRO, C.; PALMEIRA, A.; GONÇALVES, M, J. In vitro susceptibility of some species of yeasts and filamentous fungi to essential oils of Salvia Officinalis. Industrial Crops and Products, nº 26, 135-141,2007.
SINGLETON, V. L.; ROSSI, J. A. Colorimetry of Total Phenolics with Phosphomolybdic-Phosphotungstic Acid Reagents. American Journal of Enology and Viticulture, 16, 144-158, 1965.
ZEKOVIĆ, Z.; PINTAĆ, D.; MAJKIĆ, T.; VIDOVIĆ, S.; DUKIĆ-MIMICA, N.; TESLIĆ, N.; VERSARI, A.; PAVLIĆ, B. Utilization of sage by-products as raw material for antioxidants recovery – Ultrassound versus microwave-assisted extraction. Industrial Crops and Products, nº 99, 49-59, 2017.
















