Autores
Santos, P.L.L. ((UEMA)) ; Silva, L.G.P. ((UEMA)) ; Ferreira, L.A. ((UEMA)) ; Gomes, T.F. ((UEMA)) ; Gonçalves, J.C.S. ((UEMA)) ; Oliveira, A.L.T. ((UEMA)) ; Fernandes, R.M.T. ((CECEN/UEMA)) ; Khan, A. ((CECEN/UEMA))
Resumo
A escolha por um bom propelente é muito importante para o projeto de um motor
foguete. Nesse estudo avaliamos as características termodinâmicas para determinar
os parâmetros da taxa para a reação de dissociação e abstração nas reações de
decomposição das moléculas de estudo. Utilizou-se o programa Gaussian para a
geração dos cálculos com o método DFT com função de base cc-pVDZ. Com a obtenção
dos resultados inferiu-se que reações se apresentaram com liberação de calor e em
determinadas temperaturas houve absorção de calor, em relação a variação de
entropia e energia livre de Gibbs inferiu-se que as reações se apresentaram com um
grande grau de desordem e espontaneidade. Concluímos que a técnica de reação
Isodésmicas tem muito sucesso em determinar os tipos de reações de combustão.
Palavras chaves
: Termodinâmica; Decomposição térmica; DFT
Introdução
A humanidade desde cedo tem a curiosidade sobre a busca do desconhecido, essa
afirmação comprovasse com as explorações e estudos nas áreas aeroespaciais,
desde modo a escolha por um bom propelente é muito importante para o projeto de
um motor foguete. As características desejadas para um propelente é alto
desempenho e taxa de queima previsível. (PINTO, Bianca Caroline et al. p. 35-37,
2016) Os estudos acerca da química computacional obtiveram uma grande evolução
com o passar dos anos, pois a mesma reduz os custos experimentais de uma
pesquisa. A propulsão de foguetes deve liberar quantidades consideráveis de
energia. A hidrazina (N2H4) têm sido amplamente utilizados como combustível em
motores de foguete devido suas propriedades físicas adequadas como:
endotermicidade, e reatividade extremamente alta com vários oxidantes. (VENTURA,
Ocar. p.329, 2000).
A evolução da química quântica computacional tornou-se uma ferramenta bem
poderosa para adquirir grandezas termoquímicas com o aparecimento de métodos de
cálculo baseados na teoria dos funcionais de densidade (DFT) possibilita o
cálculo de propriedades termoquímicas que comparam bem com os valores
experimentais e conseguindo uma precisão excelente. (KUZNETSOV, pág. 2833-2839,
2015). Objetivo desse trabalho foi realizar uma avaliação termoquímica e
cinética da decomposição térmica das matérias de alta energias em busca de
descrever um mecanismo da reação elementar para determinar as propriedades
termoquímicas e ligações energéticas, da decomposição das várias estruturas das
matérias de alta energia utilizando o método DFT.
Material e métodos
Foram criadas três reações isodésmicas para molécula da hidrazina, por ser
reações hipotéticas onde os átomos e os tipos de ligações que se formam nos
produtos devem ser os mesmos nos reagentes. Todas as geometrias foram criadas
pelo programa GaussView considerando os comprimentos para cada ligação entre N-
N, N-H, O-O, N-O, O-H. Para cada molécula presente nas reações I, II, III, levou
em torno de trinta minutos para ser calculada. Todos os cálculos pelo programa
Gaussian utilizando método DFT (B3LYP) com função de base cc-pVDZ (DUNNING Jr.
T.H. 1989) nas temperaturas 100K, 298K, 500K e 1000K e extraindo do arquivo de
saída os seguintes resultados: Entalpia, Energia Livre de Gibbs, Entropia.
Organizando todos os dados no programa Excel e em seguida criando os gráficos
para a molécula de estudo nas temperaturas de 100K, 298K, 500K e 1000K. O
programa manuseado para criação dos gráficos foi o Origin. De posse dos
resultados termodinâmicos calculamos a constante de equilíbrio e a decomposição
térmica para determinar qual a melhor reação isodésmicas e finalmente determinar
a cinética química através do mecanismo de reação. As geometrias da decomposição
térmica das moléculas de estudo foram geradas no programa GaussView e calculada
pelo Gaussian para determinar qual a melhor temperatura da decomposição.
Resultado e discussão
A variação de entalpia é definida termodinamicamente como sendo a quantidade de
calor trocada a pressão constante. Para representar que o calor foi liberado uma
das formas utilizadas é ∆
Reações Isodésmicas da molécula Hidrazina
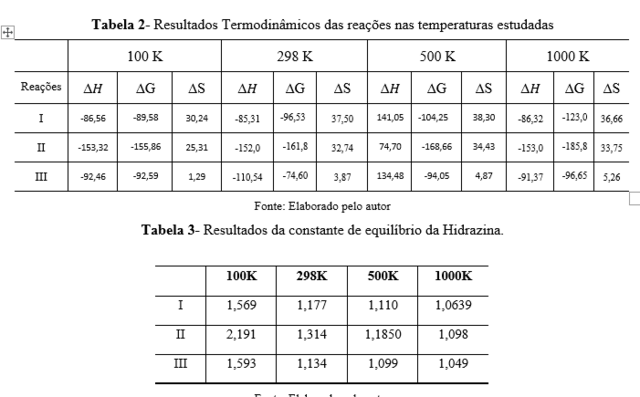
Resultados Termodinâmicos das reações nas temperaturas estudadas e Resultados da constante de equilíbrio da Hidrazina.
Conclusões
De posse dos resultados obtidos através do método DFT (B3LYP) com função de base
cc-pVDZ conclui-se que a técnica de reação Isodésmicas tem muito sucesso em
determinar os tipos de reações de combustão esclarecendo quais das reações estão
envolvidas na absorção do calor produzido durante o processo. As reações II e III
apresentaram-se maior liberação de calor, maior espontaneidade e maior desordem.
Na decomposição térmica apresentaram ser mais espontaneidade à medida que a
temperatura aumenta, sendo 1000K a melhor temperatura.
Agradecimentos
À UEMA pela concessão da bolsa e pelo fomento da pesquisa. Ao Laboratório de
Físico-Química da UEMA. Ao programa de Iniciação Científica – PIBIC/UEMA e ao
professor Alamgir Khan.
Referências
MAHAN, B., M.; MYERS, R., J.; Química um curso universitário, 4ª edição, Edgard Blücher, 1996.
PINTO, Bianca Caroline et al. FOGUETES TRIPULADOS. Anais da Mostra de Ensino, Pesquisa, Extensão e Cidadania (MEPEC), v. 1, p. 35-37, 2016.
Ribeiro, D., (2015) Entropia, Rev. Ciência Elem., V3(4):226
PINTO, Leandro Moreira de Campos. A teoria do funcional da densidade na caracterização de fases intermetálicas ordenadas. 2009.
JARDINO FILHO, Sergio Augusto. Estudo computacional de cetonas de Cookson e derivados. 2001.
DUNNING Jr. T.H., “Gaussian basis sets for use in correlated molecular calculations. I. The atoms boron through neon and hydrogen,” J. Chem. Phys., 90 (1989) 1007-23. DOI: 10.1063/1.456153;
O. N. Ventura, M. Kieninger, R. E. Cachau, S. Suhai, Chem. Phys. Lett. 329 (2000) 145.
















