ÁREA
Química Ambiental
Autores
Teixeira, Y.N. (URCA) ; Bentes, E.M. (UFCA) ; Feitosa, G.B. (UFCA) ; Sousa, H.S. (IFCE) ; Faustino, F.W. (UFCA) ; Lima, J.N.M. (URCA) ; Oliveira, E.A. (URCA) ; Menezes, J.M.C. (UFCA) ; Teixeira, R.N.P. (URCA) ; Paula Filho, F.J. (UFCA)
RESUMO
O propósito deste estudo consistiu em analisar o impacto das variáveis de temperatura de precipitação, temperatura de calcinação e tempo de calcinação no processo de síntese da ferrita de cálcio (CaFe2O4), visando à remoção de fosfato (PO43-). Além disso, buscou-se investigar a influência da dosagem de CaFe2O4, concentração inicial de PO43- e pH do meio. A otimização do procedimento envolveu a aplicação da metodologia de superfície de resposta, com o intuito de determinar os valores ótimos para cada parâmetro tanto na etapa de síntese quanto de adsorção. Os resultados revelaram capacidade de adsorção de até 21,82 mg/g e eficiência de remoção de PO43- de até 96,76%, o que atesta a notável capacidade da CaFe2O4 em remover o íon PO43- da água.
Palavras Chaves
Adsorção; Fosfato; Otimização
Introdução
Globalmente, há um esforço contínuo para avançar nas pesquisas que visam criar tecnologias e materiais ecologicamente sustentáveis. Essas inovações têm o propósito de substituir os polímeros sintéticos no contexto do tratamento de água. Grande parte das águas residuais é lançada no meio ambiente sem passar por processos de tratamento adequados. Esse cenário resulta na propagação da poluição de forma significativa (BAWIEC, 2019). Dentre a poluição por excesso de nutrientes, o PO43- desempenha um papel fundamental como o principal nutriente desencadeador do processo de eutrofização (OZACAR, 2003). Diante disso, várias pesquisas investigam procedimentos para a remoção do PO43- de matrizes líquidas. A remoção pode ser por processos químicos (precipitação e adsorção), processos físicos (microfiltração e osmose reversa) e processos biológicos (assimilação e estabilização) (SANTOS, 2018). Entre essas alternativas, a adsorção destaca-se por oferecer várias vantagens em comparação com as demais alternativas, incluindo custos operacionais reduzidos, manuseio simplificado e notável eficácia. Ferritas ecológicas emergem como candidatas promissoras no contexto do tratamento de efluentes por meio da adsorção. Entre as ferritas, a variação de cálcio (CaFe2O4), demonstra qualidades de biocompatibilidade, baixa toxicidade e a capacidade de ajuste de suas propriedades magnéticas (DEBNATH et al., 2016; GHANBARI et al., 2015). Assim sendo, o objetivo central desta pesquisa foi avaliar como as variáveis de temperatura de precipitação, temperatura de calcinação e tempo de calcinação afetam o processo de síntese da CaFe2O4, com foco na eficiência de remoção do PO43-. Adicionalmente, explorou-se a influência da dosagem de CaFe2O4, da concentração inicial de PO43- e do pH do meio.
Material e métodos
CaFe2O4 foi sintetizada através do método de co-precipitação (DAS, 2021). Os precursores usados foram: FeCl3, CaCl2.2H2O e NaOH. A reação de síntese é apresentada na Equação 1. 2FeCl3 + CaCl2 + 8NaOH → CaFe2O4↓ + 4H2O + 8NaCl 1 Após a etapa de precipitação, a CaFe2O4 foi lavada até atingir um pH neutro. A separação da CaFe2O4 do meio foi realizada por centrifugação. Em seguida, o material foi seco (110°C por 2 horas). Posteriormente, foi executada a calcinação. KH2PO4 foi utilizado para preparar o efluente sintético contaminado por PO43-. A eficiência de remoção (Remoção) e a capacidade de adsorção (qeq) foram calculadas usando as equações 2 e 3, respectivamente. Remoção = ((Co-Ceq)/Co)100 2 qeq = ((Co-Ceq)/m)V 3 Onde: Co e Ceq são as concentrações de PO43- inicial e no equilíbrio (mg/L), respectivamente; m é a massa de CaFe2O4 utilizada (g) e V o volume de cada amostra (L). Em todos os experimentos foi utilizado um volume de 50 mL por amostra. O tempo de equilíbrio foi 90 minutos. O software RStudio foi empregado para analisar os resultados experimentais e otimizar o processo. O planejamento adotado foi o Box-Behnken devido à sua eficiência e economia, necessitando de poucos experimentos para resultados robustos. Para a síntese, avaliaram-se os parâmetros: temperatura de precipitação (30, 60 e 90 °C), temperatura de calcinação (200, 300 e 400 °C) e tempo de calcinação (2, 3 e 4 horas). Na etapa de adsorção, investigaram-se: dosagem de CaFe2O4 (0,5; 1,5 e 2,5 g/L), concentração inicial de PO43- (10, 50 e 90 mg/L) e pH (4, 7 e 10).
Resultado e discussão
Na Figura 1, os primeiros parâmetros a serem avaliados foram os efeitos das
temperaturas de precipitação e calcinação (A1). Pode-se concluir que o aumento
da temperatura do sistema durante a etapa de precipitação aumenta a capacidade
de adsorção de PO43-. O comportamento contrário é observado em relação a
temperatura de calcinação, ou seja, o aumento da temperatura de calcinação
desfavorece a adsorção de PO43-.
Os efeitos de temperatura de precipitação e tempo de calcinação (B1) nos indicam
que o aumento no tempo de calcinação aumenta a capacidade de adsorção de PO43-.
Os efeitos de temperatura de calcinação e tempo de calcinação (C1) apresentam
comportamento de cela, ou seja, não apresenta ponto de mínimo nem de máximo.
Logo, foi utilizada a otimização restrita, apresentada na Figura 1 (A2, B2 e
C2), onde encontramos que, para otimizar a síntese, devemos precipitar CaFe2O4 a
90 °C e calcinar por 4 horas a uma temperatura de 313 °C. Essas condições
maximizam a capacidade de adsorção de PO43-.
Na Figura 2, os primeiros parâmetros a serem avaliados foram os efeitos da
dosagem e concentração inicial (A1). Pode-se concluir que o aumento da dosagem
aumenta a remoção de PO43-. O aumento da concentração inicial de PO43- diminui a
eficiência de remoção.
Os efeitos de dosagem e pH (B1) nos indicam que a diminuição do pH no meio
aumenta a remoção de PO43-. Os efeitos de pH e concentração inicial de PO43-
(C1) nos indicam que quanto menor a concentração de PO43- e menor o pH do meio,
maior será a remoção. Através da otimização restrita, apresentada na Figura 2
(A2, B2 e C2), encontramos que a CaFe2O4 é mais eficiente em remover PO43- em
dosagens maiores (2,5 g/L), concentrações menores de PO43- (10 mg/L) e pH ácido
(pH = 4).
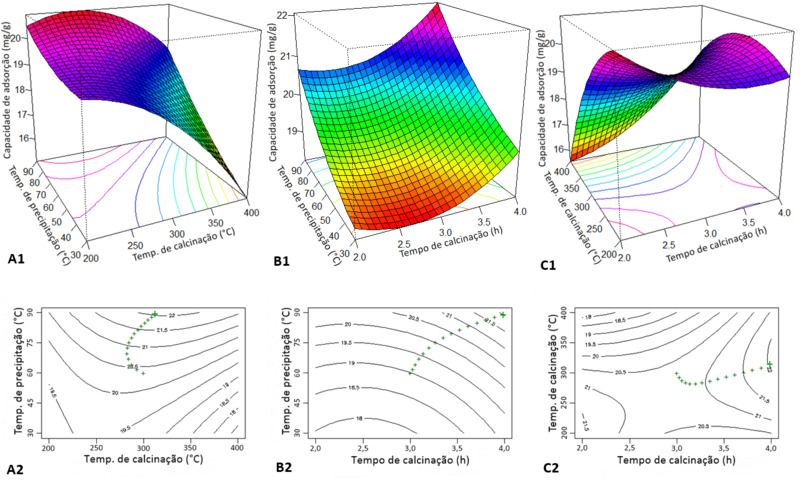
Otimização do processo de síntese para maximizar a \r\ncapacidade de adsorção de PO43-.
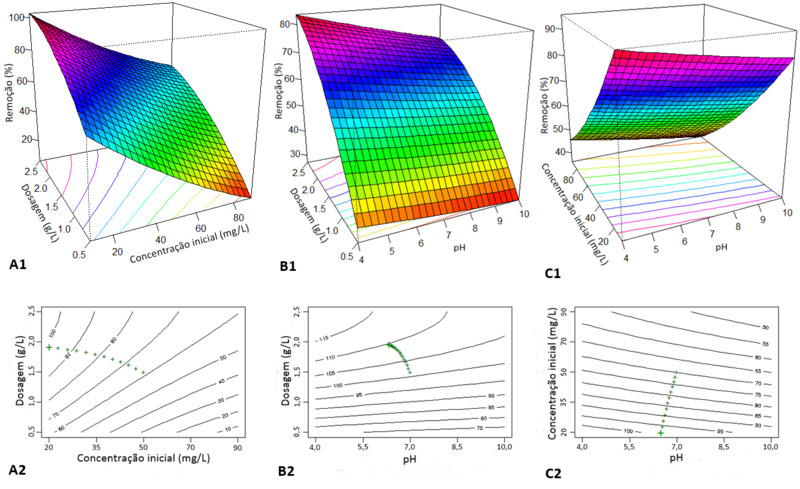
Otimização dos parâmetros de adsorção para maximizar \r\na remoção de PO43-.
Conclusões
Portanto, a capacidade de adsorção de PO43- usando CaFe2O4 é otimizada quando a temperatura usada durante a precipitação é 90 °C, o tempo de calcinação 4 h e a temperatura de calcinação 313 °C. A eficiência de remoção de PO43- é otimizada quando se utiliza dosagens maiores de CaFe2O4, concentração iniciais menores de PO43- e pH ácido. Ademais, esses são os primeiros resultados de uma pesquisa promissora, demonstrando que a CaFe2O4 pode ser sintetizada por uma rota simplificada, além de apresentar uma excelente capacidade de remover PO43- da água.
Agradecimentos
A Fundação Cearense de Apoio ao Desenvolvimento Científico e Tecnológico - FUNCAP, pelas bolsas BP5-0197-00133.01.00/22 e BMD-0008-00480.01.29/23.
Referências
BAWIEC, A. Efficiency of nitrogen and phosphorus compounds removal in hydroponic wastewater treatment plant. Environmental Technology, v. 40(16), 2062–2072, 2019.
DAS, P.; DEBNATH, A. Reactive orange 12 dye adsorption onto magnetically separable CaFe2O4 nanoparticles synthesized by simple chemical route: kinetic, isotherm and neural network modeling. Water Practice & Technology, v. 16(4), 1141-1158, 2021.
DEBNATH, A. et al. Enhanced Adsorption of Hexavalent Chromium onto Magnetic Calcium Ferrite Nanoparticles: Kinetic, Isotherm, and Neural Network Modeling. Journal of Dispersion Science and Technology, v. 37(12), 1806-1818, 2016.
GHANBARI, D. et al. Electro-spinning of cellulose acetate nanofibers: microwave synthesize of calcium ferrite nanoparticles and CA–Ag–CaFe2O4 nanocomposites. Journal of Materials Science: Materials in Electronics, v. 26, 8358-8366, 2015.
MOR, S.; et al. Municipal solid waste characterization and its assessment for potential methane generation: a case study. Science of the Total Environment, v. 371(1a), 1-10,
2006.
OLIVEIRA, M.; MACHADO, A. V.; NOGUEIRA, R. Phosphorus Removal from Eutrophic Waters with an Aluminium Hybrid Nanocomposite. Water, Air, & Soil Pollution, v. 223(8), 4831–4840, 2012.
OZACAR, M. Adsorption of phosphate from aqueous solution onto alunite. Chemosphere, v. 51(4), 321–327, 2003.
RAVINDRA, K.; KAUR, K.; MOR, S. System analysis of municipal solid waste
management in Chandigarh and minimization practices for cleaner emissions. Journal of Cleaner Production, v. 89, 251-256, 2015.
SANTOS, A. F. F. Recuperação de fósforo de efluentes líquidos por processos de adsorção. Dissertação de Mestrado. Universidade de Coimbra – UC, Coimbra, 2018.
WIUM-ANDERSEN, T. et al. Modeling the eutrophication of two mature planted
stormwater ponds for runoff control. Ecological Engineering, v. 61(part B), 601–613, 2013.