Autores
Macedo, M.A.M. (IFPB) ; Miranda, S.M.M. (IFPB) ; Andrade, S.R.A. (IFPB) ; Lucena, D.V. (IFPB) ; Clarice Oliveira, R. (IFPB)
Resumo
Este trabalho tem como objetivo explanar aos discentes de como é determinado o teor de etanol anidro combustível (EAC) na gasolina tipo C comercializada em postos de serviços, de acordo com a NBR 13993. A aula experimental abordou sobre a questão ambiental; a legislação vigente; a solubilidade do álcool com a solução utilizada (NaCl, 10%), as ligações polares e apolares, cada aluno recebeu impressa a norma supracitada. O resultado foi bastante satisfatório, o desvio padrão foi de 1,41%, indicando que todos os discentes conseguiram entender o experimento, observaram de como ocorre a solubilidade do álcool com a solução de NaCl, da importância das ligações polares e apolares. E compreenderam como se obtêm e o porquê dos 27% de EAC na gasolina, de acordo com a Resolução ambiental.
Palavras chaves
Gasolina; teor de etanol; interdisciplinaridade
Introdução
Transmitir ao aluno em sala de aula o conteúdo relacionado ao seu curso técnico e levá-lo para o laboratório, relacionando com a química, faz o aluno ter mais interesse em ambas as áreas. O discente se mostra mais interessado ao conteúdo ministrado, a ter mais questionamento sobre as áreas e, principalmente, o aprendizado torna-se mais efetivo. O assunto abordado em aula foi sobre a gasolina automotiva, que é o combustível mais popular no país, utilizada em motores de combustão interna, de veículos de pequeno a médio porte. Ela é comercializada em postos de serviços, sua composição é de 4 a 12 átomos de carbono por molécula, composta também de olefinas, cicloparafinas e aromáticos (MINATTI, 2009; DEVOLD, 2013). Um dos critérios a serem abordados foi o teor de 27 % (vinte e sete por cento) de etanol anidro combustível (EAC) na gasolina, conforme a Resolução do Conselho Interministerial do Açúcar e do Álcool (CIMA), nº 1, de 31 de agosto de 2011, sendo aceitável uma margem de erro de mais ou menos 1%, conforme disposto no Art. 1°, da Lei 10.203/2001 (ANP, 2017). Esse teor é, principalmente, para diminuir os gases tóxicos emitidos pelo carro durante a combustão, já que a combustão do etanol é bem mais limpa. Então, qual a importância de se analisar esse teor nas gasolinas comercializadas nos postos de serviços? Infelizmente, no Brasil, existe a prática de adulteração nesse teor e passar para o aluno os danos que esse método traz faz com que eles tenham uma visão dos impactos econômicos e ambientais, bem como o aumento de emissões tóxicas, maior perda na arrecadação de impostos, lucros ilegais e defeitos no veículo. A NBR 13993 (ASSOCIAÇÃO..., 2002) aborda sobre a determinação do teor de etanol anidro combustível na gasolina, que foi utilizada na aula experimental.
Material e métodos
A aula prática foi realizada no Laboratório de Processamento Primário de Fluidos e Análises Minerais (LABFLUIDOS), no Instituto Federal da Paraíba (IFPB), no campus de Campina Grande, do Curso Técnico Integrado em Petróleo e Gás. A turma concluinte (3º ano) foi dividida em grupos e cada experimento foi realizado por dois discentes, totalizando 16 duplas. Inicialmente, expôs-se uma breve abordagem teórica sobre: ligações químicas, solubilidade, refino, combustíveis, gasolina, composição, teor de etanol anidro combustível na gasolina, adulteração e resoluções. Para a obtenção dos resultados, foi utilizada a NBR 13993 (ASSOCIAÇÃO..., 2002), a amostra de gasolina foi adquirida num posto de serviço na cidade de Campina Grande-PB. Colocou-se 50 mL da amostra (gasolina) na proveta de 100 mL previamente limpa, desengordurada e seca. Adicionou-se a solução de NaCl (10% m/v) em outra proveta de 50 mL e adicionou-se na proveta com gasolina. Tampou-se a proveta e inverteu-se por dez vezes, evitando agitação enérgica, para completar a extração do álcool pela camada aquosa. Deixou-se em repouso por 15 minutos, a fim de permitir a separação completa das duas camadas. Anotou-se o volume final da camada aquosa, em mililitros. Por fim, calculou-se o teor de AEAC presente na amostra, utilizando a seguinte equação: AEAC = [(A x 2] + 1 [% em volume], em que: A é o volume final da camada aquosa, em mililitros (ASSOCIAÇÃO..., 2002). Para se verificar a precisão dos resultados, foram calculados a média e o desvio padrão. Cada aluno calculou seu teor de EAC na gasolina de acordo com a equação citada, depois calcularam a média e o desvio padrão da aula experimental.
Resultado e discussão
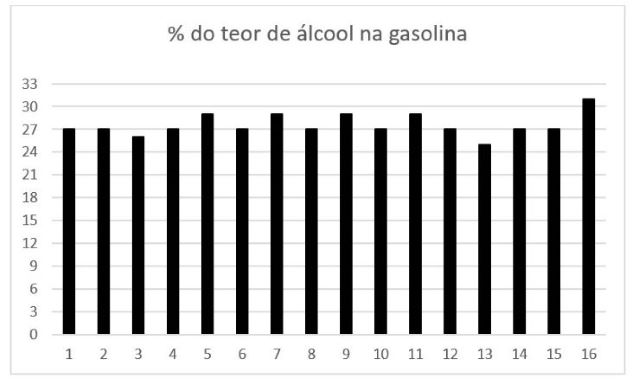
Os resultados obtidos de cada discente do teor de álcool na gasolina estão
apresentados na Figura 1. Os alunos calcularam o Desvio-padrão = 1,41% e a
Média amostral = 27,6 %. A média sozinha não é suficiente para avaliar a
precisão de um conjunto de dados, é importante avaliar o grau de dispersão dos
dados através do cálculo do desvio-padrão, o qual avalia a diferença (desvio)
entre a média e os valores obtidos. A média foi bem próxima do teor de etanol
anidro permitido pela legislação que é de 27%, a média foi de 27,6%, o desvio
padrão foi bem baixo, indicando que os alunos entenderam, interpretaram e
executaram da melhor maneira a prática e os resultados obtidos. Os discentes
puderam ver como atua a solubilidade de diferentes substâncias, que podem ser
explicadas por meio dos conceitos das ligações polares e apolares. A partir
desses conceitos, os discentes puderam entender o fenômeno pelo qual o etanol
se solubilizou na solução de cloreto de sódio, provocando um aumento no volume
da fase aquosa, o qual permite determinar o real teor de etanol anidro
combustível na gasolina, comprovando se há ou não adulteração. Desta forma, a
referida aula prática mostra a importância da experimentação no processo
ensino-aprendizagem, despertando sempre curiosidade dos discentes e uma maior
interação aluno-conteúdo-professor nas aulas experimentais.
Conclusões
Pode-se afirmar que as aulas experimentais são essenciais para o aprendizado, fazendo com que o discente tenha mais interesse no conteúdo abordado, uma vez que em sala de aula ele usa a imaginação, já no laboratório sua compreensão é maior pois ele visualiza, manuseia e executa o experimento, obtendo assim resultados que fazem entender o assunto abordado. A obtenção do teor de etanol anidro combustível na gasolina faz o aluno ter uma visão diferente de como ocorre a adulteração, dos danos causados por essa ação e, principalmente, como a química é importante para tal comprovação.
Agradecimentos
Ao Instituto Federal de Educação, Ciência e Tecnologia da Paraíba (IFPB).
Referências
ANP - AGÊNCIA NACIONAL DO PETRÓLEO GÁS NATURAL E BIOCOMBUSTÍVEL. Gasolina. 2017. Disponível em: <http://www.anp.gov.br/petroleo-derivados/155-Combustiveis/1855-gasolina>. Acesso em : 29 maio de 2019. ASSOCIAÇÃO BRASILEIRA DE NORMAS TÉCNICAS. NBR 13993: Álcool etílico combustível - Determinação do teor de gasolina, 2002. DEVOLD, H. Oil and gas production handbook An introduction to oil and gas production, transport, refining and petrochemical industry. Edition Oslo: 2013. MINATTI, E. O que é gasolina, 2009. Disponível em: <http://www.qmc.ufsc.br/qmcweb/artigos/gasolina.html >, acesso em 02 de maio de 2019.

